
Wetenschap
Wat betekent dat het als zuur of base kan werken?
Dit betekent dat ze protonen kunnen doneren of accepteren, afhankelijk van de omgeving waarin ze zich bevinden.
In een zure omgeving zullen ze als base fungeren en protonen accepteren.
In een basische omgeving gedragen ze zich als een zuur en doneren ze protonen.
Water is bijvoorbeeld een amfotere stof. In zuiver water zijn er een gelijk aantal waterstofionen (H+) en hydroxide-ionen (OH-). Dit komt omdat water een proces van zelfionisatie kan ondergaan, waarbij een watermolecuul zich splitst in een waterstofion en een hydroxide-ion. Wanneer water met een zuur wordt gemengd, zullen de waterstofionen uit het zuur reageren met de hydroxide-ionen uit het water om meer watermoleculen te vormen. Dit zal het aantal hydroxide-ionen in het water verminderen en de oplossing zuurder maken. Wanneer water met een base wordt gemengd, zullen de hydroxide-ionen uit de base reageren met de waterstofionen uit het water om meer watermoleculen te vormen. Dit zal het aantal waterstofionen in het water verminderen en de oplossing basisch maken.
 Houdt de Europese haagbeuk de bladeren de hele winter vast, net als de piramide-eik?
Houdt de Europese haagbeuk de bladeren de hele winter vast, net als de piramide-eik?  Nieuwe studie toont aan dat de Amazone zijn eigen regenseizoen maakt
Nieuwe studie toont aan dat de Amazone zijn eigen regenseizoen maakt NASA vangt vorming van tropische cycloon Kenneth in de buurt van Aldabra
NASA vangt vorming van tropische cycloon Kenneth in de buurt van Aldabra NOAA-tool brengt nu rampenrisico en kwetsbaarheid naar gemeenschapsniveau
NOAA-tool brengt nu rampenrisico en kwetsbaarheid naar gemeenschapsniveau Opkomst van dinosaurussen gekoppeld aan toenemende zuurstofniveaus
Opkomst van dinosaurussen gekoppeld aan toenemende zuurstofniveaus
Hoofdlijnen
- Waarom zijn de nakomelingen van oudere moeders minder geschikt om lang en voorspoedig te leven?
- Heeft de gezondheidsstatus van de vader bij muggen invloed op de resultaten van de nakomelingen van de moeder?
- Wat is een eencellige eukaryoot?
- Koolwaterstofafbrekende schimmel geeft zijn geheimen prijs
- Natuur versus laboratorium:de verschillen tussen experimentele evolutie en natuurlijke aanpassing
- Hoe grassen inteelt vermijden
- Droombetekenissen uitgelegd
- Waarom wordt natrium gebruikt in DNA-extractie?
- Is menselijke groei een fysieke of chemische verandering?
- Onderzoekers analyseren hoe 3D-geprinte metalen breken

- Wetenschappers onthullen verborgen katalytisch oppervlak van Ni-Au-kernschil in kooldioxidehydrogenering

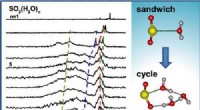
- Wetenschappers onthullen stapsgewijze hydratatiemotieven van zwaveldioxide
- Wetenschappers ontrafelen het mysterie van hoe straling metaal verzwakt, één atoom tegelijk

- Wetenschappers gebruiken nieuwe technologieën om water te zien als nooit tevoren

 Studie ontdekt waarom guppies kleurrijk zijn
Studie ontdekt waarom guppies kleurrijk zijn  Innovatie en speculatie stimuleren de zeepbelactiviteit op de aandelenmarkt, volgens nieuwe studie
Innovatie en speculatie stimuleren de zeepbelactiviteit op de aandelenmarkt, volgens nieuwe studie Geologen laten een ongekende opwarming van het Tanganyikameer zien
Geologen laten een ongekende opwarming van het Tanganyikameer zien  Hoe de klimaatverandering in de landbouw te bestrijden en tegelijkertijd banen te beschermen?
Hoe de klimaatverandering in de landbouw te bestrijden en tegelijkertijd banen te beschermen? Wetenschappers produceren hoogwaardig gips volledig uit afval
Wetenschappers produceren hoogwaardig gips volledig uit afval De voedsel- en watersystemen die astronauten nodig hebben om naar plaatsen zoals Mars te reizen
De voedsel- en watersystemen die astronauten nodig hebben om naar plaatsen zoals Mars te reizen Wetenschappers ontsluiten het geheim van wat planten doet bloeien
Wetenschappers ontsluiten het geheim van wat planten doet bloeien  Links versus rechts is dood:politiek gaat over anarchisten versus centristen, nieuwe CAGE-studieshows
Links versus rechts is dood:politiek gaat over anarchisten versus centristen, nieuwe CAGE-studieshows
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

