
Wetenschap
Hoe toon je aan dat een chemische vergelijking in evenwicht is?
Hier is een voorbeeld van een uitgebalanceerde chemische vergelijking:
CH₄ + 2O₂ → CO₂ + 2H₂O
In deze vergelijking kunnen we zien dat er aan beide zijden 1 koolstofatoom is, aan beide zijden 4 waterstofatomen en aan beide zijden 2 zuurstofatomen. Dit betekent dat de vergelijking in evenwicht is.
Als een vergelijking niet in evenwicht is, kunt u deze in evenwicht brengen door coëfficiënten toe te voegen vóór de reactanten en producten. Coëfficiënten vertellen ons hoeveel moleculen of mol van elke stof bij de reactie betrokken zijn.
Hier is een voorbeeld van hoe je een onevenwichtige vergelijking in evenwicht brengt:
2H₂ + O₂ → H₂O
In deze vergelijking zijn er 4 waterstofatomen aan de linkerkant en slechts 2 waterstofatomen aan de rechterkant. Om de vergelijking in evenwicht te brengen, kunnen we een coëfficiënt van 2 toevoegen vóór de H₂O:
2H₂ + O₂ → 2H₂O
Nu is de vergelijking in evenwicht, aangezien er nu aan beide kanten 4 waterstofatomen zijn.
 Waarom scheren zelfs de scherpste scheermessen dof maakt
Waarom scheren zelfs de scherpste scheermessen dof maakt Wetenschappers breiden PET-beeldvormingsopties uit door eenvoudigere chemie
Wetenschappers breiden PET-beeldvormingsopties uit door eenvoudigere chemie Een op fysica gebaseerd voorspellend hulpmiddel om het onderzoek naar batterijen en supergeleiders te versnellen
Een op fysica gebaseerd voorspellend hulpmiddel om het onderzoek naar batterijen en supergeleiders te versnellen  Wat is de molaire massa van een verbinding als 25,0 g opgelost in 750 ml een molariteit van 0,290 M oplevert?
Wat is de molaire massa van een verbinding als 25,0 g opgelost in 750 ml een molariteit van 0,290 M oplevert?  Akoestische focussering om microplastics in water te verzamelen
Akoestische focussering om microplastics in water te verzamelen
Hoofdlijnen
- De cel die door een virus is geïnfecteerd, wordt de?
- Een bacterieel stroomdiagram maken
- Kan een klein deeltje de plaag van het vergroenen van citrusvruchten tegengaan?
- Nieuwe dataset werpt licht op de relatie tussen verrode zon-geïnduceerde chlorofylfluorescentie en fotosynthese op bladerdakniveau
- Bloem of vlees? Genetica verklaart de voorkeur van muggen
- Hoe bacteriën zwemmen:onderzoekers ontdekken nieuwe mechanismen
- Ambitieus doel om RNA te sequencen zou de Amerikaanse economie kunnen stimuleren
- Wat doodt de Argentijnse walvissen?
- Onderzoekers ontdekken aanwijzingen over hoe de nek van giraffen is geëvolueerd
- Computationele studie laat zien hoe Ebola nucleocapside stabiliseert

- Formaatdehydrogenase reduceert koolstofdioxide tot mierenzuur
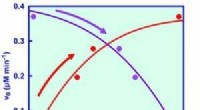
- Close-up van groeiende polymeerketen Toon sprongstappen
- Geautomatiseerde pijplijn verbetert de toegang tot geavanceerde microscopiegegevens

- Methode om microfluïdische elektrochemische technologieën toe te passen op redox-neutrale reacties met één elektronoverdracht
 Killer Nijlkrokodillen in Florida? Deskundigen zeggen dat het mogelijk is
Killer Nijlkrokodillen in Florida? Deskundigen zeggen dat het mogelijk is  We zijn helemaal blij, zegt betaalde Amazon-werknemers op Twitter
We zijn helemaal blij, zegt betaalde Amazon-werknemers op Twitter Wat chimpansees ons kunnen leren over economie
Wat chimpansees ons kunnen leren over economie  Bedreiging voor Florida neemt af, aangezien Isaias naar verwachting een tropische storm zal blijven
Bedreiging voor Florida neemt af, aangezien Isaias naar verwachting een tropische storm zal blijven Waarom meer grootouders hun kleinkinderen opvoeden
Waarom meer grootouders hun kleinkinderen opvoeden De eerste waarneming van een materiaal dat een supersolide fase van materie vertoont
De eerste waarneming van een materiaal dat een supersolide fase van materie vertoont  Hoe maak je Super sterke permanente magneten
Hoe maak je Super sterke permanente magneten  Wetenschappers ontwikkelen antimicrobiële, plantaardige voedselverpakking ter vervanging van plastic
Wetenschappers ontwikkelen antimicrobiële, plantaardige voedselverpakking ter vervanging van plastic
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

