
Wetenschap
Waarom worden elektronen aangetrokken door protonen?
$$ F =k \frac{|q_1||q_2|}{r^2} $$
Waar F de elektrostatische kracht is, is k de elektrostatische constante, zijn q_1 en q_2 de grootten van de ladingen, en is r de afstand tussen de ladingen.
In het geval van een elektron en een proton geldt:q_1 =-1,6 × 10^-19 C (de lading van een elektron) en q_2 =1,6 × 10^-19 C (de lading van een proton). De afstand daartussen ligt doorgaans in de orde van 1 x 10 ^ -10 m (de Bohr-straal). Als we deze waarden in de wet van Coulomb pluggen, krijgen we:
$$ F =(9 × 10^9 \frac{N m^2}{C^2}) \frac{(-1,6 × 10^{_19} C)(1,6 × 10^{-19} C)} {(1 × 10^{-10} m)^2} =-2,304 × 10^{−8} N $$
Dit negatieve teken geeft aan dat de kracht aantrekkelijk is. De omvang van deze kracht is erg klein, maar voldoende om het elektron in een baan rond de kern van een atoom te houden.
 Klimaatverandering verschuift timing van Europese overstromingen
Klimaatverandering verschuift timing van Europese overstromingen Stoppels brandende luchtvervuiling in India veroorzaakt economische verliezen van 30 miljard dollar, gezondheids risico's
Stoppels brandende luchtvervuiling in India veroorzaakt economische verliezen van 30 miljard dollar, gezondheids risico's Wat zijn de grassrooteffecten van de mondialisering?
Wat zijn de grassrooteffecten van de mondialisering?  Ontdekking werpt licht op het grote mysterie waarom het universum minder antimaterie heeft dan materie
Ontdekking werpt licht op het grote mysterie waarom het universum minder antimaterie heeft dan materie  Welke van deze delen, een ecosysteem, zijn biotisch, welke abiotische rotsen, wolken, vogels, lucht, gras, insecten, konijn, water, alligator, zon?
Welke van deze delen, een ecosysteem, zijn biotisch, welke abiotische rotsen, wolken, vogels, lucht, gras, insecten, konijn, water, alligator, zon?
Hoofdlijnen
- Wat hersenetende amoeben ons kunnen vertellen over de diversiteit van het leven op aarde en de evolutionaire geschiedenis
- DNA-modellen van paperclips maken
- Hoe kunnen uitstervingen de evolutie beïnvloeden van organismen die een gebeurtenis overleven?
- Maaien of niet maaien:Overlastgroei van waterplanten bij de wortel aanpakken
- Waarom is DNA-replicatie belangrijk voor de celcyclus?
- Hoe de ‘loopbandband’ zorgt voor een goede celdeling
- De kattenpest is terug na bijna 40 jaar onderduiken – dit is wat je moet weten
- Perzikperfectie:geavanceerde genennetwerken onthullen fruiteigenschappen
- Nobel werpt licht op paleogenetica, studie van oud DNA
- Ontdekken hoe het toevoegen van UV-behandeling aan waterchlorering de productie van giftige trihalomethaan daadwerkelijk kan verhogen

- Kankercellen kunnen over langere afstanden in het lichaam communiceren

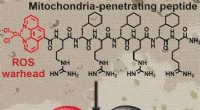
- Een metallopeptide richt zich op en verstoort de mitochondriale functie in stamcellen van borstkanker
- Draagbare chemiekit maakt het mogelijk om de zoetheid van bushfood ter plaatse te testen

- Ideale methode voor het snel testen van ziekten

 Video:Wat is de chemie achter ringworm?
Video:Wat is de chemie achter ringworm? Zullen de Olympische Spelen van 2024 in Parijs een platform zijn voor activistische protesten te midden van mondiale spanningen?
Zullen de Olympische Spelen van 2024 in Parijs een platform zijn voor activistische protesten te midden van mondiale spanningen?  Eerste symbiotische ster gedetecteerd door Gaia-satelliet
Eerste symbiotische ster gedetecteerd door Gaia-satelliet Onderzoekers gebruiken hete nano-beitel om kunstmatige botten in een petrischaal te maken
Onderzoekers gebruiken hete nano-beitel om kunstmatige botten in een petrischaal te maken Nieuw rapport toont dwingende redenen om sekswerk te decriminaliseren
Nieuw rapport toont dwingende redenen om sekswerk te decriminaliseren Wat maakt een relatie tot een functie?
Wat maakt een relatie tot een functie?  Onderzoek onthult aanzienlijke hoeveelheden bandendeeltjes die rivieren en oceanen vervuilen
Onderzoek onthult aanzienlijke hoeveelheden bandendeeltjes die rivieren en oceanen vervuilen Parker Solar Probe biedt een prachtig uitzicht op Venus
Parker Solar Probe biedt een prachtig uitzicht op Venus
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

