
Wetenschap
Hoe fotonen de chemie veranderen
* Elektronische excitatie: Het foton kan een elektron in het molecuul exciteren naar een hoger energieniveau. Dit kan ervoor zorgen dat het molecuul reactiever wordt of chemische reacties ondergaat die het normaal niet zou ondergaan.
* Trillingsexcitatie: Het foton kan ervoor zorgen dat het molecuul krachtiger gaat trillen. Dit kan leiden tot het verbreken van chemische bindingen of tot de vorming van nieuwe chemische bindingen.
* Dissociatie: Het foton kan ervoor zorgen dat het molecuul in kleinere fragmenten uiteenvalt. Dit kan gebeuren als het foton voldoende energie heeft om de bindingsenergie van het molecuul te overwinnen.
De effecten van fotonen op moleculen zijn afhankelijk van een aantal factoren, waaronder de golflengte van het licht, de intensiteit van het licht en de chemische structuur van het molecuul.
Fotochemie is een krachtig hulpmiddel dat kan worden gebruikt om nieuwe materialen te synthetiseren, chemische reacties te bestuderen en de interacties tussen licht en materie te begrijpen. Enkele van de toepassingen van fotochemie zijn onder meer:
* Zonne-energie: Fotovoltaïsche cellen gebruiken de energie van zonlicht om elektriciteit op te wekken.
* Fotokatalyse: Fotokatalysatoren worden gebruikt om chemische reacties te versnellen door licht als energiebron te gebruiken.
* Fotochromisme: Meekleurende materialen veranderen van kleur wanneer ze worden blootgesteld aan licht.
* Fluorescentie: Fluorescerende materialen zenden licht uit wanneer ze worden blootgesteld aan licht.
Fotochemie is een snel groeiend onderzoeksgebied en er worden voortdurend nieuwe toepassingen voor deze technologie ontwikkeld.
 Welke chemische stof wordt gebruikt in HydroChrome?
Welke chemische stof wordt gebruikt in HydroChrome?  Wat gebeurt er met het oxidatie nummer wanneer een atoom in een reactant elektronen verliest?
Wat gebeurt er met het oxidatie nummer wanneer een atoom in een reactant elektronen verliest?
Het oxidatiegetal van een element geeft de hypothetische lading van een atoom in een verbinding aan. Het is hypothetisch omdat in de context van een verbi
 Als 25,0 ml 1,48 m h2so4 kan worden geneutraliseerd met 27,29 koh, wat is dan de molariteit koh?
Als 25,0 ml 1,48 m h2so4 kan worden geneutraliseerd met 27,29 koh, wat is dan de molariteit koh?  Is isobutaan in mousse hetzelfde als butaan in aanstekers?
Is isobutaan in mousse hetzelfde als butaan in aanstekers?  Snel 4D-printen met polymeren met vormgeheugen
Snel 4D-printen met polymeren met vormgeheugen
 Voedsel delen als middel om afval te verminderen en stedelijke duurzaamheid te vergroten
Voedsel delen als middel om afval te verminderen en stedelijke duurzaamheid te vergroten Welke laag van de aardkorst bevat de hoogste concentratie van silicium?
Welke laag van de aardkorst bevat de hoogste concentratie van silicium?  Californië heeft de afgelopen seizoenen de meeste regen gehad. Zet de trend zich voort in 2022?
Californië heeft de afgelopen seizoenen de meeste regen gehad. Zet de trend zich voort in 2022? Zee-ijskappen waren bepalend voor de versnelling van de opwarming van de aarde tijdens de laatste deglaciatie
Zee-ijskappen waren bepalend voor de versnelling van de opwarming van de aarde tijdens de laatste deglaciatie Smog in Delhi bereikt noodniveaus tijdens bezoek van Britse prins Charles
Smog in Delhi bereikt noodniveaus tijdens bezoek van Britse prins Charles
Hoofdlijnen
- Nieuw onderzoek laat zien hoe microscopisch kleine algen in de loop van de tijd uitzonderlijk voedzaam zijn geworden, waardoor de evolutie vooruit is gegaan
- Wat is een onopvallende milt?
- Typen cellijnen
- Heeft gonorroe ons grootouders gegeven?
- Waarom eten sommige bijenkoninginnen de eieren van hun werkbij?
- Cellen afgeleid van verschillende stamcellen:hetzelfde of verschillend?
- Wat is een epidermis?
- Moleculaire biologie:zijn snel prolifererende cellen epigenetisch kneedbaar?
- Telepathie bij honden? Studie onderzoekt hoe honden denken en leren over menselijk gedrag
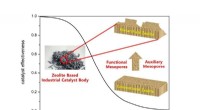
- Rationeel ontwerpen van hiërarchische zeolieten voor betere diffusie en katalysatorefficiëntie
- Onderzoeken naar enkelvoudige deeltjes wijzen de weg naar lichtschermen van de volgende generatie

- Elektronenversnellers onthullen de radicale geheimen van antioxidanten

- Onderzoekers 3D printen eerste hoogwaardige nanogestructureerde legering die zowel ultrasterk als ductiel is

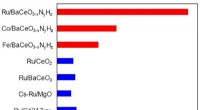
- Efficiënte bottom-up synthese van nieuw perovskietmateriaal voor de productie van ammoniak
 Kan intergenerationele samenwerking de klimaatverandering verslaan?
Kan intergenerationele samenwerking de klimaatverandering verslaan?  Heldere strepen op de maan zijn een product van ruimteverwering
Heldere strepen op de maan zijn een product van ruimteverwering Patronen van uitdunning van de grootste gletsjer van Antarctica zijn tegengesteld aan eerder waargenomen
Patronen van uitdunning van de grootste gletsjer van Antarctica zijn tegengesteld aan eerder waargenomen Advocaat:Songruiler staat terecht voor 'wat kinderen doen'
Advocaat:Songruiler staat terecht voor 'wat kinderen doen'  Hoe heet het proces waarbij delingscellen haploïde cellen vormen?
Hoe heet het proces waarbij delingscellen haploïde cellen vormen?  Factoren die van invloed zijn op de prestaties in de wiskunde
Factoren die van invloed zijn op de prestaties in de wiskunde Buckyballs geven elektron-positron-paren af in voorwaartse richtingen
Buckyballs geven elektron-positron-paren af in voorwaartse richtingen Dit is wat bedrijven en consumenten kunnen doen om moderne slavernij in toeleveringsketens aan te pakken
Dit is wat bedrijven en consumenten kunnen doen om moderne slavernij in toeleveringsketens aan te pakken
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

