
Wetenschap
De wetenschap achter het bruisen:hoe bubbels drank maken
Het bruisen en sprankelen van koolzuurhoudende dranken, algemeen bekend als 'fizz', is een heerlijke zintuiglijke ervaring die een element van genot toevoegt aan de consumptie ervan. Maar wat veroorzaakt dit bruisende gevoel precies, en hoe ontstaan er belletjes in dranken? Laten we de wetenschap achter het bruisen onderzoeken.
1. Kooldioxide (CO2) is het belangrijkste ingrediënt:
- De aanwezigheid van opgelost kooldioxidegas (CO2) is cruciaal voor het ontstaan van bruis in dranken.
- Carbonatatie treedt op wanneer CO2-gas onder hoge druk in vloeistoffen, zoals water, wordt geïnjecteerd.
2. Wet van Henry en gasoplosbaarheid:
- De wet van Henry stelt dat de hoeveelheid gas die in een vloeistof is opgelost recht evenredig is met de partiële druk van dat gas boven de vloeistof.
- Bij hogere drukken kan er meer CO2-gas in de vloeistof worden geperst, wat resulteert in een hogere concentratie opgelost gas.
3. Druk en evenwicht:
- Wanneer de druk wordt opgeheven, komt het opgeloste CO2-gas uit de oplossing en vormt het kleine belletjes.
- De bellen stijgen door het drijfvermogen naar de oppervlakte en creëren het bruiseffect.
4. Nucleatieplaatsen voor belvorming:
- Bellen vormen zich rond kleine deeltjes of onvolkomenheden in de vloeistof en fungeren als kiemplaatsen.
- Deze plekken kunnen microscopisch kleine deeltjes zijn, zoals stof, vezels of zelfs kleine onregelmatigheden in het oppervlak van de container.
5. Oppervlaktespanning en bellengroei:
- Oppervlaktespanning, de neiging van een vloeistof om het oppervlak ervan te verkleinen, biedt aanvankelijk weerstand tegen belvorming.
- Naarmate er meer CO2-gas zich ophoopt rond de kernvormingsplaatsen, overwint de druk in de bellen de oppervlaktespanning, wat leidt tot een snelle groei van de bellen.
6. Release van Bubbles en Fizz:
- Op het oppervlak van koolzuurhoudende dranken komen de meeste belletjes voor, omdat de druk lager is op het grensvlak tussen vloeistof en lucht.
- Terwijl bellen opstijgen en in de atmosfeer ontsnappen, barsten ze aan de oppervlakte, waardoor het CO2-gas vrijkomt en een bruisend schuim ontstaat.
7. Factoren die het bruisen beïnvloeden:
- Temperatuur:bij hogere temperaturen kunnen bellen sneller verdwijnen.
- Druk:Hogere drukken leiden tot meer opgelost CO2 en een intenser bruisen.
- Agitatie:Het schudden of roeren van een koolzuurhoudende drank versnelt het vrijkomen van belletjes.
Als we de wetenschap achter het bruisen begrijpen, kunnen we het samenspel van druk, gasoplosbaarheid, oppervlaktespanning en kernvorming waarderen bij het creëren van de heerlijke ervaring van mousserende dranken. Of het nu een verfrissende frisdrank, een dorstlessend biertje of een bruisende champagne is, de bruisende sensatie voegt een element van genot toe dat onze zintuiglijke ervaring versterkt.
 Sensoren ontwerpen om vreemde lichamen in voedsel te detecteren
Sensoren ontwerpen om vreemde lichamen in voedsel te detecteren Wetenschappers ontwikkelen een polymeerfilm geïnspireerd op spinnenzijde om biologische weefsels met elektronische apparaten te verbinden
Wetenschappers ontwikkelen een polymeerfilm geïnspireerd op spinnenzijde om biologische weefsels met elektronische apparaten te verbinden  Brandmembranen voor moleculair zeven
Brandmembranen voor moleculair zeven Hoe wordt Pure Cesium opgeslagen?
Hoe wordt Pure Cesium opgeslagen?  Hoe helpt Spectroscopy elementen te identificeren?
Hoe helpt Spectroscopy elementen te identificeren?
 NASA vindt zware regenval in nieuwe tropische cycloon Irondro
NASA vindt zware regenval in nieuwe tropische cycloon Irondro Waarnemingen vanuit de lucht van de Aziatische moesson zien dat ozonafbrekende stoffen de stratosfeer in zweven
Waarnemingen vanuit de lucht van de Aziatische moesson zien dat ozonafbrekende stoffen de stratosfeer in zweven  Onderzoek koppelt fracking aan hogere radonniveaus in huizen in Ohio
Onderzoek koppelt fracking aan hogere radonniveaus in huizen in Ohio Zware regenval in Bangladesh onderzocht met NASA's IMERG
Zware regenval in Bangladesh onderzocht met NASA's IMERG Een hertekende wereld:zorgen over het klimaat, niet over COVID, zegt James Gaia Lovelock
Een hertekende wereld:zorgen over het klimaat, niet over COVID, zegt James Gaia Lovelock
Hoofdlijnen
- Onderzoek bevestigt het:we worden echt dommer
- Hoe soorten versteend hout te identificeren
- Zijn er evolutionaire wortels voor menselijke obesitas?
- De functie van veel eiwitten blijft onduidelijk
- Het Australische Great Barrier Reef heeft moeite om te overleven
- Vragen en antwoorden over epigenetica:Wat het embryo ons kan leren over celherprogrammering
- Een onderzoeker uit de staat Iowa bestudeert hoe enzymen cellulose afbreken
- Wetenschappers presenteren een nieuwe methode om elk eiwit in elk soort cel direct en snel te vernietigen
- Wat onderscheidt mensen van chimpansees en andere apen? | Hoe dingen werken
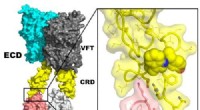
- Zoetheid voelen op moleculair niveau
- Nieuw antischimmelmiddel van mierenboerderijen

- Bacteriefabrieken kunnen hoogwaardige eiwitten maken voor ruimtemissies

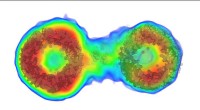
- Krachtige nieuwe beeldvormingsmethode onthult in detail hoe deeltjes in oplossing bewegen
- Kan een stromend vloeistofachtig materiaal zijn structurele orde handhaven zoals kristallen?

 Studie vindt een grote toename van de opname van koolstofdioxide in de oceaan langs het West-Antarctisch Schiereiland
Studie vindt een grote toename van de opname van koolstofdioxide in de oceaan langs het West-Antarctisch Schiereiland Zullen FAA's plannen voor 737 MAX buiten de VS vliegen?
Zullen FAA's plannen voor 737 MAX buiten de VS vliegen? Machine learning-techniek helpt draagbare apparaten beter te worden in het diagnosticeren van slaapstoornissen en kwaliteit
Machine learning-techniek helpt draagbare apparaten beter te worden in het diagnosticeren van slaapstoornissen en kwaliteit Plakband en simulaties helpen bij het beoordelen van het risico van microplastics
Plakband en simulaties helpen bij het beoordelen van het risico van microplastics Smaakt geweldig, minder storten ... bier in een papieren fles
Smaakt geweldig, minder storten ... bier in een papieren fles Meervoudig, gepersonaliseerd zacht exosuit breekt nieuwe wegen
Meervoudig, gepersonaliseerd zacht exosuit breekt nieuwe wegen ESA's zonsverduisteringsmaker, Proba-3
ESA's zonsverduisteringsmaker, Proba-3  BMW gaat elektrische Mini bouwen in China
BMW gaat elektrische Mini bouwen in China
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

