
Wetenschap
Een duidelijker beeld van hoe ijzer reageert in de omgeving
1. Oxidatie: IJzer is gevoelig voor oxidatie, wat optreedt wanneer het in contact komt met zuurstof. Dit proces resulteert in de vorming van ijzeroxiden, beter bekend als roest. Roest is een roodbruine verbinding die zich vormt op het oppervlak van ijzer wanneer het wordt blootgesteld aan lucht en vocht. De oxidatie van ijzer is een elektrochemisch proces waarbij elektronen worden overgedragen tussen ijzeratomen en zuurstofmoleculen.
2. Reductie: IJzer kan ook reductiereacties ondergaan, waarbij het elektronen verkrijgt en wordt gereduceerd tot een lagere oxidatietoestand. Dit proces vindt vaak plaats in aanwezigheid van reductiemiddelen, zoals waterstof of koolmonoxide. Vermindering van ijzer kan leiden tot de vorming van elementair ijzer of ijzerverbindingen met lagere oxidatietoestanden, zoals ijzer(II)- of ijzer(III)-oxiden.
3. Ontbinding: IJzer kan oplossen in water, vooral in zure omgevingen. Wanneer ijzer in contact komt met water, ondergaat het een reeks reacties die resulteren in de vorming van gehydrateerde ijzerionen, zoals Fe(II)- of Fe(III)-ionen. Het oplossen van ijzer wordt beïnvloed door factoren zoals pH, temperatuur en de aanwezigheid van opgeloste zuurstof of complexvormers.
4. Complexiteit: IJzer kan complexen vormen met verschillende liganden, waaronder organische moleculen en anorganische anionen. Complexering verandert de chemische eigenschappen van ijzer en beïnvloedt de reactiviteit en biologische beschikbaarheid ervan. IJzer kan bijvoorbeeld complexen vormen met liganden zoals citraat, oxalaat of humusachtige stoffen, wat de oplosbaarheid, het transport en de interacties met andere stoffen in het milieu kan beïnvloeden.
5. Neerslag: IJzer kan onder bepaalde omstandigheden uit de oplossing neerslaan, zoals veranderingen in de pH of de toevoeging van precipitatiemiddelen. Neerslag van ijzer komt vaak voor in de vorm van ijzeroxiden, hydroxiden of carbonaten. De vorming van ijzerneerslag kan belangrijk zijn bij het verwijderen van ijzer uit water- of afvalwaterzuiveringsprocessen en kan ook bijdragen aan de vorming van ijzerrijke mineralen in het milieu.
6. Biologische interacties: IJzer speelt een cruciale rol in verschillende biologische processen en is essentieel voor veel organismen, waaronder planten, dieren en micro-organismen. IJzer kan interageren met biologische systemen door opname en gebruik door organismen, betrokkenheid bij enzymatische reacties en deelname aan biogeochemische cycli. Biologische processen kunnen de cyclus, transformatie en beschikbaarheid van ijzer in het milieu beïnvloeden.
Over het algemeen wordt de reactiviteit van ijzer in het milieu beïnvloed door een combinatie van factoren, waaronder de beschikbaarheid van zuurstof, pH, temperatuur, de aanwezigheid van complexvormers, biologische activiteit en de specifieke omgevingsomstandigheden. Het begrijpen van deze reacties is belangrijk op verschillende gebieden, waaronder de geologie, milieuchemie, bodemkunde en ecologie.
 Onderzoekers tikken ongebruikelijke - en waardevolle - ongerepte lucht om de impact van vervuiling te onthullen
Onderzoekers tikken ongebruikelijke - en waardevolle - ongerepte lucht om de impact van vervuiling te onthullen Zeemeeuwgedrag bij aardbevingen en veranderingen in het weer
Zeemeeuwgedrag bij aardbevingen en veranderingen in het weer Hoe beïnvloedt invallende zonnestraling stedelijke canyons?
Hoe beïnvloedt invallende zonnestraling stedelijke canyons? Hoe bosbranden ook impact hebben op meren
Hoe bosbranden ook impact hebben op meren  Het risico op vroeggeboorte neemt toe bij het affakkelen van gas, als gevolg van diepgewortelde milieuonrechtvaardigheden op het Amerikaanse platteland
Het risico op vroeggeboorte neemt toe bij het affakkelen van gas, als gevolg van diepgewortelde milieuonrechtvaardigheden op het Amerikaanse platteland
Hoofdlijnen
- Hoe gisten erin slagen de genetische onbalans van extra chromosomen te compenseren
- Mogelijk is er een nieuwe biologieregel aan het licht gekomen, die het inzicht in evolutie en veroudering vergroot
- Bijen en vlinders gaan achteruit in westelijk en zuidelijk Noord-Amerika
- Wat hondeneigenaren moeten weten over leptospirose
- Hoe is een kleine bij in Frans-Polynesië terechtgekomen? Acht nieuwe soorten helpen het wetenschappelijke mysterie op te lossen
- Wetenschappers krijgen een nieuw inzicht in het herstelproces van nucleotide-excisie
- Wetenschappers ontdekken hoe het SARS-CoV-2-virus het replicatieprogramma in geïnfecteerde cellen initieert
- Kolonies tellen in de microbiologie
- Ondiepwaterwinning is geen duurzaam alternatief voor diepwaterwinning, beweren wetenschappers
- Water + lucht + elektriciteit =waterstofperoxide

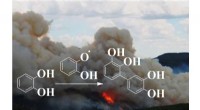
- Bruine koolstof van aromatische verontreinigende stoffen wordt uitgestoten tijdens verbranding en bosbranden
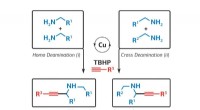
- Hoe inerte verbindingen ionen kunnen stelen

- Chemicus stelt nieuwe methode voor voor het synthetiseren van voorlopers voor Parkinson-medicijnen
- Tale of the tape:plakkerige stukjes zorgen voor betere batterijen

 Afbeelding:De waterrecyclingfaciliteit van het onderzoeksstation Concordia
Afbeelding:De waterrecyclingfaciliteit van het onderzoeksstation Concordia Zeebodem van Fram Strait is een gootsteen voor microplastic uit de Arctische en Noord-Atlantische Oceaan
Zeebodem van Fram Strait is een gootsteen voor microplastic uit de Arctische en Noord-Atlantische Oceaan Muondetector belangrijk voor beeldvorming en bewaking van opslagplaatsen voor kooldioxide
Muondetector belangrijk voor beeldvorming en bewaking van opslagplaatsen voor kooldioxide Hoe win je de Booker-prijs:is er een formule voor het beste in fictie?
Hoe win je de Booker-prijs:is er een formule voor het beste in fictie? Nieuwe aanwijzingen over de oorsprong van stellaire massa's
Nieuwe aanwijzingen over de oorsprong van stellaire massa's Bali geeft een momentopname van hoe 'overtoerisme' eruit ziet in de ontwikkelingslanden
Bali geeft een momentopname van hoe 'overtoerisme' eruit ziet in de ontwikkelingslanden  Tesla onthult Model Y SUV, uitbreiden naar populair segment
Tesla onthult Model Y SUV, uitbreiden naar populair segment Schoolkeuze leidt niet tot sociale mix tussen scholen
Schoolkeuze leidt niet tot sociale mix tussen scholen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

