
Wetenschap
Gemodificeerde cafeïnemoleculen helpen medisch onderzoek vooruit
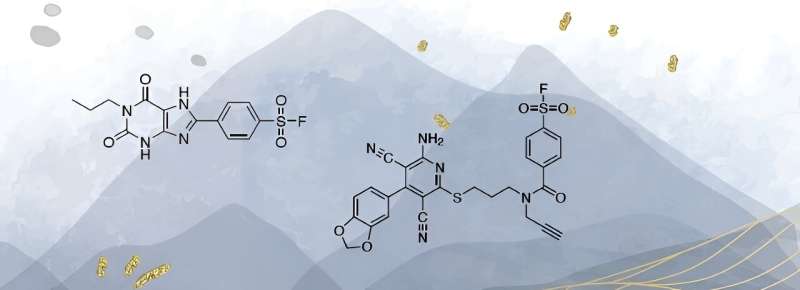
Voordat onderzoekers gerichte medicijnen kunnen ontwikkelen, moeten ze precies weten hoe een ziekte werkt. Biochemicus Bert Beerkens creëerde moleculen waarmee ze dat kunnen achterhalen. Hij gebruikte cafeïne als basis voor nieuwe moleculen die onderzoek naar bepaalde receptoreiwitten op cellen mogelijk maken.
Als scheikundestudent raakte Bert Beerkens gefascineerd door het onderzoeksveld waarmee je met de chemie allerlei processen in het lichaam kunt bestuderen. "Je ontwerpt en produceert dan moleculen die geen geneeskrachtige werking hebben, maar die andere onderzoekers helpen bij hun werk aan een bepaalde aandoening."
In zijn Ph.D. onderzoek ging Beerkens aan de slag om moleculen te maken die binden aan een eiwit dat normaal gesproken de stof adenosine bindt. Adenosine zit overal in ons lichaam. Het maakt deel uit van DNA en ook van ATP:adenosinetrifosfaat. Hierdoor wordt energie in alle levende cellen opgeslagen en beschikbaar gemaakt daar waar het nodig is.
Beerkens:“Adenosine is ook een signaalstof voor de communicatie tussen cellen. Als er veel adenosine rond een cel zit, kan dat betekenen dat een cel in de omgeving is gestorven.” Dan zwerft adenosine rond uit afgebroken ATP, en een naburige cel pikt het op met speciale receptoren op het celmembraan. "Afhankelijk van het type cel dat de adenosine opneemt, kan het resultaat zijn dat de immuunrespons wordt geremd. Sommige tumoren misbruiken dit mechanisme door actief adenosinereceptoren te produceren."
Stevig eraan binden en de receptor labelen
Om dit te onderzoeken zijn moleculen nodig die net als adenosine binden aan adenosinereceptoren. Beerkens ging de uitdaging aan. Cafeïne werd de basis van de stoffen die hij ontwikkelde. "Cafeïne bindt zich ook aan de receptor, alleen niet erg sterk."
Beerkens experimenteerde met extra atoomgroepen die op het cafeïnemolecuul waren gesubstitueerd. Hij slaagde erin moleculen te maken die niet alleen stevig aan de receptor binden, maar ook alleen aan dit type receptor en aan niets anders. "Er zijn vier verschillende adenosinereceptoren. Voor drie daarvan heb ik geschikte moleculen kunnen ontwerpen. Voor de vierde heeft mijn voorganger dat al gedaan."
Klikchemie bleek de oplossing, net als Lego
De moleculen moesten niet alleen stevig en selectief aan de receptor binden, maar er ook een moleculair label op plakken. “Dan kunnen onderzoekers zien of en waar welk type receptor aanwezig is.” Die waarneming moest ook in levend celmateriaal mogelijk zijn, dus zonder hoge doses radioactieve straling.
Dit was een lastig punt in het project van Beerkens. "Daar zijn we in geslaagd door gebruik te maken van klikchemie." Vorig jaar ging de Nobelprijs voor de scheikunde naar de ontwikkeling van dit soort chemie. "Het werkt als Lego. Wanneer het cafeïneachtige molecuul aan de adenosinereceptor wordt bevestigd, klikt een ander molecuul dat bijvoorbeeld licht uitzendt erop."
Beerkens behaalde zijn Ph.D. in november, nadat zijn resultaten eerder waren gepubliceerd. Is er een onmiddellijke stroom van onderzoekers die de moleculen gebruiken? “Zes maanden geleden kwam er een verzoek uit de VS. Een ziekenhuis wilde onderzoek doen naar een ziekte waarbij adenosine een rol lijkt te spelen. Daarnaast gebeurt het nog steeds vooral in en rond ons lab, samen met het LUMC. Het gaat om onderzoek in adenosinereceptoren op bepaalde immuuncellen, om te zien wat een goed doelwit zou zijn voor medicijnen om op in te werken."
Meer informatie: Op affiniteit gebaseerde profilering van de adenosinereceptoren. wetenschappelijkepublicaties.universi … /handle/1887/3656497
Aangeboden door Universiteit Leiden
 Het periodiek systeem onderwijzen aan vijfde beoordelaars
Het periodiek systeem onderwijzen aan vijfde beoordelaars Een plastic film die virussen kan doden met behulp van kamerverlichting
Een plastic film die virussen kan doden met behulp van kamerverlichting X-ray mapping verbetert het potentieel van lichtgewicht magnesium
X-ray mapping verbetert het potentieel van lichtgewicht magnesium Hoe het percentage ionisatie te berekenen gegeven de pH
Hoe het percentage ionisatie te berekenen gegeven de pH  Chemische grenstechniek gebruiken om staal te maken dat sterk en flexibel is zonder een hoog koolstofgehalte
Chemische grenstechniek gebruiken om staal te maken dat sterk en flexibel is zonder een hoog koolstofgehalte
 Simulaties demonstreren mogelijke mechanismen voor de vorming van zwarte gaten met gemiddelde massa in bolvormige sterrenhopen
Simulaties demonstreren mogelijke mechanismen voor de vorming van zwarte gaten met gemiddelde massa in bolvormige sterrenhopen  Waarom hebben planten en dieren stikstof nodig?
Waarom hebben planten en dieren stikstof nodig?  Magneten worden gebruikt om algenmoleculen te extraheren voor de schoonheid, biokunststofindustrieën
Magneten worden gebruikt om algenmoleculen te extraheren voor de schoonheid, biokunststofindustrieën Sheriff:Bosbranden wijzen op het nut van oude technologie
Sheriff:Bosbranden wijzen op het nut van oude technologie Kansen in het voordeel van Greta Thunberg voor de Vredesprijs, maar experts sceptisch
Kansen in het voordeel van Greta Thunberg voor de Vredesprijs, maar experts sceptisch
Hoofdlijnen
- Onderzoekers helpen migrerende zalm de hotspot van sterfte te overleven
- Een schakelaar voor de interne klok:onderzoek naar kwantumbiologie voor nieuwe medische therapieën
- Tornado's Effecten op mensen
- Onderwaterkwekerijen helpen de mediterrane visbestanden nieuw leven in te blazen
- Hoe goed kennen mensen zichzelf eigenlijk?
- Virtuele Labrador kan onderzoekers helpen bij het aanpakken van hondenbeten
- Artefacten suggereren aankomst van mensen in Australië 18,
- Hoe de dalingssnelheid te berekenen
- Wat gebruikt Gamma Roggen?
- Legos of life:een diepe duik in de 3D-structuren van eiwitten onthult belangrijke bouwstenen
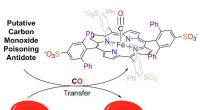
- Een remedie voor koolmonoxidevergiftiging ontgrendelen
- Nieuwe aanpak zal helpen bij het identificeren van medicijnen die eiwitten aan elkaar kunnen lijmen

- Onderzoekers stemmen de kleur en thermische eigenschappen van materialen afzonderlijk af

- De beste zeoliet bouwen

 Een kansbeperkend bewegingsplanningssysteem voor hoogdimensionale robots
Een kansbeperkend bewegingsplanningssysteem voor hoogdimensionale robots Hoe beïnvloedt de temperatuur de luchtdruk?
Hoe beïnvloedt de temperatuur de luchtdruk?  Onderzoek toont aan dat verzuring van de oceaan grote impact heeft op het leven in zee
Onderzoek toont aan dat verzuring van de oceaan grote impact heeft op het leven in zee Ideeën voor lesgeven aan kleuters
Ideeën voor lesgeven aan kleuters De natuur is de sleutel tot het koesteren van groene waterzuiveringsinstallaties
De natuur is de sleutel tot het koesteren van groene waterzuiveringsinstallaties Hoe procentuele afname berekenen
Hoe procentuele afname berekenen  Wat betekent een negatieve T-waarde?
Wat betekent een negatieve T-waarde?  CNT's gebruiken als infraroodsensoren
CNT's gebruiken als infraroodsensoren
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

