
Wetenschap
Orale peptiden:een nieuw tijdperk in de ontwikkeling van geneesmiddelen
Decennia lang is een aanzienlijk aantal eiwitten, die essentieel zijn voor de behandeling van verschillende ziekten, ongrijpbaar gebleven voor orale medicamenteuze behandeling. Traditionele kleine moleculen hebben vaak moeite om zich te binden aan eiwitten met vlakke oppervlakken of vereisen specificiteit voor bepaalde eiwithomologen. Grotere biologische geneesmiddelen die zich op deze eiwitten kunnen richten, vereisen doorgaans injectie, waardoor het gemak en de toegankelijkheid voor de patiënt worden beperkt.
In een nieuwe studie gepubliceerd in Nature Chemical Biology wetenschappers van het laboratorium van professor Christian Heinis bij EPFL hebben een belangrijke mijlpaal bereikt in de ontwikkeling van geneesmiddelen. Hun onderzoek opent de deur naar een nieuwe klasse oraal verkrijgbare geneesmiddelen, waarmee een al lang bestaand probleem in de farmaceutische industrie wordt aangepakt.
"Er zijn veel ziekten waarvoor de doelwitten zijn geïdentificeerd, maar medicijnen die deze doelen binden en bereiken, konden niet worden ontwikkeld", zegt Heinis. "De meeste daarvan zijn soorten kanker, en veel doelwitten bij deze kankers zijn eiwit-eiwit-interacties die belangrijk zijn voor de tumorgroei, maar niet kunnen worden geremd."
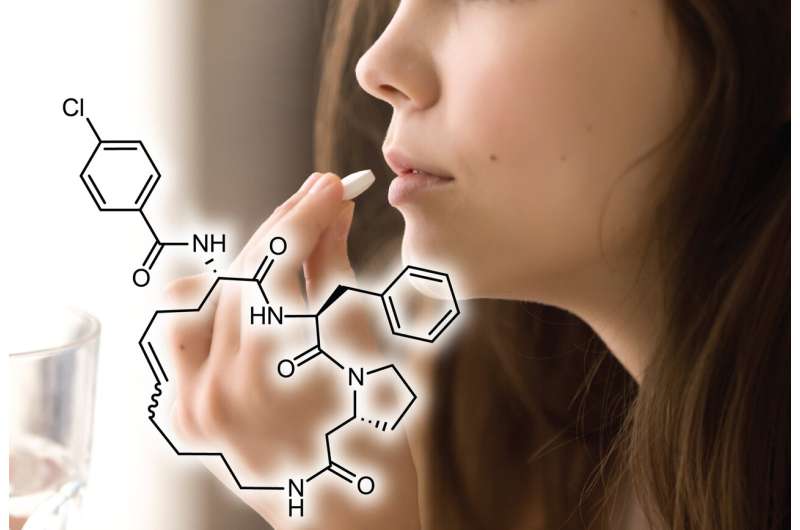
De studie concentreerde zich op cyclische peptiden, veelzijdige moleculen die bekend staan om hun hoge affiniteit en specificiteit bij het binden van uitdagende ziektedoelen. Tegelijkertijd is de ontwikkeling van cyclische peptiden als orale geneesmiddelen moeilijk gebleken, omdat ze snel worden verteerd of slecht worden geabsorbeerd door het maag-darmkanaal.
"Cyclische peptiden zijn van groot belang voor de ontwikkeling van geneesmiddelen, omdat deze moleculen zich kunnen binden aan moeilijke doelen waarvoor het een uitdaging was om medicijnen te genereren met behulp van gevestigde methoden", zegt Heinis. "Maar de cyclische peptiden kunnen doorgaans niet oraal worden toegediend – als pil – wat de toepassing ervan enorm beperkt."
Doorbraak op het gebied van fietsen
Het onderzoeksteam richtte zich op het enzym trombine, dat een kritisch ziektedoelwit is vanwege zijn centrale rol in de bloedstolling; het reguleren van trombine is de sleutel tot het voorkomen en behandelen van trombotische aandoeningen zoals beroertes en hartaanvallen.
Om cyclische peptiden te genereren die zich kunnen richten op trombine en voldoende stabiel zijn, ontwikkelden de wetenschappers een tweestaps combinatorische synthesestrategie om een enorme bibliotheek van cyclische peptiden met thioetherbindingen te synthetiseren, die hun metabolische stabiliteit verbeteren wanneer ze oraal worden ingenomen.
“We zijn er nu in geslaagd cyclische peptiden te genereren die binden aan een ziektedoelwit van onze keuze en die ook oraal kunnen worden toegediend”, zegt Heinis. "Daartoe hebben we een nieuwe methode ontwikkeld waarbij duizenden kleine cyclische peptiden met willekeurige sequenties op nanoschaal chemisch worden gesynthetiseerd en onderzocht in een high-throughput proces."
Twee stappen, één pot
Het nieuwe methodeproces omvat twee stappen en vindt plaats in dezelfde reactieve container, een kenmerk dat scheikundigen 'één pot' noemen.
De eerste stap is het synthetiseren van lineaire peptiden, die vervolgens een chemisch proces ondergaan waarbij een ringachtige structuur wordt gevormd – in technische termen ‘gecycliseerd’. Dit wordt gedaan met behulp van 'bis-elektrofiele linkers' (chemische verbindingen die worden gebruikt om twee moleculaire groepen met elkaar te verbinden) om stabiele thioetherbindingen te vormen.
In de tweede fase ondergaan de gecycliseerde peptiden acylering, een proces waarbij carbonzuren eraan worden gehecht, waardoor hun moleculaire structuur verder wordt gediversifieerd.
De techniek elimineert de noodzaak van tussentijdse zuiveringsstappen, waardoor screening met hoge doorvoer rechtstreeks in de syntheseplaten mogelijk wordt, waarbij de synthese en screening van duizenden peptiden wordt gecombineerd om kandidaten te identificeren met een hoge affiniteit voor specifieke ziektedoelen – in dit geval trombine. P>
Met behulp van de methode heeft de Ph.D. De student die het project leidde, Manuel Merz, was in staat een uitgebreide bibliotheek van 8.448 cyclische peptiden te genereren met een gemiddelde molecuulmassa van ongeveer 650 Dalton (Da), slechts iets boven de maximale limiet van 500 Da die wordt aanbevolen voor oraal verkrijgbare kleine moleculen.
De cyclische peptiden vertoonden ook een hoge affiniteit voor trombine.
Bij testen op ratten vertoonden de peptiden een orale biologische beschikbaarheid tot 18%, wat betekent dat wanneer het cyclische peptidegeneesmiddel oraal wordt ingenomen, 18% ervan met succes in de bloedbaan terechtkomt en een therapeutisch effect heeft. Gezien het feit dat oraal toegediende cyclische peptiden over het algemeen een biologische beschikbaarheid van minder dan 2% vertonen, is het verhogen van dat aantal tot 18% een aanzienlijke vooruitgang voor geneesmiddelen in de categorie biologische geneesmiddelen, waartoe ook peptiden behoren.
Doelen stellen
Door de orale beschikbaarheid van cyclische peptiden mogelijk te maken, heeft het team mogelijkheden geopend voor de behandeling van een reeks ziekten die moeilijk te bestrijden zijn met conventionele orale medicijnen. De veelzijdigheid van de methode betekent dat deze kan worden aangepast om zich te richten op een breed scala aan eiwitten, wat mogelijk kan leiden tot doorbraken op gebieden waar momenteel niet aan de medische behoeften wordt voldaan.
"Om de methode toe te passen op meer uitdagende ziektedoelen, zoals eiwit-eiwitinteracties, zullen waarschijnlijk grotere bibliotheken moeten worden gesynthetiseerd en bestudeerd", zegt Manuel Merz. "Door verdere stappen van de methoden te automatiseren lijken bibliotheken met meer dan een miljoen moleculen binnen handbereik."
In de volgende stap van dit project zullen de onderzoekers zich richten op verschillende intracellulaire eiwit-eiwit-interactiedoelen waarvoor het moeilijk was om remmers te ontwikkelen op basis van klassieke kleine moleculen. Zij zijn ervan overtuigd dat voor ten minste enkele daarvan oraal toepasbare cyclische peptiden ontwikkeld kunnen worden.
Meer informatie: Alexander L. Nielsen, De novo ontwikkeling van kleine cyclische peptiden die oraal biologisch beschikbaar zijn, Natuurchemische biologie (2023). DOI:10.1038/s41589-023-01496-y
Journaalinformatie: Natuurchemische biologie
Aangeboden door Ecole Polytechnique Federale de Lausanne
 Ondergrondse glasvezelsensoren registreren geluiden van COVID-lockdown, heropening
Ondergrondse glasvezelsensoren registreren geluiden van COVID-lockdown, heropening Parijs roept klimaatnoodtoestand uit
Parijs roept klimaatnoodtoestand uit Terwijl we ons fixeren op het coronavirus, De aarde raast op een catastrofe af die erger is dan het uitsterven van de dinosauriërs
Terwijl we ons fixeren op het coronavirus, De aarde raast op een catastrofe af die erger is dan het uitsterven van de dinosauriërs Wat doen schrobbers in rookstapels?
Wat doen schrobbers in rookstapels?  Geglobaliseerde economie die water maakt, energie- en landonzekerheid erger:studie
Geglobaliseerde economie die water maakt, energie- en landonzekerheid erger:studie
Hoofdlijnen
- Extreme zoutstress veroorzaakt bladbeweging
- De 3 soorten bacteriën
- Wil je tijgers redden? Je kunt maar beter je cijfers op een rij hebben
- 10 slechtste aanpassingen in het dierenrijk
- Hoe de bacteriegroei in petrischalen te meten
- Het verschil tussen gensequentie en DNA-vingerafdrukken
- Diversiteit en immigratie verhogen de productiviteit in microbiële gemeenschappen
- Heeft die astroloog u goed gelezen? Dat is het Barnum-effect
- Mummies buikjes om de evolutie van de spijsvertering te onthullen
- Nieuw proces versnelt medicamenteuze behandelingen voor virale infecties en kanker

- Druppels beklimmen kan leiden tot efficiëntere waterwinning

- Groeiende HCA-kristallen

- Wetenschappers creëren op een eenvoudige manier onmogelijke materialen
- Oplosmiddelen van de volgende generatie vangen koolstof op met de helft van de energie

 Toevallige ontdekking van sterke en onbreekbare moleculaire schakelaar
Toevallige ontdekking van sterke en onbreekbare moleculaire schakelaar Wat is de grijze goo-nachtmerrie?
Wat is de grijze goo-nachtmerrie?  Hoe win je een Nobelprijs?
Hoe win je een Nobelprijs?  Vorm van coronavirus beïnvloedt de overdracht ervan, vindt onderzoek
Vorm van coronavirus beïnvloedt de overdracht ervan, vindt onderzoek NASA lanceert weersatelliet van de volgende generatie
NASA lanceert weersatelliet van de volgende generatie Modelleringsstrategie stelt wetenschappers in staat om manieren te onderzoeken om opwarming te beperken, bijwerkingen verminderen
Modelleringsstrategie stelt wetenschappers in staat om manieren te onderzoeken om opwarming te beperken, bijwerkingen verminderen Organisch tin in polymeren verhoogt hun lichtabsorptie
Organisch tin in polymeren verhoogt hun lichtabsorptie Problemen met een TI 84 Plus
Problemen met een TI 84 Plus
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

