
Wetenschap
Hoe moleculaire handigheid ontstond in de vroege biologie
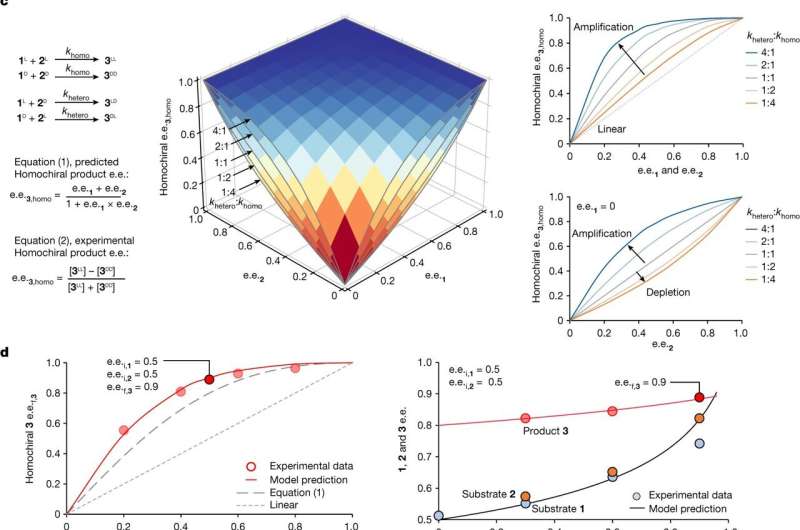
Moleculen hebben vaak een structurele asymmetrie die chiraliteit wordt genoemd, wat betekent dat ze kunnen verschijnen in alternatieve, spiegelbeeldversies, vergelijkbaar met de linker- en rechterversie van menselijke handen. Een van de grote mysteries over de oorsprong van het leven op aarde is dat vrijwel alle fundamentele moleculen van de biologie, zoals de bouwstenen van eiwitten en DNA, in slechts één chirale vorm voorkomen.
Scheikundigen van Scripps Research hebben in twee spraakmakende onderzoeken nu een elegante oplossing voor dit mysterie voorgesteld, die laat zien hoe deze eigenhandigheid of 'homochiraliteit' in de biologie een gevestigde waarde had kunnen worden.
De onderzoeken zijn gepubliceerd in de Proceedings of the National Academy of Sciences en in De natuur . Samen suggereren ze dat de opkomst van homochiraliteit grotendeels te danken is aan een scheikundig fenomeen dat kinetische resolutie wordt genoemd, waarbij de ene chirale vorm overvloediger wordt dan de andere als gevolg van snellere productie en/of langzamere uitputting.
"Er zijn veel voorstellen gedaan over hoe homochiraliteit in specifieke moleculen ontstond – specifieke aminozuren bijvoorbeeld – maar we hadden echt een meer algemene theorie nodig", zegt Donna Blackmond, Ph.D., professor en John C. Martin voorzitter in de Afdeling Scheikunde bij Scripps Research, die beide onderzoeken leidde.
Afgestudeerde student Jinhan Yu en postdoctoraal onderzoeksmedewerker Min Deng, Ph.D., waren de eerste auteurs van de twee onderzoeken.
Het raadsel van homochiraliteit
De chemie over de oorsprong van het leven is het grootste deel van de afgelopen eeuw een druk vakgebied geweest. De beoefenaars ervan hebben tientallen belangrijke reacties ontdekt die plausibel plaatsvonden op de vroege, ‘prebiotische’ aarde en die de eerste DNA’s, RNA’s, suikers, aminozuren en andere moleculen produceerden die het leven in stand hielden. In dit oeuvre ontbreekt echter een plausibele prebiotische theorie voor het ontstaan van homochiraliteit.
"Er is in het veld een tendens geweest om het chiraliteitsprobleem te negeren bij het zoeken naar plausibele reacties die de eerste biologische moleculen hadden kunnen maken", zegt Blackmond. "Het is frustrerend, want zonder reacties die homochiraliteit bevorderen, zouden we geen leven hebben."
Gewone chemische reacties die chirale moleculen produceren, hebben de neiging gelijke ("racemische") mengsels van links- en rechtshandige vormen op te leveren. Buiten de biologie doet deze vermenging er doorgaans niet toe, omdat beide vormen meestal vergelijkbare of identieke eigenschappen hebben.
Binnen de biologie is het echter, als gevolg van de uitgebreide homochiraliteit, vaak zo dat alleen de links- of rechtshandige vorm van een chiraal molecuul nuttige eigenschappen heeft; de andere kan inert of zelfs giftig zijn. Cellen sturen dus vaak reacties om specifieke chirale vormen te verkrijgen met behulp van hoogontwikkelde enzymen.
De prebiotische aarde zou dergelijke enzymen echter niet hebben gehad – dus hoe is homochiraliteit ooit ontstaan?
Een paradoxaal resultaat
In hun onderzoek in Proceedings of the National Academy of Sciences Blackmond en haar team hebben dit probleem voor aminozuren aangepakt. Deze kleine organische moleculen worden door alle levende wezens op aarde gebruikt als bouwstenen voor eiwitten, maar bestaan in de biologie alleen in de linkshandige chirale vorm.
De onderzoekers probeerden specifiek homochiraliteit te reproduceren in een centraal proces in de aminozuurproductie, transaminatie genaamd, door gebruik te maken van een relatief eenvoudige, plausibele prebiotische chemie die complexe enzymen uitsluit.
In vroege tests werkte de experimentele reactie van het team en leverde aminozuren op die verrijkt waren voor de ene chirale vorm ten opzichte van de andere. Het probleem was dat de favoriete vorm de rechtshandige vorm was, de vorm die de biologie niet gebruikt.
"We zaten een tijdje vast, maar toen ging het lampje branden. We beseften dat we een deel van de reactie in omgekeerde volgorde konden uitvoeren", zegt Blackmond.
Toen ze dat deden, maakte de reactie niet langer bij voorkeur rechtshandige aminozuren. In een treffend voorbeeld van kinetische resolutie consumeerde en uitgeput het in plaats daarvan bij voorkeur de rechtshandige versies, waardoor er meer van de gewenste linkshandige aminozuren overbleven. Het diende dus als een plausibele route naar homochiraliteit voor aminozuren die in levende cellen worden gebruikt.
Alles samenbinden
Voor de Natuur In hun studie onderzochten de scheikundigen een eenvoudige reactie waarmee aminozuren in de vroegste levensvormen mogelijk aan elkaar waren gekoppeld tot de eerste korte eiwitten (ook bekend als peptiden). De reactie was eerder gepubliceerd door een andere onderzoeker, maar was nooit onderzocht op het vermogen ervan om homochirale peptiden te produceren uit racemische of bijna-racemische mengsels van aminozuren.
Opnieuw stuitten de scheikundigen op wat een onoverkomelijk obstakel leek:ze ontdekten dat bij het vormen van peptideketens van aminozuren de reactie sneller werkte voor koppelingen van linkshandige met rechtshandige aminozuren – het tegenovergestelde van de gewenste homochirale peptiden. .
Toch zette het team door. Uiteindelijk ontdekten ze dat wanneer één type aminozuur in de uitgangspool van aminozuren zelfs maar een matige dominantie van de linkshandige vorm had – zoals hun andere onderzoek plausibel maakte – de snellere reactiesnelheid voor linkshandige naar rechtshandige vormen koppelingen putten bij voorkeur rechtshandige aminozuren uit, waardoor er een steeds grotere concentratie linkshandige aminozuren overblijft.
Bovendien hadden de links-rechts-links-rechts-peptiden een sterkere neiging om samen te klonteren en als vaste stoffen uit de oplossing te vallen. Deze kinetische resolutie-gerelateerde verschijnselen leverden dus uiteindelijk een verrassend zuivere oplossing op van vrijwel volledig linkshandige peptiden.
Voor Blackmond bieden de ogenschijnlijk paradoxale mechanismen die in deze onderzoeken aan het licht zijn gekomen, de eerste overtuigende en brede verklaring voor de opkomst van homochiraliteit – een verklaring die waarschijnlijk niet alleen werkt voor aminozuren, zegt ze, maar ook voor andere fundamentele moleculen van de biologie, zoals DNA en RNA.
Meer informatie: Jinhan Yu et al., Prebiotische toegang tot enantio-verrijkte aminozuren via peptide-gemedieerde transaminatiereacties, Proceedings of the National Academy of Sciences (2024). DOI:10.1073/pnas.2315447121
Donna Blackmond, Symmetriebreuk en chirale amplificatie bij prebiotische ligatiereacties, Natuur (2024). DOI:10.1038/s41586-024-07059-y. www.nature.com/articles/s41586-024-07059-y
Journaalinformatie: Natuur , Proceedings van de Nationale Academie van Wetenschappen
Aangeboden door het Scripps Research Institute
 Efficiënte bottom-up synthese van nieuw perovskietmateriaal voor de productie van ammoniak
Efficiënte bottom-up synthese van nieuw perovskietmateriaal voor de productie van ammoniak Het testen van de mogelijkheid om nikkelhoudende katalysatoren te gebruiken om multi-koolstofproducten te produceren
Het testen van de mogelijkheid om nikkelhoudende katalysatoren te gebruiken om multi-koolstofproducten te produceren Toevallige ontdekking van sterke en onbreekbare moleculaire schakelaar
Toevallige ontdekking van sterke en onbreekbare moleculaire schakelaar Voor schonere lucht, water, en aarde
Voor schonere lucht, water, en aarde Onderzoekers stimuleren bloedvatvorming met suiker
Onderzoekers stimuleren bloedvatvorming met suiker
Hoofdlijnen
- Krillgedrag brengt koolstof naar de diepten van de oceaan
- Hoe kleurt licht perzikschillen rood?
- Het bevorderen van de gewasveredeling door middel van gerichte genoommodificatie
- De gevaarlijkste gebieden voor aanvaringen met schepen met walvishaaien onthuld
- Sterven mensen in politiehechtenis aan opgewonden delirium?
- Moeder-kind linkerzijde face-to-face voorkeur bleek zich uit te strekken tot walrussen en Indiase vliegende vossen
- Supergenetica:genen die beschermen tegen COVID-19 en meer
- Human Heart Science Projects
- Een geïntegreerde beoordeling van vaatplantensoorten in Amerika
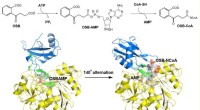
- Wetenschappers onthullen verschillende substraatbindingsmodus in o-succinylbenzoyl-CoA-synthetase
- Wetenschappers vinden nieuwe manieren om chemicaliën voor bioraffinage te gebruiken

- Herstellen van actief pompend hartweefsel met op mosselen geïnspireerde weefsellijm

- Nieuwe synthetische eiwitten wedijveren met hun natuurlijke tegenhangers in protonentransport

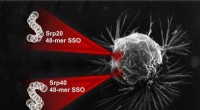
- Biochemici melden een manier om de onsterfelijkheid van kankercellen met oligonucleotiden te stoppen
 Wormen in de ruimte - het moleculaire spierexperiment
Wormen in de ruimte - het moleculaire spierexperiment Documentdump van Boeing toont verontrustend beeld op 737 MAX:officieel
Documentdump van Boeing toont verontrustend beeld op 737 MAX:officieel De ultieme groene technologie:computers maken die 10, 000 keer minder energie
De ultieme groene technologie:computers maken die 10, 000 keer minder energie Wetenschappers gebruiken zelfassemblage om deeltjes ter grootte van een molecuul te maken met ladingen
Wetenschappers gebruiken zelfassemblage om deeltjes ter grootte van een molecuul te maken met ladingen Ohio concentreert zich op het verminderen van schadelijke Lake Erie-algen
Ohio concentreert zich op het verminderen van schadelijke Lake Erie-algen Amazon/Deliveroo-deal staat voor diepgaand onderzoek in het VK
Amazon/Deliveroo-deal staat voor diepgaand onderzoek in het VK Kunnen drones straaljagers vervangen?
Kunnen drones straaljagers vervangen?  Verschillende manieren om elektriciteit te maken
Verschillende manieren om elektriciteit te maken
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

