
Wetenschap
Onverwacht gedrag gezien bij efficiënte katalysatoren voor schone energie
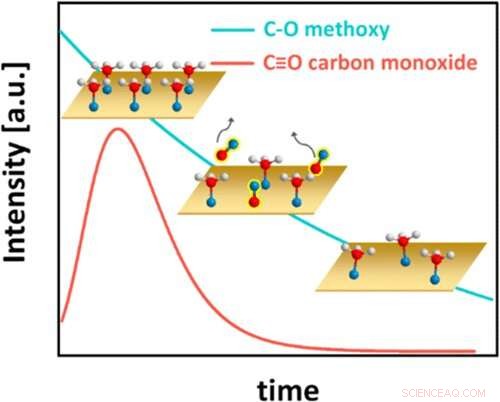
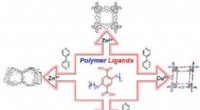
Grafisch abstract. Krediet:ACS-katalyse (2022). DOI:10.1021/acscatal.1c05933
Onderzoekers van het Weizmann Institute of Science en het Brookhaven National Laboratory van het Amerikaanse Department of Energy (DOE) hebben de dynamiek op moleculair niveau onderzocht wanneer methanol wordt omgezet in waterstof met behulp van een koperkatalysator, waarbij het hele systeem onder omgevingsdruk en temperatuur staat. . Deze studie, die verrassende informatie opleverde over het gedrag van de methanol op verschillende koperoppervlakken, zal onderzoekers helpen de best presterende koperkatalysator voor dit proces te vinden en, meer in het algemeen, hun begrip van koperkatalysatoren als groep vergroten.
Methanol (een verbinding van waterstof, koolstof en zuurstof) is een veelzijdig materiaal in de energie-industrie. Het kan gebruikt worden als brandstof zelf of, zoals in dit onderzoek, om een andere brandstof te produceren:waterstof. Methanol is een toonaangevende kandidaat voor waterstofopslagtechnologieën, met name in brandstofceltoepassingen in auto's. Een vloeistof op kamertemperatuur, gemakkelijk om mee te werken en compatibel met de bestaande benzine-infrastructuur. Het bevat ook een relatief grote hoeveelheid waterstof per volume. Maar om waterstof efficiënt te produceren, heeft methanol de hulp van een katalysator en een relatief hoge temperatuur nodig.
In deze studie, beschreven in de online editie van ACS Catalysis, van 14 juni 2022, , bestudeerden de Weizmann- en Brookhaven-onderzoekers een methanol / koper-systeem - methanoldamp gebonden of "geadsorbeerd" op een koperoppervlak - waarvoor geen hoge temperatuur nodig was. Ze concentreerden zich op 'methanolontleding', de eenvoudigste van de vier reacties die waterstof uit methanol kunnen produceren. Van de mogelijke katalysatoren voor de reactie worden die op basis van koper (Cu) als de meest veelbelovende beschouwd. Dit is te wijten aan verschillende factoren, waaronder de gunstige elektronische structuur voor katalytische activiteit en relatief lage kosten en milieuveiligheid in vergelijking met andere metalen. Om de rol van Cu beter te begrijpen, is het essentieel dat wetenschappers een grondig moleculair begrip krijgen van de interactie tussen methanoldamp en Cu-oppervlakken.
Onderzoekers van Weizmann en het Center for Functional Nanomaterials (CFN), een DOE Office of Science User Facility in Brookhaven, keken naar drie Cu-oppervlakken om te leren hoe de methanol eraan hechtte en hoe het zich gedroeg. Deze drie oppervlaktegeometrieën worden vaak onderzocht als katalysatoren vanwege de manier waarop de Cu-atomen zijn gerangschikt, waardoor ze meer beschikbaar zijn voor elektronische interactie met andere verbindingen. De groep ontdekte dat de methanol op alle drie de oppervlakken op onverwachte manieren werkt.
"De trend die we op alle drie de oppervlakken zagen, was dat eerst veel methanol werd geadsorbeerd en vervolgens uiteenviel in verschillende componenten die desorbeerden. Na enige tijd bereikte de methanoldekking een evenwichtspunt", zegt Ashley Head, een onderzoeker bij de Interface. Sciences/Catalysis-groep bij de CFN en een van de auteurs van het artikel. "We hadden dit gedrag niet eerder gezien en hadden ook niet verwacht."
Om de dynamiek hiervan te bestuderen, gebruikte de groep zowel infrarood (IR) als röntgenspectroscopietechnieken, de laatste uitgevoerd bij het CFN.
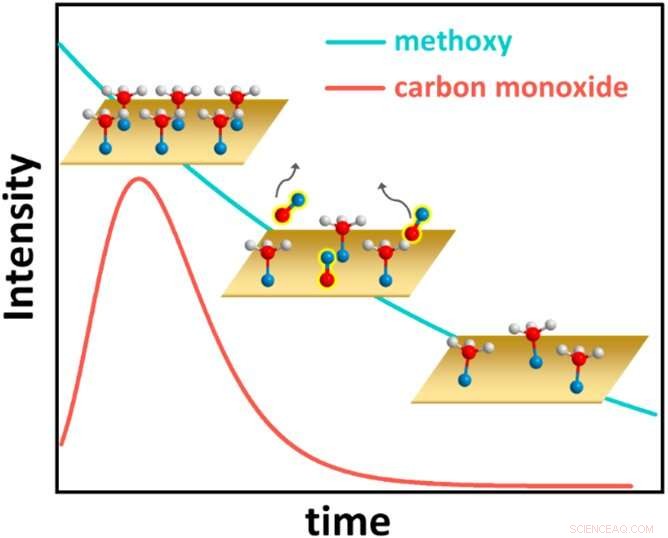
Deze figuur toont het verrassende kinetische gedrag van het methanol-op-koper-systeem, waarbij waterstofatomen worden weergegeven als witte bollen, zuurstofatomen als blauwe bollen en koolstofatomen als rode bollen. Aanvankelijk bedekt methanol het koper (Cu) oppervlak grondig (afbeelding linksboven). Elk methanolmolecuul verliest dan een waterstofatoom en vormt een chemische binding met het Cu, waardoor het een koolstof-zuurstofsoort wordt die bekend staat als methoxy. De oppervlaktemethoxy reageert op zijn beurt om koolmonoxide (CO) te vormen, dat van het oppervlak desorbeert (middenafbeelding, met CO-dekking in de tijd weergegeven door de rode lijn). De methoxydekking neemt dan gestaag af (afbeelding rechtsonder en blauwe lijn). Uiteindelijk wordt een evenwichtsmethoxydekking bereikt (niet getoond). Krediet:Brookhaven National Laboratory
Het IR-werk, uitgevoerd bij Weizmann, leverde informatie op over welke chemische soorten methanol zich op het Cu-oppervlak vormden door te meten hoe de moleculen trillen. De specifieke trillingen kunnen worden gekoppeld aan specifieke verbindingen.
De IR-gegevens gaven aan dat de methanol zwaar op het koper adsorbeerde en een directe binding met het Cu vormde, waardoor een chemische component werd gevormd die bekend staat als methoxy. De methoxydekking nam toen geleidelijk af. Dit gedrag werd op alle drie de oppervlakken waargenomen, met kleine afwijkingen.
"Deze dynamiek komt niet overeen met wat gevestigde modellen van dit systeem ons vertellen dat we zouden moeten zien", zegt Baran Eren, een onderzoeker bij de afdeling Chemische en Biologische Fysica van Weizmann en de corresponderende auteur van het artikel. "In plaats daarvan volgt de evolutie van de methoxydekking in de tijd een buitengewoon adsorptiekinetiekmodel."
Hij vervolgde:"We stellen voor dat een kortlevende vorm van methanol gebonden aan waterstof de bron is van de aanvankelijke dichte methoxylaag."
De informatie uit de IR-gegevens werd bevestigd bij CFN, waar de groep röntgenfoto-elektronspectroscopie (APXPS) gebruikte. Bij deze techniek bekrachtigen röntgenstralen elektronen in een monster, waardoor ze loskomen. Die uitgeworpen elektronen bevatten waardevolle informatie. In dit geval gaven ze extra inzicht in het gedrag van de methanol op het Cu-oppervlak en de omgevingsomstandigheden, in realtime. Met APXPS kunnen onderzoekers gemakkelijker molecuuldekking op oppervlakken berekenen dan met IR-spectroscopie.
Naarmate de tijd verstreek, werd de overmaat methoxy geëlimineerd naarmate er meer en meer waterstof werd geproduceerd, waardoor koolmonoxide achterbleef dat als een gas uit het koper de-adsorbeerde. De methoxy die overbleef bereikte een punt van gelijkmatige dekking - een evenwichtspunt. Met name de kinetiek van dit proces was aanzienlijk sneller op het meer los gepakte Cu-oppervlak in vergelijking met de andere twee, die dichter gepakt zijn.
In toekomstig werk is de groep van plan om door te gaan met het bestuderen van methanol/Cu-systemen om meer te weten te komen over hun dynamiek en of sommige van deze gedragingen kunnen worden gevonden in andere systemen dan methanol op Cu. + Verder verkennen
Op heterdaad betrapt:belangrijke chemische tussenproducten bij de reactie van verontreinigende stof tot brandstof geïdentificeerd
Hoofdlijnen
- Wat maakt de mens menselijk?
- Wetenschappers maken een einde aan een mysterie van 50 jaar en onthullen hoe bacteriën zich kunnen verplaatsen
- Wel of niet fokken? Trekkende vrouwelijke vlinders staan voor een moessondilemma
- Hoe een tRNA-reeks te krijgen van een DNA-reeks
- Hoe is de katoenplant aangepast om te overleven?
- Wat kan je spit je vertellen over je DNA?
- Roofzuchtige bacteriën die patrijspoorten maken en fresco's schilderen in schadelijke bacteriën
- Warmteminnende bacteriën van een Antarctische vulkaan kunnen olieverontreiniging helpen aanpakken
- Sahelanthropus, de oudste vertegenwoordiger van de mensheid, was inderdaad tweevoetig
- Goed passende brandvertragende werkkleding voor dames

- Microben kunnen de productie van geneesmiddelen efficiënter maken
- Machine learning voorspelt mechanische eigenschappen van poreuze materialen
- Verbeterde stabiliteit in de aanwezigheid van water kan de uitstoot van broeikasgassen in de schoorsteen helpen verminderen
- Planten modelleren efficiëntere thermische koelingsmethode

 Aurora-mysteries ontgrendeld met NASA's THEMIS-missie
Aurora-mysteries ontgrendeld met NASA's THEMIS-missie Wetenschappers turbochargeren hoge resolutie, 3D-beeldvorming
Wetenschappers turbochargeren hoge resolutie, 3D-beeldvorming Isotopen – Verbeterd proces voor medicijnen
Isotopen – Verbeterd proces voor medicijnen Chinese smartphonegigant Xiaomi debuteert in Londen
Chinese smartphonegigant Xiaomi debuteert in Londen Arctische meren ontdooien elk jaar vroeger
Arctische meren ontdooien elk jaar vroeger Waarom hebben mensen andere haarkleur?
Waarom hebben mensen andere haarkleur?  In San Francisco, tech-boom heeft ervoor gezorgd dat mensen hun huis niet hebben geprijsd
In San Francisco, tech-boom heeft ervoor gezorgd dat mensen hun huis niet hebben geprijsd Organische polymeren tonen zonnig potentieel
Organische polymeren tonen zonnig potentieel
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


