
Wetenschap
Onthulde ontbrekende stap in de vorming van lipiden kan detectie van vroegere klimaten mogelijk maken
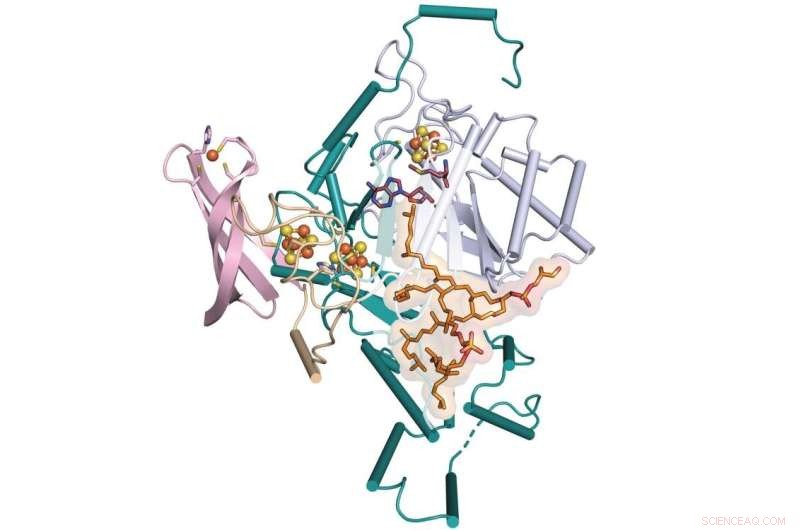
Een team van Penn State en de University of Illinois Urbana-Champaign heeft de ontbrekende stap bepaald in de vorming van een molecuul genaamd GDGT, dat een veelbelovende kandidaat is voor gebruik als indicator van het klimaat in het verleden. Het team bepaalde de röntgenkristalstructuur van een enzym dat dit proces faciliteert, GDGT/MAS genaamd, dat hier is gebonden aan aanvullende cofactoren. Krediet:Booker Lab / Penn State
De ontbrekende stap in de vorming van een lipidemolecuul waarmee bepaalde eencellige organismen de meest extreme omgevingen op aarde kunnen overleven, is nu ontcijferd. Dit nieuwe begrip, ontdekt door een team van biochemici van Penn State en de University of Illinois Urbana-Champaign, zou het vermogen van de lipiden kunnen verbeteren om te worden gebruikt als een indicator van temperatuur in de geologische tijd.
Het lipide, glyceroldibifytanylglyceroltetraether (GDGT) genoemd, wordt aangetroffen in het celmembraan van sommige soorten archaea, eencellige organismen waarvan oorspronkelijk werd gedacht dat het bacteriën waren, maar die nu als een aparte groep worden beschouwd. Dit lipide biedt de stabiliteit voor sommige soorten om te gedijen in omgevingen met extreem hoge temperaturen, zoutgehalte of zuurgraad, zoals thermische ventilatieopeningen in de oceaan, warmwaterbronnen en hyperzout water. De unieke stabiliteit van GDGT maakt het ook mogelijk om het honderden of zelfs duizenden jaren nadat het organisme sterft te detecteren. Omdat deze organismen de neiging hebben om meer GDGT te produceren bij hogere temperaturen, wordt het beschouwd als een veelbelovende kandidaat voor het schatten van de temperatuur over de geologische tijd.
"Om GDGT nauwkeurig te kunnen gebruiken als een proxy om veranderingen in geologische temperaturen te reconstrueren, moeten wetenschappers beter begrijpen hoe het wordt gemaakt, welke genen ervoor coderen en welke soorten het kunnen creëren", zegt Squire Booker, een biochemicus bij Penn State , een onderzoeker bij het Howard Hughes Medical Institute, en leider van het onderzoeksteam. "Maar tot nu toe was er een ontbrekende stap in de vorming van dit lipide. We gebruikten beeldvormingstechnieken in combinatie met chemische en biochemische methoden om de chemische route voor deze ontbrekende stap te deconstrueren."
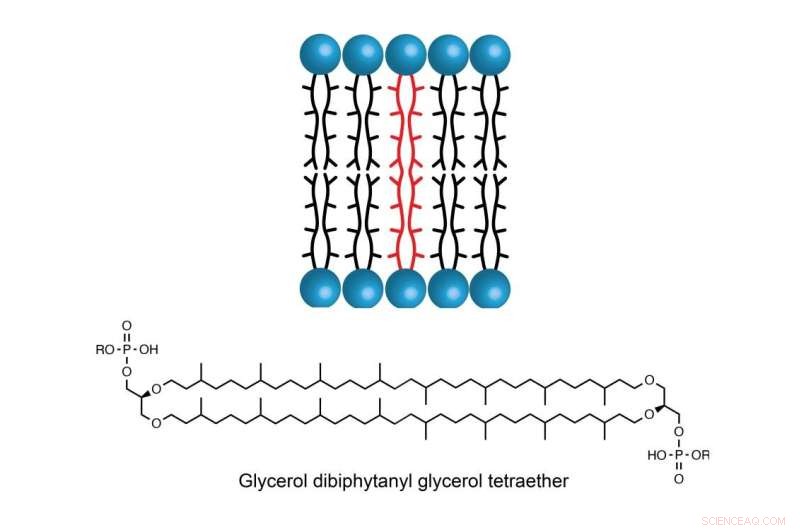
Het molecuul GDGT wordt aangetroffen in het celmembraan van sommige soorten archaea, waardoor de eencellige organismen kunnen gedijen in omgevingen met extreem hoge temperaturen, zoutgehalte of zuurgraad. Krediet:Booker Lab / Penn State
De stabiliteit van GDGT is gedeeltelijk te danken aan de twee lange koolwaterstofketens die zich door het membraan uitstrekken. Maar hoe deze twee ketens aan elkaar worden gekoppeld, heeft wetenschappers tientallen jaren in verwarring gebracht.
"Het koppelen van de koolstoffen aan het einde van de twee koolwaterstofketens is echt een uitdaging voor de chemie omdat ze inert zijn - ze zijn chemisch inactief", zegt Cody Lloyd, een afgestudeerde student aan Penn State en een lid van het onderzoeksteam. "We hebben het enzym geïdentificeerd dat deze terminale koolstoffen activeert en deze koppeling mogelijk maakt. Bovendien kennen we nu het gen dat voor dit enzym codeert, wat het gebruik van GDGT als indicator van vroegere klimaten zou moeten verbeteren."
Het enzym dat de koppeling van de twee koolwaterstofketens vergemakkelijkt, behoort tot een klasse van eiwitten die radicale SAM-eiwitten worden genoemd en waarvan bekend is dat ze een belangrijke rol spelen in een verscheidenheid aan chemische reacties, waaronder de productie van antibiotica, de modificatie van eiwitten, DNA en RNA, en de creatie van verschillende biomoleculen.
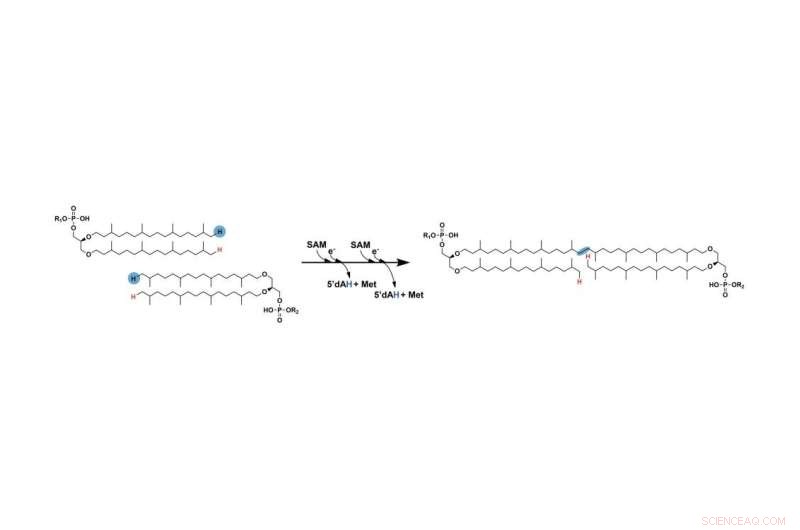
De voorheen ontbrekende stap in de vorming van GDGT omvat het verbinden van twee lange koolwaterstofketens. De twee blauw gemarkeerde waterstofatomen worden uiteindelijk verwijderd en de ketens verbinden zich uiteindelijk op de plekken waar die atomen zijn verwijderd. Een radicaal SAM-enzym vergemakkelijkt dit proces. Krediet:Booker Lab / Penn State
De eerste stap is vergelijkbaar met die van andere reacties waarbij radicale SAM-enzymen betrokken zijn:het radicale SAM-enzym gebruikt een van zijn ijzer-zwavelclusters om een molecuul genaamd S-adenosyl-L-methionine (SAM) te splitsen, waardoor een "vrije radicaal" ontstaat. of een ongepaard elektron dat zeer reactief is en de reactie vooruit helpt. Vervolgens plukt de radicaal een waterstofatoom van de koolstof aan het einde van de keten. In een latere stap herhaalt dit proces zich met de tweede keten met behulp van een tweede molecuul SAM.
"Uiteindelijk binden de koolstofatomen aan het einde van elk van de ketens aan elkaar op de plaats waar de waterstofatomen zijn verwijderd", zei Lloyd. "Maar zodra de waterstof van de eerste keten is verwijderd, wordt het zo onstabiel dat het met vrijwel alles kan reageren. Om tijdelijk te voorkomen dat de eerste keten reageert met off-targets, bindt de koolstof zich aan een zwavelatoom van een ander de drie ijzerzwavelclusters van het enzym."
Zodra de waterstof uit de tweede keten is verwijderd, moedigt het resulterende radicaal de eerste keten aan om zichzelf te verwijderen van de ijzer-zwavelcluster op het enzym en in plaats daarvan te binden aan de tweede keten. Dit resulteert erin dat de twee ketens aan elkaar worden gebonden, wat de ontbrekende stap in de vorming van GDGT voltooit. De onderzoekers presenteren hun resultaten in een paper die online en in print verschijnt in het nummer van 1 september van het tijdschrift Nature .
"Dit is een volledig nieuw gebruik van een ijzer-zwavelcluster, en dit is het eerste voorbeeld in de natuur van de koppeling van twee volledig inerte koolstofatomen met deze elektronenconfiguratie, die chemici sp3 gehybridiseerd noemen," zei Booker. "Er is veel interesse geweest in het maken van dit soort koolstof-koolstofbindingen van sp3-gehybridiseerde koolstoffen als onderdeel van farmaceutische en andere industriële producten. De natuur heeft miljoenen jaren de tijd gehad om dit uit te zoeken, dus we blijven naar de natuur kijken voor inspiratie voor synthetische reacties, zoals dit nieuwe gebruik van een ijzer-zwavelcluster." + Verder verkennen
De sleutel tot de vorming van een krachtig antibioticum is nu duidelijk
 Onderzoekers vinden bewijs om het gedrag van langzame aardbevingen te verklaren
Onderzoekers vinden bewijs om het gedrag van langzame aardbevingen te verklaren Gigantische lavakoepel bevestigd in de Japanse Kikai Caldera
Gigantische lavakoepel bevestigd in de Japanse Kikai Caldera Het omzetten van voedselafval in diervoeder kan een deel van de uitstoot van vee wegnemen
Het omzetten van voedselafval in diervoeder kan een deel van de uitstoot van vee wegnemen Emissies van elektriciteitsopwekking leiden tot vroegtijdige sterfgevallen voor sommige raciale groepen
Emissies van elektriciteitsopwekking leiden tot vroegtijdige sterfgevallen voor sommige raciale groepen Succesvolle opnames van de snelste aurora-flikkering
Succesvolle opnames van de snelste aurora-flikkering
Hoofdlijnen
- Wat zijn drie primaire doelen van mitose?
- Orgelsystemen betrokken bij homeostase
- Nieuw apparaat zoomt in op microbengedrag op de juiste schaal
- Onderzoekers presenteren nieuw wiskundig model voor het bestuderen van niercellen
- De methoden van inventarisatie in Microbes
- Van Alaska tot Amazonia:de eerste wereldwijde kaarten met eigenschappen die de groei van vegetatie stimuleren
- Meld-en-klauwzeer:de lacunes in de inspanningen van Zuid-Afrika om het onder controle te houden
- Vergelijking voor glucosemetabolisme
- Zijn mensen het slimste dier?
- Windturbinebladen kunnen ooit worden gerecycled tot zoete lekkernijen

- Nieuw slim polymeer gloeit helderder wanneer uitgerekt

- Nieuwe meettechniek kan pulpfabrieken miljoenen besparen

- Lab-gekweekte pigmenten en voedselbijproducten:de toekomst van natuurlijke textielkleurstoffen

- Nieuwe machine learning-benadering vergemakkelijkt het zoeken naar moleculaire conformeren in complexe moleculen
 Stikstof verminderen met boor en bier
Stikstof verminderen met boor en bier Schoolprojecten: Elektrisch project
Schoolprojecten: Elektrisch project  De pandemische recessie heeft 9,8 miljoen meer Amerikanen in voedselonzekerheid geduwd
De pandemische recessie heeft 9,8 miljoen meer Amerikanen in voedselonzekerheid geduwd Eerste Arabische set voor ISS zegt dat reis geschiedenis zal schrijven
Eerste Arabische set voor ISS zegt dat reis geschiedenis zal schrijven Wat gebeurt er als u water geeft met frisdrank?
Wat gebeurt er als u water geeft met frisdrank?  Ambtenaren, kiezers, meer bezorgd zijn over oceaanafval na presentaties van kinderen
Ambtenaren, kiezers, meer bezorgd zijn over oceaanafval na presentaties van kinderen Overzicht van Chinees atmosferisch wetenschappelijk onderzoek in de afgelopen 70 jaar:klimaat en klimaatverandering
Overzicht van Chinees atmosferisch wetenschappelijk onderzoek in de afgelopen 70 jaar:klimaat en klimaatverandering Waarom we soms een hekel hebben aan de goede man
Waarom we soms een hekel hebben aan de goede man
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

