
Wetenschap
Verborgen symmetrie gevonden in chemische kinetische vergelijkingen
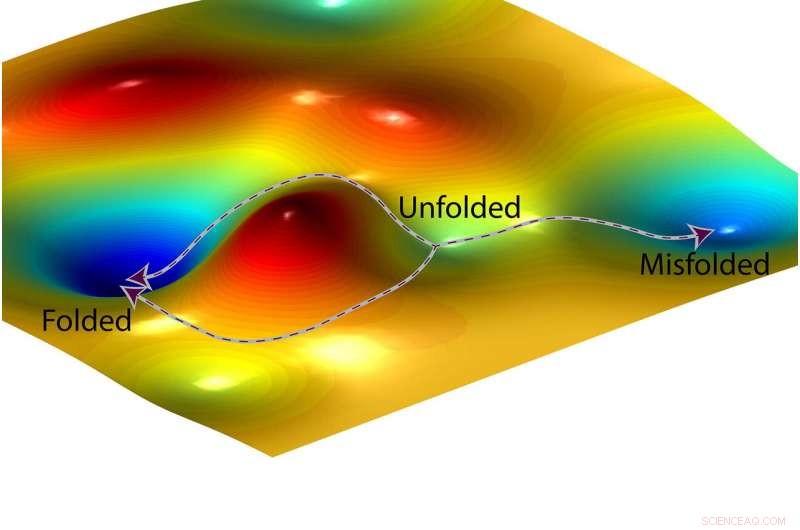
Een artistieke weergave van een landschap met vrije energie en twee mogelijke paden die een eiwit kan volgen (links) om correct te vouwen en een derde pad (rechts) dat leidt tot een verkeerd gevouwen toestand. Krediet:O. Igoshin/Rice University
Onderzoekers van Rice University hebben een verborgen symmetrie ontdekt in de chemische kinetische vergelijkingen die wetenschappers lang hebben gebruikt om veel van de chemische processen die essentieel zijn voor het leven te modelleren en te bestuderen.
De vondst heeft gevolgen voor het ontwerp van geneesmiddelen, genetica en biomedisch onderzoek en wordt beschreven in een studie die deze maand in de Proceedings van de National Academy of Sciences . Om de biologische gevolgen te illustreren, studie co-auteurs Oleg Igoshin, Anatoly Kolomeisky en Joel Mallory van Rice's Centre for Theoretical Biological Physics (CTBP) gebruikten drie brede voorbeelden:eiwitvouwing, enzymkatalyse en motorproteïne-efficiëntie.
In ieder geval, de onderzoekers toonden aan dat een eenvoudige wiskundige verhouding laat zien dat de kans op fouten wordt bepaald door kinetiek in plaats van thermodynamica.
"Het kan een eiwit zijn dat zich in de juiste versus de verkeerde conformatie vouwt, een enzym dat het juiste versus het verkeerde aminozuur in de polypeptideketen opneemt, of een motoreiwit dat per ongeluk achteruit stapt in plaats van vooruit, " zei Igoshin, een CTBP-onderzoeker en hoogleraar bio-engineering bij Rice. "Al die eigenschappen kunnen worden uitgedrukt als een verhouding van twee stationaire fluxen, en we ontdekten dat biologische eigenschappen die in deze termen worden uitgedrukt onder kinetische controle staan."
Het voorbeeld van het vouwen van eiwitten illustreert de implicaties voor het ontwerp van geneesmiddelen. Alle eiwitten vouwen in een karakteristieke vorm, en een fractie verkeerd gevouwen in de verkeerde vorm. Het verkeerd vouwen van eiwitten is in verband gebracht met enkele erfelijke genetische aandoeningen en ziekten, en medicijnmakers zijn geïnteresseerd in het maken van medicijnen die de kans op het verkeerd vouwen van eiwitten kunnen verkleinen.
Voordat het vouwt, een eiwit heeft energie, als een bal die bovenop een heuvel zit. Folding is de afdaling van dit energieke startpunt naar de plaats waar de bal stopt met rollen. Chemici gebruiken vaak een visueel hulpmiddel dat een "vrije-energielandschap" wordt genoemd om energieniveaus in chemische reacties in kaart te brengen. Het landschap ziet eruit als een bergketen met toppen en dalen, en de afdaling van het uitgevouwen startpunt van een eiwit naar het volledig opgevouwen eindpunt kan eruitzien als een bergweg die door een reeks valleien slingert. Zelfs als een stad langs de weg lager ligt, een reiziger moet misschien heuvels beklimmen om van de ene vallei naar de andere te komen op de weg naar beneden.
"We hebben laten zien dat het de barrières zijn, de hoge punten tussen valleien, die deze verhoudingen bepalen, ' zei Igoshin. 'De diepten van de valleien doen er niet toe.
"Als je een medicijn wilt krijgen dat een eiwit helpt om correct te vouwen, bijvoorbeeld, onze voorspelling is dat het medicijn een barrière langs het vouwpad moet kunnen verminderen, "zei hij. "Als het alleen de valleien treft, bijvoorbeeld door de stabiliteit van sommige intermediaire conformaties langs het vouwpad te verbeteren, het zal de verhouding van keren dat het eiwit correct versus fout vouwt niet veranderen."
Igoshin zei dat het werk voortkwam uit een onderzoek uit 2017 waarin hij, Kolomeisky en voormalig CTBP-postdoctoraal onderzoeker Kinshuk Banerjee toonden aan dat de nauwkeurigheid van enzymatische katalyse kinetisch werd gecontroleerd. Igoshin beschreef de ontdekking als een "soort onderliggende symmetrie van vergelijkingen."
"Als je kijkt naar de verhoudingen van fluxen, je krijgt deze interessante annulering, en alle termen die met deze waarden te maken hebben, heffen elkaar op, en je krijgt de onveranderlijkheid, " zei hij. "Toen we dit resultaat voor het eerst kregen, het leek ons contra-intuïtief. Vervolgens, we wisten niet zeker of het toeval was, omdat we het in het vorige artikel voor slechts twee specifieke kinetische schema's lieten zien. Het werk van Joel heeft nu aangetoond dat het kan worden gegeneraliseerd naar dit brede scala aan systemen."
Igoshin zei dat de symmetrie "niet zo moeilijk te bewijzen was, maar niemand heeft het eerder opgemerkt."
"Ik denk dat het een zeer interessant fysiek resultaat is dat grote implicaties heeft in de biologie, " zei hij. "Het zou kunnen helpen de grenzen te bepalen van wat mogelijk is in termen van het beheersen en optimaliseren van eigenschappen op systeemniveau in veel biologische processen."
 Nieuw ontwerp van roterende vloeistofreactor lost problemen op met huidige reactoren
Nieuw ontwerp van roterende vloeistofreactor lost problemen op met huidige reactoren Fabrikanten van generieke geneesmiddelen zien nieuwe kansen in het verschiet
Fabrikanten van generieke geneesmiddelen zien nieuwe kansen in het verschiet Unieke medicijnstructuren vinden met kunstmatige intelligentie en chemie
Unieke medicijnstructuren vinden met kunstmatige intelligentie en chemie Onderzoekers creëren methode die infecties snel en nauwkeurig kan detecteren
Onderzoekers creëren methode die infecties snel en nauwkeurig kan detecteren Theoretische opbrengsten berekenen
Theoretische opbrengsten berekenen
 Grote hiaten in onderzoek naar microplastics in Noord-Amerika, studie vondsten
Grote hiaten in onderzoek naar microplastics in Noord-Amerika, studie vondsten Soorten zoetwaterschildpadden
Soorten zoetwaterschildpadden  Modellen suggereren dat fouten verbonden zijn via Californias Imperial Valley
Modellen suggereren dat fouten verbonden zijn via Californias Imperial Valley Wasmiddelmoleculen kunnen fluctuaties in atmosferische methaanconcentraties veroorzaken
Wasmiddelmoleculen kunnen fluctuaties in atmosferische methaanconcentraties veroorzaken Een giftige chemische stof in mariene ecosystemen blijkt een heilzame rol te spelen
Een giftige chemische stof in mariene ecosystemen blijkt een heilzame rol te spelen
Hoofdlijnen
- Gescheiden sinds de dinosauriërs, bamboe-etende lemuren, panda's delen gemeenschappelijke darmmicroben
- Ecologische onderzoeksmethoden: observeren, experimenteren en modelleren
- Maakt Koud U Slaperig?
- Team publiceert onderzoek naar ongewone genevolutie in bacteriën
- Wetenschappers vinden potentiële wapens voor de strijd tegen antibioticaresistentie
- Hoe maak je een 3D-model van het spierstelsel voor een wetenschapsklasse
- Hoe zijn fotosynthese en cellulaire ademhaling gerelateerd?
- Begrazing van vee schaadt leefgebied van reuzenpanda's
- Is er eerder enige vorm van exploratie op Mercurius gedaan
- Moleculaire draden bouwen, één atoom tegelijk
- Hoe de hoeveelheid koper (II) sulfaat pentahydraat te berekenen

- Kan kunstmatige intelligentie nieuwe deuren openen voor het ontdekken van materialen?

- Onderzoekers breiden forensische methode uit om mensen te identificeren die eiwitten uit botten gebruiken

- Lichtgewicht van periodiek systeem speelt grote rol in het leven op aarde

 Wetenschappers wenden zich tot vuurvliegjes om de OLED-efficiëntie te verbeteren
Wetenschappers wenden zich tot vuurvliegjes om de OLED-efficiëntie te verbeteren Gebruik van recombinant DNA in Agriculture
Gebruik van recombinant DNA in Agriculture Robotboot vaart de geschiedenis in door de Atlantische oversteek te voltooien
Robotboot vaart de geschiedenis in door de Atlantische oversteek te voltooien Resonantie: definitie, types, frequentie en voorbeelden
Resonantie: definitie, types, frequentie en voorbeelden Elektrotechnisch team ontwikkelt verder dan 5G draadloze transceiver
Elektrotechnisch team ontwikkelt verder dan 5G draadloze transceiver Leveren van duurzaam geproduceerde bouwstenen van biomateriaal uit plantaardige grondstoffen
Leveren van duurzaam geproduceerde bouwstenen van biomateriaal uit plantaardige grondstoffen Kleurstoffen uit atmosferische kooldioxide
Kleurstoffen uit atmosferische kooldioxide SpaceX klaar om NASA's nieuwe planeetjager te vernietigen, TESS
SpaceX klaar om NASA's nieuwe planeetjager te vernietigen, TESS
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

