
Wetenschap
Nieuw model beschrijft fasescheiding die antilichaamoplossingen bederft
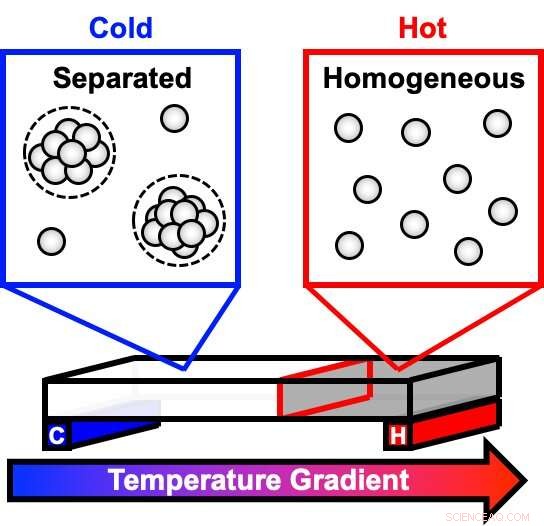
Een nieuwe studie gebruikte een temperatuurgradiënt om te observeren hoe sterk geconcentreerde antilichaamoplossingen, zoals die in sommige medicijnen voorkomen, opsplitsen in fasen, als een olie- en wateroplossing. Bij koudere temperaturen, troebele druppeltjes beginnen zich te vormen in de eens heldere oplossing. Naarmate de druppeltjes groeien en naar de bodem van de container zakken, de oplossing scheidt zich in twee verschillende fasen. Deze fasescheiding kan de houdbaarheid en stabiliteit van een medicijn beïnvloeden. Krediet:Cremer Lab, Penn State
Een nieuw wiskundig model beschrijft hoe sterk geconcentreerde antilichaamoplossingen zich in verschillende fasen scheiden, vergelijkbaar met een mengsel van olie en water. Deze scheiding kan de stabiliteit en houdbaarheid van sommige geneesmiddelen die monoklonale antilichamen gebruiken, verminderen, waaronder enkele die worden gebruikt voor de behandeling van auto-immuunziekten en kanker. Een team van wetenschappers van Penn State en MedImmune, LLC (nu AstraZeneca) onderzocht de thermodynamica en kinetiek, de relaties tussen temperatuur, energie, en de snelheden van chemische reacties, van het fenomeen met behulp van een innovatieve methode die de snelle studie van meerdere monsters tegelijk mogelijk maakt. Een paper waarin hun model wordt beschreven, verschijnt op 22 juli, 2019, in het journaal Proceedings van de National Academy of Sciences .
Veel medicijnen worden tegenwoordig als vaste stoffen opgeslagen en opgelost in IV-zakken voor levering aan patiënten, maar de farmaceutische industrie is op weg naar medicijnen die als vloeistof kunnen worden bewaard en via een injectie kunnen worden toegediend. Sommige van deze medicijnoplossingen, zoals die worden gebruikt voor de behandeling van auto-immuunziekten en sommige vormen van kanker, hoge concentraties monoklonale antilichamen bevatten - eiwitten die zich hechten aan lichaamsvreemde stoffen, zoals bacteriën en virussen, ze markeren voor vernietiging door het immuunsysteem van de patiënt.
"Hooggeconcentreerde eiwitoplossingen kunnen in verschillende fasen uiteenvallen, zoals een vinaigrette-saladedressing die in de loop van de tijd in lagen uiteenvalt, " zei Bradley Rogers, afgestudeerde student scheikunde aan Penn State en eerste auteur van het artikel. "Fasescheiding is een van de wegen die deze medicijnen onstabiel en ongeschikt maken voor gebruik. De klassieke methode om dit proces te begrijpen, omvat het manipuleren van de temperatuur van één monster in de loop van de tijd. We gebruikten een microfluïdica-platform met temperatuurgradiënt om snel naar veel temperaturen tegelijk te kijken. "
Een antilichaamrijke oplossing begint als een heldere vloeistof bij kamertemperatuur, maar als de oplossing afkoelt, troebele druppeltjes beginnen zich te vormen. Overuren, de druppeltjes zakken naar de bodem, met verdunde vloeistof bovenop, waardoor het monster duidelijk lijkt. Het team gebruikte een innovatief apparaat dat een reeks temperaturen over een temperatuurgradiënt creëert en gebruikte een techniek genaamd dark-field imaging om te meten hoe snel dit proces plaatsvindt. Vervolgens berekende het team verschillende parameters om de thermodynamica en kinetiek van het systeem beter te begrijpen, inclusief de temperaturen waarbij faseovergangen plaatsvinden en de hoeveelheid energie die nodig is om van de ene fase naar de volgende te gaan - activeringsenergieën.
"We hebben vastgesteld dat de snelheid waarmee een oplossing in twee fasen wordt gescheiden, een vreemde afhankelijkheid van temperatuur heeft, " zei Rogers. "Deze relatie is veel gecompliceerder voor geconcentreerde antilichaamoplossingen dan voor andere systemen. We hebben lang geprobeerd om de gegevens te begrijpen, maar uiteindelijk hebben we een model ontwikkeld dat verklaart wat we zien."
Het model beschrijft hoe antilichaammoleculen aan elkaar plakken als de temperatuur daalt, vormen druppeltjes die groeien als extra moleculen samenkomen. Dit omkeerbare proces gebeurt steeds sneller met dalende temperatuur, omdat de oplossing steeds meer verzadigd raakt met vrije antilichaammoleculen. Vervolgens, terwijl de oplossing blijft afkoelen, druppeltjes kleven aan andere druppeltjes en zakken naar de bodem. Bij nog koudere temperaturen, de oplossing vormt een gel en kan de scheiding niet voltooien, zelfs in de loop van een maand.
"In een enkel experiment we kunnen de homogene heldere oplossing visualiseren, de troebele oplossing als druppeltjes beginnen te vormen, de fasegescheiden vloeistof, en de gel, zei Paul Cremer, J. Lloyd Huck leerstoel natuurwetenschappen aan Penn State en senior auteur van het artikel. "Eerder onderzoek beschreef deze verschillende toestanden, en ons model beschrijft de wiskunde en temperatuurafhankelijke kinetiek achter wat wij denken dat er gebeurt."
Volgende, het onderzoeksteam is van plan te onderzoeken of hun model fasescheiding in andere systemen kan verklaren. Ze zijn ook van plan om te testen of parameters die uit dit soort experimenten zijn verzameld, de stabiliteit en houdbaarheid van therapieën kunnen voorspellen.
"Als deze parameters ons kunnen helpen de stabiliteit en houdbaarheid te voorspellen, kunnen we misschien betere kandidaat-geneesmiddelen selecteren, " zei Rogers. "We kunnen misschien ook de ideale oplossingseigenschappen bepalen voor een veelbelovend kandidaat-geneesmiddel om het stabiel te houden."
Naast Rogers en Cremer, the research team includes Kelvin Rembert, Matthew Poyton, Halil Okur, Amanda Kale, and Tinglu Yang at Penn State and Jifeng Zhang from AstraZeneca. The work was supported by MedImmune LLC (now AstraZeneca). Additional support was provided by the National Science Foundation.
 Op kobalt gebaseerde katalysatoren kunnen de productie van waterstof uit water op industriële schaal versnellen
Op kobalt gebaseerde katalysatoren kunnen de productie van waterstof uit water op industriële schaal versnellen Synthese op het oppervlak van grafeenmoleculen en hun superroosters
Synthese op het oppervlak van grafeenmoleculen en hun superroosters Enzym-aangedreven protocellen stijgen naar de top
Enzym-aangedreven protocellen stijgen naar de top Wat is de standaardmethode voor kalibratie van een geleidbaarheidsmeter?
Wat is de standaardmethode voor kalibratie van een geleidbaarheidsmeter?  Wetenschappers ontdekken hoe oppervlakken het vroege leven op aarde hebben kunnen helpen beginnen
Wetenschappers ontdekken hoe oppervlakken het vroege leven op aarde hebben kunnen helpen beginnen
 Geologen publiceren nieuwe details over de evolutie van de Oost-Afrikaanse Rift Valley
Geologen publiceren nieuwe details over de evolutie van de Oost-Afrikaanse Rift Valley De natuur heeft mensen nodig en hier is waarom
De natuur heeft mensen nodig en hier is waarom Bossen planten kan de planeet meer afkoelen dan gedacht
Bossen planten kan de planeet meer afkoelen dan gedacht Gebruikten microben om giftig elektronisch afval op te ruimen - hier is hoe
Gebruikten microben om giftig elektronisch afval op te ruimen - hier is hoe De rol van het klimaat op de evolutie van sedimenten en riffen ontrafelen over millennial-tijdschalen
De rol van het klimaat op de evolutie van sedimenten en riffen ontrafelen over millennial-tijdschalen
Hoofdlijnen
- Wat is een extra ring van DNA in bacteriën?
- Wat is het verschil tussen planten, schimmels en dieren?
- Chimpstudie onthult hoe de hersenstructuur onze evolutie heeft gevormd
- Leeftijd van moeders beïnvloedt genetische overeenkomst tussen tweelingen
- Nieuwe database catalogiseert planten die verontreiniging opnemen
- Wat is een molecuul dat wordt geproduceerd door DNA uit twee verschillende bronnen te combineren?
- Wat is de functie van tracking-kleurstof in gelelektroforese?
- Diversiteit van grote dieren speelt een belangrijke rol in koolstofcyclus
- Drie soorten vezelig bindweefsel
- Wetenschappers ontwerpen manier om onschadelijke bacteriën te gebruiken om zware metalen in drinkwater te detecteren

- Microdeeltjes gecreëerd door een nieuwe 3D-fabricagemethode kunnen lang na injectie medicijnen of vaccins vrijgeven

- Hoe maakten de oude meesters hun ultramarijn?
- Nieuwe bevindingen werpen licht op de ontwikkeling van op liposomen gebaseerde remmers
- Slimme inkt voegt nieuwe dimensies toe aan 3D-printen

 Hoe de symmetrie lijn te vinden in een kwadratische vergelijking
Hoe de symmetrie lijn te vinden in een kwadratische vergelijking  Flood-projecten voor School
Flood-projecten voor School Schedelscans vertellen hoe 's werelds eerste honden hun prooi vingen
Schedelscans vertellen hoe 's werelds eerste honden hun prooi vingen Botten uit de La Brea-teerputten tonen de gevaren van een kieskeurige eter
Botten uit de La Brea-teerputten tonen de gevaren van een kieskeurige eter Spiraalvormig licht, nanodeeltjes en inzichten in de structuur van levens
Spiraalvormig licht, nanodeeltjes en inzichten in de structuur van levens China zendt ruimtevaartuigfoto's uit vanaf de verre kant van de manen
China zendt ruimtevaartuigfoto's uit vanaf de verre kant van de manen Kleine injecteerbare sensor kan onopvallende, alcoholcontrole op lange termijn
Kleine injecteerbare sensor kan onopvallende, alcoholcontrole op lange termijn Door de bomen het bos missen:een onverwacht beeld van de bossen in New York City
Door de bomen het bos missen:een onverwacht beeld van de bossen in New York City
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

