
Wetenschap
Wetenschappers lossen ruwe olie op in water om de samenstelling ervan te bestuderen

Illustratie. Olie opgelost in water. Krediet:@tsarcyanide/MIPT
Onderzoekers van MIPT, Skoltech, het Gezamenlijk Instituut voor Hoge Temperaturen van de Russische Academie van Wetenschappen, en Lomonosov Moscow State University rapporteren een nieuwe benadering van analyse van oliesamenstelling. Ze gebruikten hoge temperaturen en druk om olie op te lossen in water en de samenstelling ervan te analyseren. De nieuwe methode voldoet aan de principes van groene chemie, omdat er geen milieugevaarlijke oplosmiddelen nodig zijn. De krant is gepubliceerd in Analytische en bioanalytische chemie .
Ruwe olie wordt bijna nooit in zijn ruwe vorm gebruikt. Maar het is noodzakelijk om de precieze samenstelling te kennen om de raffinage zo efficiënt mogelijk te maken. Ruwe olie bestaat uit meer dan 100, 000 verbindingen, waarbij de exacte samenstelling van het monster varieert op basis van het veld waaruit het is geëxtraheerd. De extreme complexiteit van ruwe olie maakt het onmogelijk om ze in afzonderlijke verbindingen te scheiden. Zwaardere fracties, die bij 300 graden Celsius niet vluchtig zijn, moeten nog goed worden bestudeerd. Het is bekend dat ze voornamelijk uit fenolen bestaan, ketonen, carbazolen, pyridinen, chinolinen, dibenzofuranen en carbonzuren. Naast dat, ruwe olie uit sommige velden kan ook zwavelverbindingen bevatten. Veel koolwaterstoffen hebben identieke formules, met hetzelfde aantal koolstof, waterstof, en zuurstofatomen, maar verschillen in hun regelingen, d.w.z., het zijn isomeren.
De enorm verschillende structuren vertonen duidelijk verschillende chemische eigenschappen. Zwaardere koolwaterstoffen bestaan uit veel atomen, wat meer structurele variabiliteit voor elke verbinding betekent.
Massaspectrometrie geeft informatie over de elementaire samenstelling van stoffen en hun molecuulmassa, maar maakt vaak geen onderscheid tussen verschillende isomeren. Dergelijke informatie kan worden verkregen door analyse van isotopenuitwisseling. Deze methode is gebaseerd op het feit dat, afhankelijk van welke specifieke verbindingen ruwe olie of een ander monster vormen, zuurstof- en waterstofatomen zullen meer of minder tijd nodig hebben om te worden vervangen door hun isotopen - in wezen dezelfde elementen, maar met een andere massa. Water is de meest gemakkelijk beschikbare en de schoonste bron van isotopen, maar olie is onder normale omstandigheden onoplosbaar in water, dus krachtige zuren en alkali moeten in plaats daarvan worden gebruikt. Maar zuren hebben de neiging om organische verbindingen af te breken, vooral bij hoge temperaturen, waardoor de samenstelling van het monster verandert.
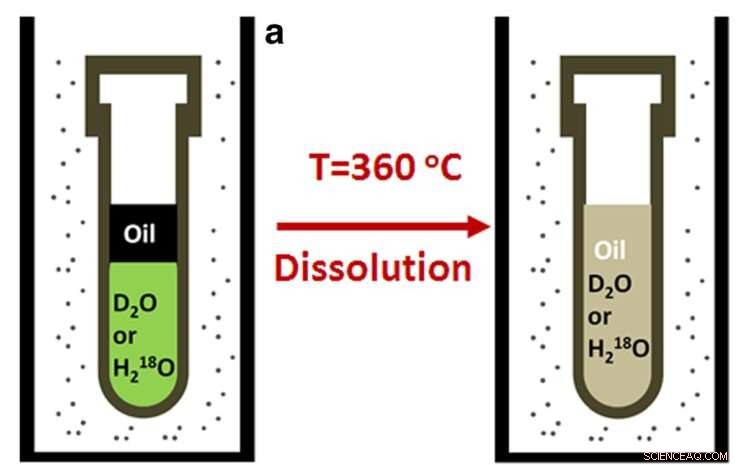
Figuur 1. Olie opgelost in oververhit water Credit:Reserachers
Het is bekend, echter, dat in water onoplosbare verbindingen kunnen worden opgelost in oververhitte, of superkritisch, water bij temperaturen aanzienlijk meer dan 100 graden C, daarom werd besloten deze methode toe te passen op ruwe olie. De onderzoekers bewezen dat het mogelijk was om een oplossing van ruwe olie op waterbasis te bereiken door de temperatuur en druk te verhogen en de samenstelling ervan te analyseren. Het monster werd gedurende één uur bij een druk boven 300 atm in zwaar water (waarin de waterstof vervangen is door deuterium) tot 360 graden Celsius verhit.
De onderzoekers vergeleken massaspectra van het oorspronkelijke monster en het monster na de isotoopuitwisselingsreactie. De verzamelde gegevens gaven meer informatie over de structuur van de verbindingen die ruwe olie bevatten. Deze methode kan worden gebruikt om andere complexe niet-polaire verbindingen op moleculair niveau te bestuderen.
"Isotooplabels mogen alleen op specifieke posities in het molecuul worden ingebouwd, vergelijkbaar met het lock-and-key-model, " zei professor Skoltech en MIPT Eugene Nikolaev, die ook aan het hoofd staat van het laboratorium voor massaspectrometrie bij Skoltech. "We kunnen de moleculaire structuur analyseren door massaspectrometrie met hoge resolutie te gebruiken om de wisselkoers te meten, zelfs als het onmogelijk is om afzonderlijke verbindingen te scheiden en hun structuur met andere methoden te identificeren."
"De reserves aan lichte ruwe olie raken op. Hydrokraken van stookolie, die wordt gekenmerkt door zijn zeer complexe en slecht bestudeerde moleculaire structuur, speelt een steeds grotere rol bij de productie van benzine. Hydrokrakers zijn duur, ze worden niet in Rusland geproduceerd, en ze vereisen het gebruik van speciale katalysatoren. We hebben een manier gevonden om furanen te identificeren, pyridinen, en nafteenzuren in ruwe olie zonder toevlucht te hoeven nemen tot het complexe distillatieproces, " zegt Joeri Kostyukevich, een van de auteurs van het artikel en een senior onderzoeker bij Skoltech en MIPT laboratoria. "We hopen dat ons onderzoek zal helpen om de structuur en samenstelling van ruwe olie beter te begrijpen, bijdragen aan de ontwikkeling van nieuwe katalysatoren voor efficiëntere olieraffinage, en verbeterde monitoring van de oliekwaliteit in hoofdpijpleidingsystemen mogelijk maken."
 De toekomst van biobrandstoffen in het donker
De toekomst van biobrandstoffen in het donker Moderne vervalsers ontmaskeren
Moderne vervalsers ontmaskeren Quantum dots houden atomen op afstand om katalyse te stimuleren
Quantum dots houden atomen op afstand om katalyse te stimuleren Cryo-elektronenmicroscopische structuur van een proton-geactiveerd chloridekanaal genaamd TMEM206
Cryo-elektronenmicroscopische structuur van een proton-geactiveerd chloridekanaal genaamd TMEM206 Testen van de antibacteriële eigenschappen van hydrofobe oppervlakken op het ISS
Testen van de antibacteriële eigenschappen van hydrofobe oppervlakken op het ISS
 Onderzoek naar de duurzaamheid van de Indiase suikerindustrie
Onderzoek naar de duurzaamheid van de Indiase suikerindustrie Nieuw model kan helpen bij de wederopbouw van eroderend land in de kust van Louisiana
Nieuw model kan helpen bij de wederopbouw van eroderend land in de kust van Louisiana Waar zijn alle schelpen gebleven?
Waar zijn alle schelpen gebleven?  Stoffige regenvalrecords onthullen nieuw begrip van het langetermijnklimaat op aarde
Stoffige regenvalrecords onthullen nieuw begrip van het langetermijnklimaat op aarde Satellietbeelden laten zien waar grote hoeveelheden methaan vrijkomen in het Perm Basin
Satellietbeelden laten zien waar grote hoeveelheden methaan vrijkomen in het Perm Basin
Hoofdlijnen
- Chloroplast: definitie, structuur en functie (met diagram)
- De functie van macromoleculen
- Meelkracht om voedselzekerheid te vergroten
- "3-D Printing Goes Cellular
- Hoe ziet een menselijke cel eruit?
- Hoe levert embryologie bewijs voor evolutie?
- Onderzoekers creëren 3D-celarrays voor meer realistische experimentele biologische omgevingen
- Hoe zuurstofgas wordt geproduceerd tijdens fotosynthese?
- Klimaatverandering veroorzaakt veranderingen in mariene fanerogame populaties
- Effect van menselijke activiteiten op het milieu

- Huidvaccinatie met micronaaldpleister, influenzafusie-eiwit verbetert de werkzaamheid van griepvaccins

- Team ontdekt een mechanisme dat planten gebruiken om fotosynthese in te schakelen
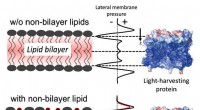
- Neutronen onderzoeken zuurstofgenererend enzym voor een groenere benadering van schoon water
- Onderzoekers ontwikkelen smartphonelezer voor snellere infectietests

 Siliciumchips combineren licht en ultrageluid voor een betere signaalverwerking
Siliciumchips combineren licht en ultrageluid voor een betere signaalverwerking Nanodeeltjestherapie die LDL en visolie gebruikt, doodt leverkankercellen
Nanodeeltjestherapie die LDL en visolie gebruikt, doodt leverkankercellen Team ontwikkelt een detector die laterale phishing-aanvallen stopt
Team ontwikkelt een detector die laterale phishing-aanvallen stopt Grade School Robot Projects
Grade School Robot Projects Manieren om landvervuiling te verminderen
Manieren om landvervuiling te verminderen  Kunstmatige intelligentie moet maatschappelijk verantwoord zijn, zegt nieuw beleidsrapport
Kunstmatige intelligentie moet maatschappelijk verantwoord zijn, zegt nieuw beleidsrapport Overschilderbare chemotherapie verkleint huidtumoren bij muizen
Overschilderbare chemotherapie verkleint huidtumoren bij muizen Sporen van oud regenwoud op Antarctica wijzen op een warmere prehistorische wereld
Sporen van oud regenwoud op Antarctica wijzen op een warmere prehistorische wereld
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

