
Wetenschap
Het ion vormen dat het universum heeft gemaakt
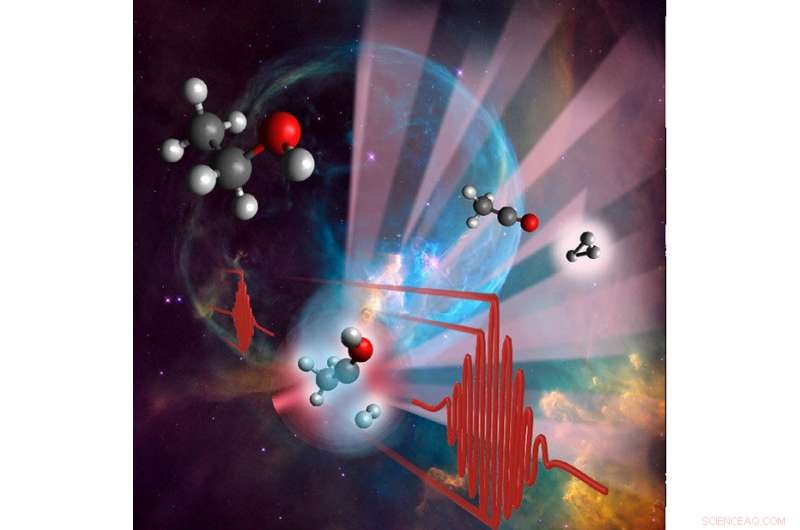
Het triwaterstofkation, H 3+ , speelt een belangrijke rol in de interstellaire chemie, waar het de vorming van water en organische moleculen vergemakkelijkt. Onderzoekers hebben ontdekt hoe het kation zich vormt wanneer organische moleculen (met name alcoholen) worden geëxciteerd door een intense laserpuls (artist rendition). Weten hoe de kationen zich vormen, brengt ons dichter bij het begrijpen van de chemie die leidde tot het leven zoals wij dat kennen. Krediet:Marcos Dantus, Michigan State universiteit
Het triwaterstofkation, H 3+ , is het startpunt voor bijna alle moleculen in het heelal. Typisch, H 3+ wordt gevormd door botsingen met waterstofgas, maar de chemie ervan op moleculair niveau is relatief onbekend. Wanneer organische moleculen worden geraakt door een laserpuls, ze worden geïoniseerd en de reactie begint. Vervolgens, de moleculen vallen uiteen in verschillende fragmenten; één daarvan is H 3+ . Ze zijn in staat om de details van deze reactie te meten:de tijdschalen, opbrengst, en hoe chemische bindingen worden verbroken en gevormd. Deze experimenten geven ook belangrijke details over elke stap van de reactie die plaatsvindt op ultrakorte (sneller dan een miljoenste van een miljoenste van een seconde) tijdschalen.
De bevindingen zijn belangrijk voor de astrochemie omdat organische moleculen, inclusief alcoholen, in de ruimte aanwezig zijn. Dit is een stap verder in het leren hoe organische moleculen zich vormen en zich gedragen in het universum. Ook, het feit dat het vormen van H 3+ een neutraal waterstofmolecuul dat rondzwerft en een ander waterstofatoom wegneemt, is significant. Waarom? Roaming-chemie is een nieuw en relatief onbekend fenomeen; dit werk biedt inzicht in dit soort chemische processen.
Wetenschappers hebben aanvullende manieren bedacht waarop het triwaterstofkation, H
3+
, het meest voorkomende ion in het heelal, wordt geproduceerd na activering met hoge energie van alcoholen en andere organische moleculen. Ondanks de sterke afstoting tussen geladen deeltjes, het team ontdekte dat een rondzwervend waterstofmolecuul verantwoordelijk was voor de chemische reactie die H . produceerde
3+
. De onderzoekers voerden het onderzoek uit met behulp van intense femtoseconde laserpulsen en instrumentatie die de resulterende ionen van experimentele metingen konden detecteren. De reactie vindt plaats in 100 of 340 quadriljoenste van een seconde, afhankelijk van het startmolecuul. Ze bevestigden de mechanismen met behulp van kwantummechanische berekeningen en door ion-ion-coïncidentiemetingen. De onderzoeksresultaten zijn belangrijk voor de astrochemie en om te begrijpen hoe organische moleculen zich vormen en zich gedragen in het universum. Verder, deze bevindingen zijn relevant wanneer intense lasers worden gebruikt voor chirurgische ingrepen.
 Onderzoekers infuseren bacteriën met zilver om de energie-efficiëntie in brandstofcellen te verbeteren
Onderzoekers infuseren bacteriën met zilver om de energie-efficiëntie in brandstofcellen te verbeteren Universele latente aniondonoren voor ultralage werkfunctie-oplossing-verwerkbare elektroden
Universele latente aniondonoren voor ultralage werkfunctie-oplossing-verwerkbare elektroden Onderzoeksteam vindt mogelijke nieuwe aanpak voor medicijnen tegen slaapziekte
Onderzoeksteam vindt mogelijke nieuwe aanpak voor medicijnen tegen slaapziekte Domino-achtige kristallisatie van glas
Domino-achtige kristallisatie van glas Onderzoekers verbinden eerst siliciumatomen op oppervlakken
Onderzoekers verbinden eerst siliciumatomen op oppervlakken
 Cry me a river:lage waterstanden zorgen voor chaos in Duitsland
Cry me a river:lage waterstanden zorgen voor chaos in Duitsland Net-zero:klimaatbesparende doelstelling of vertragingstactiek?
Net-zero:klimaatbesparende doelstelling of vertragingstactiek? Studie vindt fysieke verwering van steenafbraak belangrijker dan eerder werd erkend
Studie vindt fysieke verwering van steenafbraak belangrijker dan eerder werd erkend Over voedselketens in het toendra-ecosysteem
Over voedselketens in het toendra-ecosysteem Drastische veranderingen nodig in landbouwpraktijken om gelijke tred te houden met klimaatverandering
Drastische veranderingen nodig in landbouwpraktijken om gelijke tred te houden met klimaatverandering
Hoofdlijnen
- De cyanideverdediging:hoe één bacterie roofdieren remt met gif
- Wat maakt DNA-vingerafdrukken uniek?
- Wat gebeurt er met je cellen als je gedehydrateerd bent?
- Duiven beter in multitasken dan mensen:studie
- Onderzoekers verkrijgen gegevens over de ontwikkeling van kippenembryo's
- Onderzoek toont aan dat commerciële oogst van brekende schildpadden leidt tot bevolkingsafname
- Hoe het Curiosity-project werkt
- Welke organen maken het vaatstelsel op?
- Timing van migratie verandert voor zangvogels aan de Pacifische kust
- Elektronen versterken de calorische koeling in vaste toestand in hexagonale sulfiden

- Video:Hoe de houdbaarheidsdatum van medicijnen werkt

- Wetenschappers ontwerpen moleculair systeem voor kunstmatige fotosynthese
- Ideeën voor schoolreizen voor de middelbare school Scheikunde

- (Re)generatie volgende:nieuwe strategie om steigers te ontwikkelen voor regeneratie van gewrichtsweefsel

 Auto-audiosystemen vormen een groter gevaar dan sms'en, pot
Auto-audiosystemen vormen een groter gevaar dan sms'en, pot Top 10 milieuvriendelijke vervangers voor plastic
Top 10 milieuvriendelijke vervangers voor plastic  Wetenschapper kijkt naar AI, lenzen om massa's vrij zwevende planeten te vinden
Wetenschapper kijkt naar AI, lenzen om massa's vrij zwevende planeten te vinden Vijf niveaus van de biosfeer
Vijf niveaus van de biosfeer Bewijs gevonden van vroege jager-verzamelaars die een hele giftige slang aten
Bewijs gevonden van vroege jager-verzamelaars die een hele giftige slang aten Onderscheid maken tussen leerlingen die raden en degenen die het weten
Onderscheid maken tussen leerlingen die raden en degenen die het weten Onzichtbare barrière doorbraak een zegen voor elektronica, kunstwerken en meer
Onzichtbare barrière doorbraak een zegen voor elektronica, kunstwerken en meer Historische metingen van de zee-oppervlaktetemperatuur corrigeren
Historische metingen van de zee-oppervlaktetemperatuur corrigeren
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

