
Wetenschap
Bacterieel eiwit kan helpen bij het vinden van materialen voor je volgende smartphone
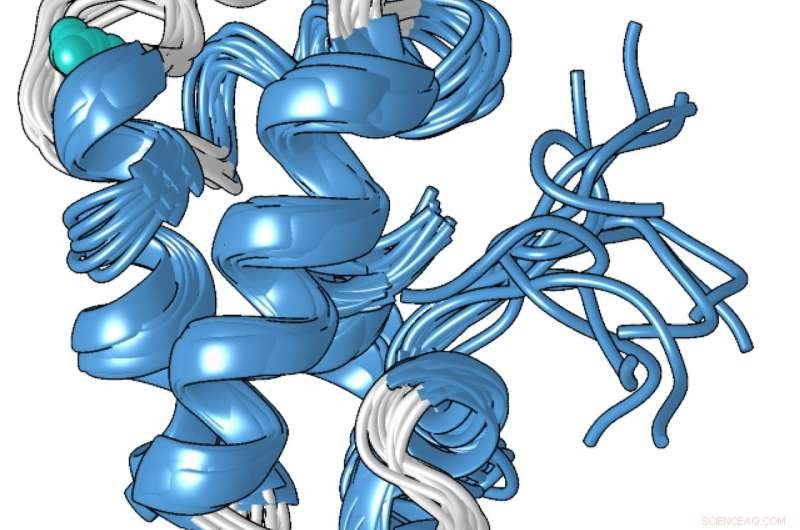
Een structureel model van de compacte metaalgebonden vorm van het lanmoduline-eiwit, dat 100 miljoen keer beter bindt aan lanthaniden - de zeldzame aardmetalen die worden gebruikt in smartphones en andere technologieën - dan aan andere metalen zoals calcium. Krediet:Penn State
Een nieuw ontdekt eiwit kan helpen bij het opsporen, doelwit, en verzamel uit het milieu de zeldzame aardmetalen die in smartphones worden gebruikt. Twee nieuwe studies door onderzoekers van Penn State beschrijven het eiwit, dat 100 miljoen keer beter bindt aan lanthaniden - de zeldzame aardmetalen die worden gebruikt in smartphones en andere technologieën - dan aan andere metalen zoals calcium. De eerste studie, die verschijnt in de Tijdschrift van de American Chemical Society , beschrijft het eiwit, en het tweede papier, die online in het tijdschrift verschijnt Biochemie , beschrijft zijn unieke structuur, die waarschijnlijk een rol speelt in zijn opmerkelijke selectiviteit voor lanthaniden.
"Onlangs, er is veel belangstelling geweest voor het vergroten van de toegankelijkheid van zeldzame aardelementen zoals lanthaniden, die worden gebruikt in de schermen en elektronica van smartphones, batterijen van hybride auto's, lasers, en andere technologieën, " zei Joseph Cotruvo Jr., assistent-professor en Louis Martarano Professor in loopbaanontwikkeling in de chemie aan Penn State en auteur van beide studies. "Omdat de fysieke eigenschappen van zeldzame-aarde-elementen zo op elkaar lijken, het kan moeilijk zijn om er een in het bijzonder te targeten en te verzamelen. Begrijpen hoe dit eiwit lanthaniden bindt met zo'n ongelooflijk hoge selectiviteit, zou manieren kunnen onthullen om deze belangrijke metalen te detecteren en te richten."
Het onderzoeksteam ontdekte het eiwit, die ze lanmodulin noemden, binnen de bacterie Methylobacterium extorquens, die op plantenbladeren en in de bodem groeit en een belangrijke rol speelt in de manier waarop koolstof door de omgeving beweegt. De bacteriën hebben lanthaniden nodig voor de goede werking van sommige van hun enzymen, waaronder een die de bacteriën helpt om koolstof te verwerken, die nodig is voor zijn groei.
"Deze bacteriën hebben lanthaniden en andere metalen zoals calcium nodig om te groeien, " zei Cotruvo. "Ze hebben een manier nodig om elk metaal uit de omgeving te halen en ervoor te zorgen dat elk naar de juiste plaats in de cel gaat. Het lijkt erop dat deze bacteriën een unieke manier hebben ontwikkeld om lanthaniden in het milieu aan te pakken, waar ze veel minder overvloedig zijn dan andere metalen zoals calcium."
De unieke structuur van het eiwit, die Cotruvo in samenwerking met het laboratorium van Scott Showalter heeft vastgesteld, universitair hoofddocent scheikunde aan Penn State, kan verklaren waarom het 100 miljoen keer beter is in het binden van lanthaniden dan calcium. Bij afwezigheid van metaal, Cotruvo legde uit, het eiwit is meestal ongestructureerd, maar wanneer metaal aanwezig is, het verandert de conformatie in een compact, goed gedefinieerde structuur.
De nieuwe compacte vorm bevat vier structuren die "EF-handen" worden genoemd. Menselijke cellen bevatten veel eiwitten met EF-handen, die betrokken zijn bij het gebruik van calcium voor functies zoals het afvuren van neuronen en het samentrekken van spieren. Deze eiwitten binden ook lanthaniden, hoewel lanthaniden fysiologisch niet relevant zijn bij mensen en de eiwitten slechts 10 of 100 keer meer kans hebben om lanthaniden te binden dan dat ze calcium binden. De compacte structuur van het lanmodulin-eiwit bevat ook een aminozuur genaamd proline op een unieke positie in elk van de EF-handen, die kunnen bijdragen aan de lanthanideselectiviteit van het eiwit.
"Het mechanisme van de selectiviteit van lanmodulin voor lanthaniden is nog niet duidelijk, maar we denken dat het neerkomt op de structurele verandering die optreedt in de aanwezigheid van metalen, " zei Cotruvo. "Deze structurele verandering is belangrijk voor de functie van het eiwit; bijvoorbeeld, sommige eiwit-eiwit-interacties kunnen alleen plaatsvinden als het eiwit in zijn compacte vorm is. Er is een zeer kleine hoeveelheid lanthaniden nodig om de conformatieverandering te induceren, maar het zou veel meer calcium vergen, meer dan de bacteriën kunnen hebben, om de verandering daadwerkelijk teweeg te brengen. Dit zou helpen om selectiviteit voor lanthaniden in cellen te garanderen."
Begrijpen hoe het eiwit zo selectief is, kan inzichten verschaffen voor het verzamelen van lanthaniden voor industriële doeleinden, inclusief winning uit mijnafvalstromen.
"Het is een uitdaging om deze stromen te verwerken om de zeldzame aardelementen op een economische manier van andere metalen te scheiden, " zei Cotruvo, "zowel vanwege de geringe hoeveelheid zeldzame aardmetalen en hun onoplosbaarheid, die grote hoeveelheden zuur nodig hebben om ze in oplossing te houden. Het verlagen van de pH verlaagt typisch de affiniteit voor metalen, maar we denken dat dit eiwit begint met zo'n hoge affiniteit dat het deze uitdagingen kan helpen overwinnen. We onderzoeken momenteel deze mogelijkheid."
Naast het onderzoeken van het selectiviteitsmechanisme van het eiwit en de functie van de uniek gelokaliseerde aminozuren, het onderzoeksteam onderzoekt ook de affiniteit van het eiwit voor andere metalen, omdat lanthaniden vaak worden aangetroffen in de aanwezigheid van andere metalen, inclusief ijzer, mangaan, en aluminium, die in grotere hoeveelheden voorkomen.
"We zijn ook erg geïnteresseerd in de biologische functie van het eiwit, " zei Cotruvo. "Maar uiteindelijk hopen we dat het begrijpen van het eiwit zal leiden tot milieuvriendelijkere manieren om zeldzame aardmetalen uit het milieu te halen."
 Een oplossing aandrijven:professor neemt de leiding over het verbeteren van de veiligheid van lithium-ionbatterijen
Een oplossing aandrijven:professor neemt de leiding over het verbeteren van de veiligheid van lithium-ionbatterijen LED-ing the way:een schone en handige methode om kunststof oppervlakken voor de industrie te oxideren
LED-ing the way:een schone en handige methode om kunststof oppervlakken voor de industrie te oxideren Team werpt nieuw licht op fotosynthese
Team werpt nieuw licht op fotosynthese Onderzoekers ontwikkelen eenvoudige methode om melkproducten in 3D te printen
Onderzoekers ontwikkelen eenvoudige methode om melkproducten in 3D te printen Wat is de chemische MDI?
Wat is de chemische MDI?
 Onderzoekers werken eraan om Biscayne Bay terug te brengen van de rand
Onderzoekers werken eraan om Biscayne Bay terug te brengen van de rand Video:Grondwater in kaart brengen vanuit de lucht
Video:Grondwater in kaart brengen vanuit de lucht Twee vitale buffers tegen klimaatverandering liggen net voor de kust
Twee vitale buffers tegen klimaatverandering liggen net voor de kust Wetenschapsupdate over klimaatverandering:van kwaad tot erger
Wetenschapsupdate over klimaatverandering:van kwaad tot erger Opinie:Brazilië moet zijn overgebleven ongecontacteerde inheemse Amazones beschermen
Opinie:Brazilië moet zijn overgebleven ongecontacteerde inheemse Amazones beschermen
Hoofdlijnen
- Wetenschappers onderzoeken de gevolgen voor de nationale veiligheid van genbewerking
- Onderzoek onthult hoe cellen zich herbouwen na mitose
- De Saguaro Cactus is een iconisch symbool van het Amerikaanse zuidwesten
- Hoe hoog kan een boom worden?
- Kraaien en keapapegaaien blijken het nut van objecten te leren, vergelijkbaar met de manier waarop menselijke baby's het doen
- Wat zijn de functies van glazen schuif- en afdekglaasjes?
- Wetenschappers maken cellen die de tastzin mogelijk maken
- Maak kennis met Cheddar Man:Your New Stone Age Crush
- Elk levend wezen maakt deel uit van een ecosysteem. Hier is hoe ze werken
- Vloeistof-vloeistofovergangen kristalliseren nieuwe ideeën voor moleculaire vloeistoffen

- Ontwerpen van selectieve reacties om biologische processen te moduleren

- Wetenschappers leggen de momenten van ontluikende kristalvorming en groei vast

- Verbetering van de kristalgroei met behulp van polyelektrolytoplossingen en afschuifstroming
- Nanodiamanten als fotokatalysatoren

 Poll vindt brede steun voor landarbeiders die door pandemie werken
Poll vindt brede steun voor landarbeiders die door pandemie werken Nanodraadlens kan zijn beeldvormende eigenschappen herconfigureren
Nanodraadlens kan zijn beeldvormende eigenschappen herconfigureren Dieren die in het tropische woud leven en die omnivoren zijn
Dieren die in het tropische woud leven en die omnivoren zijn Hervorming van energiesubsidies in het Midden-Oosten werkt op patronage gebaseerd autocratisch bestuur bij
Hervorming van energiesubsidies in het Midden-Oosten werkt op patronage gebaseerd autocratisch bestuur bij Wat is een stormvloedkering en waarom is het zo gevaarlijk?
Wat is een stormvloedkering en waarom is het zo gevaarlijk? Controleren microben de vorming van gigantische koperafzettingen?
Controleren microben de vorming van gigantische koperafzettingen? Onderzoekers ontwikkelen biologisch afbreekbaar geprint display
Onderzoekers ontwikkelen biologisch afbreekbaar geprint display Van deepfakes tot nepnieuws, een scala aan invloeden is bedoeld om kiezersbeslissingen vorm te geven
Van deepfakes tot nepnieuws, een scala aan invloeden is bedoeld om kiezersbeslissingen vorm te geven
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

