
Wetenschap
Moleculair viroloog bestrijdt griep op moleculair niveau
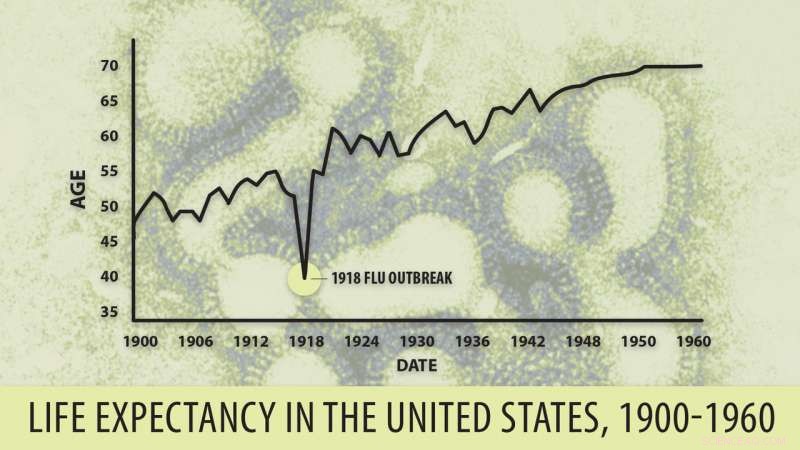
1918 "Spaanse" griep Krediet:UAB
Moleculair viroloog Chad Petit, doctoraat, gebruikt basiswetenschap om griep te bestrijden - door middel van experimenten op atomair niveau.
Dit omvat een dodelijk pluimvee-influenzavirus in China, het H7N9-vogelgriepvirus. Sinds 2013, H7N9 heeft 1 geïnfecteerd 625 mensen, doden 623. Hoewel niet erg besmettelijk voor mensen, slechts drie mutaties kunnen dat veranderen, H7N9 veranderen in de gevreesde ziekte X, de term die gezondheidsexperts gebruiken voor de volgende onbekende oorzaak van een wereldwijde epidemie.
In onderzoek om grieptherapieën tegen H7N9 en andere griepstammen te verbeteren, Petit en zijn collega's van de Universiteit van Alabama in Birmingham hebben de bindingsplaats en het remmingsmechanisme gedetailleerd beschreven voor twee experimentele remmers van influenzavirussen met kleine moleculen. Hun rapport is gepubliceerd in de Tijdschrift voor biologische chemie .
De twee experimentele remmers die door Petit zijn bestudeerd, een UAB-assistent-professor biochemie en moleculaire genetica, zijn kleine moleculen waarvan het precieze werkingsmechanisme onbekend was. De remmers richten zich op de functie van een belangrijk influenza-eiwit genaamd NS1, die meerdere rollen heeft om de immuunrespons van het lichaam tijdens influenza-infectie te blokkeren. Dus, NS1 is essentieel voor de overleving en het aanpassingsvermogen van het griepvirus.
Petit en collega's gebruikten nucleaire magnetische resonantie, of NMR, spectroscopie om interacties van de remmers met NS1 te onderzoeken. Ze toonden eerst aan dat de remmers - A9 en A22 genaamd - een interactie aangingen met slechts een van de twee onafhankelijk gevouwen domeinen van NS1, het NS1-effectordomein.
De onderzoekers merkten op dat de structuren van beide kleine-molecuul-remmers erg leken op een fragment van een gastheereiwit genaamd CPSF30 dat het NS1-effectordomein bindt om de immuunrespons van het lichaam te kortsluiten. Daarom, de onderzoekers veronderstelden dat A9 en A22 de virale replicatie van influenza blokkeren en de NS1-functie blokkeren door de interactie tussen het NS1-effectordomein en CPSF30 te verstoren.
NMR-gegevens onthulden de specifieke aminozuren van het NS1-effectordomein die betrokken zijn bij binding van remmers. De onderzoekers gebruikten twee significant verschillende NS1-eiwitten van verschillende influenzastammen, waaronder de H7N9-stam - toonde aan dat vergelijkbare sequenties van aminozuren in de twee NS1-eiwitten betrokken waren bij de binding van remmers.
Het 1918 "Spaanse" griep NS1-eiwit
Naast de Chinese H7N9 NS1 het andere geteste NS1-eiwit was het NS1-effectordomein van de "Spaanse" griep van 1918, die een eeuw geleden een derde van de wereldbevolking infecteerde en 50 miljoen tot 100 miljoen mensen doodde.
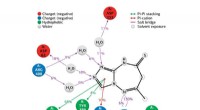
De UAB-onderzoekers gebruikten vervolgens röntgenkristallografie, onder leiding van UAB Microbiologie assistent-professor Todd Green, doctoraat, om de driedimensionale structuur van het NS1-effectordomein van de "Spaanse" griep van 1918 te bepalen. Hierdoor konden ze de A9/A22-bindingsplaats op die structuur in kaart brengen, die hun hypothese bevestigden:A9 en A22 interageren met de hydrofobe pocket van het NS1-effectordomein waarvan bekend is dat deze bindt aan het gastheereiwit CPSF30.
De kristallografiegegevens toonden ook aan dat het NS1-effectordomein kan dimeriseren, gebruikmakend van een interface die verschilt van twee andere bekende dimeren van het NS1-effectordomein. De biologische betekenis van deze nieuwe dimeervorm is onbekend.
"Allemaal samen, onze bevindingen leveren sterk bewijs voor het werkingsmechanisme van twee anti-influenzaverbindingen die zich richten op NS1, en de bevindingen dragen bij aan significante structurele inzichten in NS1 waarvan we hopen dat ze de ontwikkeling en optimalisatie van grieptherapieën op basis van A9 en A22 zullen bevorderen en informeren, ' zei Petit.
De behoefte aan nieuwe antivirale verbindingen is groot. Elk jaar, griepstammen doden 250, 000 tot 500, 000 mensen wereldwijd, en het virus staat bekend om snelle veranderingen om pandemische stammen te produceren waar maar weinig mensen immuniteit tegen hebben. Virale resistentie heeft de effectiviteit beperkt van verschillende eerdere antivirale verbindingen die werden ontwikkeld om griep te behandelen.
 Ontdekkingsreiziger Amundsens-schip keert na 100 jaar terug naar Noorwegen
Ontdekkingsreiziger Amundsens-schip keert na 100 jaar terug naar Noorwegen Satellieten laten zien dat orkaan Gert wordt getroffen door windschering
Satellieten laten zien dat orkaan Gert wordt getroffen door windschering Veranderende variabele in vergelijking die wordt gebruikt om klimaatverandering te projecteren om een nauwkeurigere schatting van neerslagveranderingen te geven
Veranderende variabele in vergelijking die wordt gebruikt om klimaatverandering te projecteren om een nauwkeurigere schatting van neerslagveranderingen te geven Britse temperatuurrecords tuimelden in 2019
Britse temperatuurrecords tuimelden in 2019 De onderwaterwereld van het rif van Belizes redden
De onderwaterwereld van het rif van Belizes redden
Hoofdlijnen
- Hoe CIPA werkt
- Transformatie, transductie en vervoeging: gentransfer in Prokaryotes
- Hoe beïnvloedt fosforylering de eiwitactiviteit?
- Wat zijn voorbeelden van homozygote dominanten?
- Het leven van een albatros:individualiteit aanpakken in populatiestudies
- Onderzoek creëert een manier om varkens te beschermen tegen PRRS tijdens de voortplanting
- Verdringing in de huid:stamcellen voelen buurtdichtheid om beslissingen te nemen
- Kan een Vision Board uw toekomst echt beïnvloeden?
- Wat zit er in je tarwe? Wetenschappers voegen het genoom van de meest voorkomende broodtarwe samen
- Chemicus synthetiseert nieuwe verbindingen met sterke antidiabetische eigenschappen
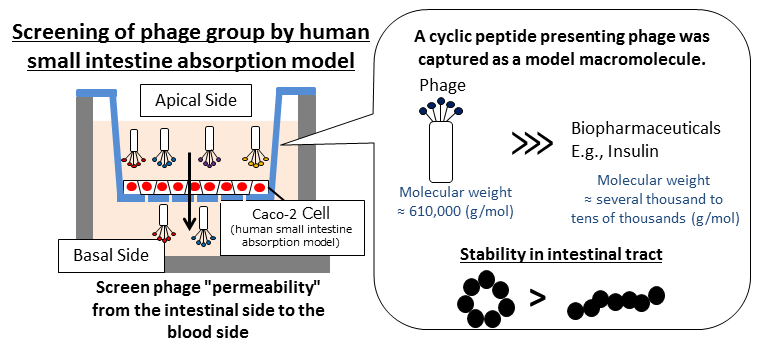
- Doorlatende peptiden in de dunne darm vergemakkelijken de opname van het spijsverteringskanaal
- Nieuw onderzoek onthult potentieel voor systemen van synthetische materialen die hun grootte kunnen tellen en voelen
- Detectie van meerdere sepsis-biomarkers uit volbloed - snel gemaakt, nauwkeurig, en goedkoop

- Gas onder druk zetten

 Na COVID-19:herijking van het Amerikaanse onderwijssysteem
Na COVID-19:herijking van het Amerikaanse onderwijssysteem Steden en gemeenschappen in de VS verliezen 36 miljoen bomen per jaar
Steden en gemeenschappen in de VS verliezen 36 miljoen bomen per jaar Near-Earth asteroïden spectroscopisch onderzoek bij de Isaac Newton-telescoop
Near-Earth asteroïden spectroscopisch onderzoek bij de Isaac Newton-telescoop Onderzoekers kijken met een frisse blik naar de Michaelis-Menten-vergelijking
Onderzoekers kijken met een frisse blik naar de Michaelis-Menten-vergelijking Hoe beschermen zeeschildpadden zich?
Hoe beschermen zeeschildpadden zich?  Ons onderzoek bracht twijfelachtige onderzoekspraktijken van ecologen en biologen aan het licht - dit is wat dat betekent
Ons onderzoek bracht twijfelachtige onderzoekspraktijken van ecologen en biologen aan het licht - dit is wat dat betekent Wie zoomt wie? Hoe de coronaviruscrisis eindelijk het sociale in sociale media brengt
Wie zoomt wie? Hoe de coronaviruscrisis eindelijk het sociale in sociale media brengt Is het verwrongen mysterie van snelle radio-uitbarstingen opgelost?
Is het verwrongen mysterie van snelle radio-uitbarstingen opgelost?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

