
Wetenschap
Onderzoekers kijken met een frisse blik naar de Michaelis-Menten-vergelijking

Magnus Kjærgaard (links) en Mateusz Dyla dagen een van de hoekstenen van de biochemie uit, de Michaelis-Menten-vergelijking omdat ze laten zien dat veel enzymen in signaalroutes onafhankelijk zijn van de substraatconcentratie, omdat het substraat fysiek verbonden is met het enzym. Krediet:Mateusz Dyla
Onderzoekers van de Universiteit van Aarhus dagen een van de hoekstenen van de biochemie uit, de Michaelis-Menten-vergelijking. Ze laten zien dat veel enzymen in signaalroutes onafhankelijk zijn van de substraatconcentratie, omdat het substraat fysiek verbonden is met het enzym. Met deze resultaten, misschien is het ooit mogelijk om medicijnen te ontwikkelen die niet alleen gericht zijn op het enzym, maar ook van invloed op hoe het is verbonden met zijn substraat.
Cellen sturen signalen door enzymcascades, waarbij het ene enzym het signaal doorgeeft aan het volgende. In dergelijke cascades, het is cruciaal dat het enzym de juiste substraten herkent om ervoor te zorgen dat, bijvoorbeeld, een hormoon activeert de juiste cellulaire activiteiten. Eiwitkinasen, de enzymen in dergelijke cascades, zijn op zichzelf meestal niet specifiek genoeg, en daarom vertrouwen ze op andere eiwitten om ze fysiek te verbinden met de juiste substraten.
"Momenteel, we beschrijven signaalenzymen met vergelijkingen die zijn ontwikkeld voor metabole enzymen, Magnus Kjærgaard legt uit. "Metabolische enzymen die energie maken voor ons lichaam, bijvoorbeeld, veel substraten per minuut moeten verwerken. In tegenstelling tot, signaalenzymen werken als schakelaars, en hoeft vaak maar één substraat om te zetten om effect te hebben. Daarom, de vergelijkingen die zijn ontwikkeld om metabole enzymen te beschrijven, zijn minder relevant voor signaalenzymen."
Al meer dan honderd jaar, biochemici hebben de activiteit van enzymen beschreven met behulp van de Michaelis-Menten-vergelijking, die beschrijft hoe de activiteit toeneemt met een verhoogde substraatvergelijking. Wanneer het enzym is verbonden met zijn substraat, het maakt niet uit hoeveel substraat er aanwezig is. In plaats daarvan, de snelheid van de reactie hangt af van hoe het enzym is verbonden met het substraat en dus met het connectormolecuul. Tot nu, we hebben geen enkele beschrijving gehad van hoe de structuur van dergelijke moleculen enzymatische reacties beïnvloedde.
"Normaal gesproken, de vraag die u probeert te beantwoorden, is welke grafiekvorm de enzymactiviteit beschrijft. We hadden een veel fundamenteler probleem, " zegt eerste auteur Mateusz Dyla. "Wat moeten we op de X-as zetten in plaats van concentratie?"
Connectormoleculen regelen cellulaire signalering
De auteurs maakten een modelsysteem waarmee ze de verbinding tussen het enzym en het substraat konden veranderen. Ze gebruikten dit om te meten hoe de lengte van een flexibele connector de eerste katalyseronde door het enzym beïnvloedt. die in milliseconden plaatsvond. Eindelijk, ze kwamen uit op een vergelijking die beschrijft hoe de snelheid van het enzym afhangt van de verbinding tussen enzym en substraat. Deze vergelijking suggereerde dat connectormoleculen een over het hoofd geziene rol spelen bij het beheersen van cellulaire signalering.
De verbinding tussen enzym en substraat is ook van invloed op welke substraten het enzym de voorkeur geeft. Substraten die er hetzelfde uitzien, kunnen heel verschillend zijn wanneer het enzym slechts één verbonden substraat verwerkt.
"Het is als het verschil tussen hoe lang ik erover doe om een enkele hotdog te eten, en hoeveel hotdogs ik in een hele week kan eten, " legt Magnus uit. "In de loop van een week, Ik zal worden beperkt door hoe snel ik de hotdogs kan verteren. Dit is niet relevant voor de tijd die nodig is om de eerste hotdog te eten. Daarom, de twee soorten metingen geven verschillende resultaten. Als je kinase-switches wilt begrijpen, je moet je concentreren op de eerste katalyseronde."
Op de lange termijn, dit kan gevolgen hebben voor de ontwikkeling van geneesmiddelen die gericht zijn op kinasen in, bijvoorbeeld, kanker. Mateusz legt uit:"We hopen dat het op een dag mogelijk zal zijn om medicijnen te maken die niet alleen gericht zijn op het enzym, maar richt zich ook op hoe het is verbonden met zijn substraat."
De resultaten zijn gepubliceerd in het internationale tijdschrift PNAS .
 Knipperend licht verandert bacteriën in chemische fabrieken
Knipperend licht verandert bacteriën in chemische fabrieken Gebruik witte azijn en isopropylalcohol
Gebruik witte azijn en isopropylalcohol Kan kunstmatige intelligentie nieuwe deuren openen voor het ontdekken van materialen?
Kan kunstmatige intelligentie nieuwe deuren openen voor het ontdekken van materialen? Video:Kan Google u helpen de vlekken te verwijderen?
Video:Kan Google u helpen de vlekken te verwijderen? Bepaling van de kristalstructuur van een DNA-gestabiliseerd zilveren nanocluster
Bepaling van de kristalstructuur van een DNA-gestabiliseerd zilveren nanocluster
 Parels van wijsheid:Japanse gekweekte boerderijen glinsteren nog steeds
Parels van wijsheid:Japanse gekweekte boerderijen glinsteren nog steeds Onderzoekers ontdekken nieuw sedimentarchief voor historisch klimaatonderzoek
Onderzoekers ontdekken nieuw sedimentarchief voor historisch klimaatonderzoek Het functioneren van terrestrische ecosystemen wordt bepaald door drie hoofdfactoren:
Het functioneren van terrestrische ecosystemen wordt bepaald door drie hoofdfactoren: VK krijgt steeds meer kans op +40C-temperaturen:studie
VK krijgt steeds meer kans op +40C-temperaturen:studie Studie vordert het begrijpen van de verhalen van het oude klimaat verteld door kleine schelpen
Studie vordert het begrijpen van de verhalen van het oude klimaat verteld door kleine schelpen
Hoofdlijnen
- Soorten menselijke schedelvormen
- Monster ontdekt in het Canadese Noordpoolgebied
- Wat zou er gebeuren als een cel geen Golgi-lichamen had?
- Wetenschappers volgen haaien die DNA-fragmenten uit de zee plukken
- Wetenschappers creëren op verzoek endocytose door cellen warm te bedraden
- Studie identificeert nieuwe malariaparasieten in wilde bonobo's
- Wat gebeurt er met een cel als deze geen DNA-chromosomen kopieert voordat deze zich deelt?
- Commensalisme: definitie, types, feiten en voorbeelden
- Hoe een tRNA-sequentie uit een DNA-sequentie te krijgen
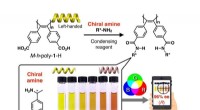
- Kleurcodering moleculaire spiegelbeelden
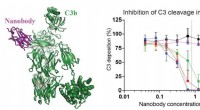
- Een klein eiwit met veel toepassingen
- Onderzoekers onthullen nieuwe inzichten in synthetische gencircuits

- sneller, groenere manier om koolstofbollen te produceren

- Model voor machinaal leren helpt bij het karakteriseren van verbindingen voor het ontdekken van geneesmiddelen

 Amerikaanse FTC onderzoekt Facebook-gegevensschandaal:media
Amerikaanse FTC onderzoekt Facebook-gegevensschandaal:media Hoe de concentratie van ionen in een 0,010 waterige oplossing van zwavelzuur
Hoe de concentratie van ionen in een 0,010 waterige oplossing van zwavelzuur De grootste Ichthyosaurus was een zwangere moeder, zeggen paleontologen
De grootste Ichthyosaurus was een zwangere moeder, zeggen paleontologen De nadelen van het gebruik van Gasohol als alternatieve brandstofbron voor benzine
De nadelen van het gebruik van Gasohol als alternatieve brandstofbron voor benzine  Algoritmen hebben de menselijke besluitvorming al overgenomen
Algoritmen hebben de menselijke besluitvorming al overgenomen Hoe slapen schildpadden?
Hoe slapen schildpadden?  Topologische isolatoren - één glimp is genoeg
Topologische isolatoren - één glimp is genoeg Chirurgische wegwerpmaskers die het beste zijn om duidelijk te worden gehoord tijdens het spreken, studie vondsten
Chirurgische wegwerpmaskers die het beste zijn om duidelijk te worden gehoord tijdens het spreken, studie vondsten
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | German | Dutch | Danish | Norway | Swedish |

-
Wetenschap © https://nl.scienceaq.com

