
Wetenschap
Een nieuw verband tussen glucose- en lipidenregulatie in het kankermetabolisme
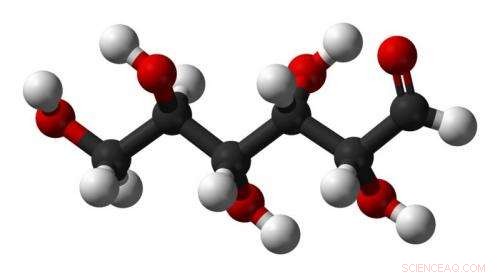
Glucose C6H12O6. Krediet:Wikipedia.
Onderzoekers van het Albert Einstein College of Medicine en de Shanghai Jiao Tong University School of Medicine in China hebben een enzym geïdentificeerd dat kankercellen helpt de bouwmaterialen te maken die ze nodig hebben om zich snel te vermenigvuldigen. Het remmen van dit enzym kan een strategie zijn om de groei van kanker te vertragen, leiden tot effectievere behandelingen. De studie werd gepubliceerd in het nummer van 27 april van de Tijdschrift voor biologische chemie .
Terwijl gezonde menselijke cellen de meeste vetzuren en cholesterol krijgen die ze nodig hebben om hun celmembranen op te bouwen uit de bloedbaan, kankercellen kunnen niet wachten tot hun bouwstoffen via deze route worden afgeleverd. In plaats daarvan, kankercellen verhogen vaak de activiteit van de enzymen die betrokken zijn bij het synthetiseren van lipiden in de cel.
Een van deze families van enzymen zijn de sterolregulerende elementen bindende eiwitten, of SREBP's. SREBP's reizen naar celkernen en zetten genen aan die betrokken zijn bij de productie van lipiden, meestal als reactie op specifieke signalen. In sommige kankercellijnen, waaronder bepaalde lever, colon- en borstkanker, een bepaalde SREBP genaamd SREBP1a is overactief.
Fajun Yang, een universitair hoofddocent ontwikkelings- en moleculaire biologie aan Albert Einstein, bestudeert precies hoe kankercellen zichzelf van lipiden voorzien. Het nieuw gepubliceerde onderzoek naar SREBP1a begon toen Xiaoping Zhao, de hoofdauteur van de nieuwe studie, was een postdoctoraal onderzoeker in Yang's lab, en ging verder als een samenwerking toen Zhao zijn eigen laboratorium begon aan de Shanghai Jiao Tong University.
In de nieuwe studie het team ontdekte dat SREBP1a overactief kon zijn in kankercellen dankzij een ander enzym, pyruvaatkinase M2 (PKM2). Het was toevallig ook bekend dat PKM2 betrokken is bij het voorzien van overtollige energie van hongerige kankercellen via een ander mechanisme:door een klein molecuul genaamd pyruvaat tijdens het glucosemetabolisme chemisch te modificeren. In de nieuwe studie de onderzoekers toonden aan dat PKM2 ook in staat was om SREBP1a te modificeren.
"Niemand had eerder gezegd dat deze man, PKM2, reguleert het lipidenmetabolisme, " zei Yang. "Dus eigenlijk zagen we dat dit een nieuwe verbinding is tussen een regulator van het glucosemetabolisme en een regulator van het lipidemetabolisme. In kankercellen, beide worden abnormaal geactiveerd."
Wanneer PKM2 en SREBP1a interageren, de SREBP1a wordt stabieler, bleek uit de studie. Hierdoor kan SREBP1a genen aanzetten die betrokken zijn bij lipidesynthese. Met behulp van een klein eiwit dat de interactie zou kunnen blokkeren, de auteurs waren in staat om de overtollige lipideproductie te stoppen en de groei van kankercellen te vertragen.
"De kankercel voelt als, 'Oh, Ik vast tot de dood!'" zei Yang. "De tumorcellen worden bijzonder gevoelig; ook al kunnen ze veel glucose opzuigen, ze kunnen de bouwstenen van het celmembraan niet maken. Indien gecombineerd met een ander medicijn, dan is dit een potentiële therapeutische benadering."
De aanpak is veelbelovend omdat het zich richt op eiwitten die niet sterk tot expressie worden gebracht in gezonde cellen. Als de groei van kankercellen zou kunnen worden vertraagd door deze weg te blokkeren, patiënten kunnen lagere doses nodig hebben van de giftige medicijnen die de kankercellen daadwerkelijk doden, en dus minder bijwerkingen ervaart.
 Enkele moleculen vastgelegd op video met een ongekende 1, 600 beelden per seconde
Enkele moleculen vastgelegd op video met een ongekende 1, 600 beelden per seconde Goedkoop, efficiënte en stabiele foto-elektrode kan de watersplitsing met zonne-energie verbeteren
Goedkoop, efficiënte en stabiele foto-elektrode kan de watersplitsing met zonne-energie verbeteren Peptide-hydrogels kunnen traumatisch hersenletsel helpen genezen
Peptide-hydrogels kunnen traumatisch hersenletsel helpen genezen Innovatieve combinatie van harde en zachte materialen verbetert de hechting op ruwe oppervlakken
Innovatieve combinatie van harde en zachte materialen verbetert de hechting op ruwe oppervlakken Superkritisch antwoord op afgewerkte olie gevonden
Superkritisch antwoord op afgewerkte olie gevonden
 Pijpleiding ontspoord, zo is de klimaatstrategie van Canada
Pijpleiding ontspoord, zo is de klimaatstrategie van Canada Waarom werden twee Egyptische mummies begraven met gouden tongen?
Waarom werden twee Egyptische mummies begraven met gouden tongen?  Zweedse onderzoekers stimuleren minder vliegen, met nieuwe tool om klimaatimpact onder de aandacht te brengen
Zweedse onderzoekers stimuleren minder vliegen, met nieuwe tool om klimaatimpact onder de aandacht te brengen Studie:eigenlijk potplanten verbeteren de luchtkwaliteit binnenshuis niet
Studie:eigenlijk potplanten verbeteren de luchtkwaliteit binnenshuis niet Ontdooiende permafrost zit vol ijsvormende deeltjes die in de atmosfeer kunnen komen
Ontdooiende permafrost zit vol ijsvormende deeltjes die in de atmosfeer kunnen komen
Hoofdlijnen
- Carnivoren weten dat het eten van andere karkassen van carnivoren ziekten overdraagt
- Afrikaanse pinguïns blijken samen te werken om vissen bijeen te jagen om te foerageren
- Waarom heeft de evolutie ons niet het vermogen gegeven om zoet water te ruiken?
- Wetenschappers brengen nieuwe inzichten in de erfelijkheid van de ernst van de hiv-infectie
- Genetische instructies van moeder bepalen het patroon voor embryonale ontwikkeling
- Het effect van temperatuur op celmembranen
- Diabetesmedicijn helpt bij het repareren van UV-beschadigd DNA in cellen van maankinderen
- Hoe een cel te splitsen in Two
- Hoe reproduceren algen zich?
- Chemische reacties voltooien

- Onderzoekers leggen in realtime rondzwervende moleculaire fragmenten vast

- Loodvrij, efficiënte perovskiet voor fotovoltaïsche cellen
- De ontwikkeling van laagdimensionale nanomaterialen kan een revolutie teweegbrengen in toekomstige technologieën
- Een kleur van poreuze materialen in- en uitschakelen met zuur

 Een breuk omzetten in een verhouding
Een breuk omzetten in een verhouding  Bevroren bellen viraal video-geïnspireerd onderzoek nu gepubliceerd
Bevroren bellen viraal video-geïnspireerd onderzoek nu gepubliceerd China bereidt missie voor om ruimtevaartuigen op de verre kant van de manen te laten landen
China bereidt missie voor om ruimtevaartuigen op de verre kant van de manen te laten landen ster licht, ster helder zoals uitgelegd door wiskunde
ster licht, ster helder zoals uitgelegd door wiskunde Basisrichtlijnen voor wachtwoorden kunnen de accountbeveiliging drastisch verbeteren, studie toont
Basisrichtlijnen voor wachtwoorden kunnen de accountbeveiliging drastisch verbeteren, studie toont Amazon investeert in elektrische auto-startup Rivian
Amazon investeert in elektrische auto-startup Rivian Ethanol stimuleert grootschalige uitbreiding van Braziliaanse landbouwgrond
Ethanol stimuleert grootschalige uitbreiding van Braziliaanse landbouwgrond Hoe zijn isotopen belangrijk bij het bestuderen van het menselijk lichaam?
Hoe zijn isotopen belangrijk bij het bestuderen van het menselijk lichaam?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

