
Wetenschap
Een klein eiwit met veel toepassingen
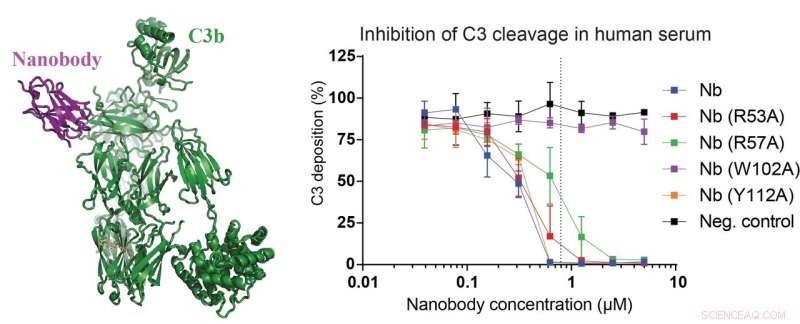
Het linkerpaneel van de figuur toont de structuur van het nieuw ontwikkelde nanolichaam (magenta) gebonden aan een C3-fragment genaamd C3b (groen). In de rechter panelen gegevens die aantonen dat het nanobody en de mutanten hiervan in staat zijn om de splitsing van C3 in 15 procent humaan serum te remmen. De onderzoekers construeerden ook een nanobody-mutant die het remmende effect op de C3-splitsing (paarse curve) volledig verliest, waardoor het een perfecte negatieve controle is. Krediet:Rasmus Kjeldsen Jensen en Janus Asbjørn Schatz-Jakobsen, Universiteit van Aarhus
Onderzoekers van de afdeling Moleculaire Biologie en Genetica en van de afdeling Biogeneeskunde van de Universiteit van Aarhus hebben samen een lama-antilichaam ontwikkeld en beschreven dat een significante impact kan hebben voor toekomstige diagnostiek en behandeling van, bijv. nier ziekten.
Het onderzoeksteam bestudeerde een eiwit genaamd C3 uit het deel van het aangeboren immuunsysteem dat bekend staat als het complementsysteem. Bij herkenning van pathogene organismen of stervende lichaamscellen, C3 wordt gesplitst door bloedenzymen als onderdeel van een afweermechanisme. Deze enzymen staan bekend als C3-convertasen, en de splitsing van C3 resulteert in twee fragmenten. Het fragment genaamd 3b bindt direct aan de pathogenen, terwijl het andere fragment immuuncellen rekruteert en stimuleert om het doelwit te elimineren.
Bij een gezond persoon cellen worden beschermd tegen de effecten van de C3-splitsing. Echter, als gevolg van mutaties in het DNA, deze bescherming kan verloren gaan, het risico op het ontwikkelen van chronische ontstekingsziekten of auto-immuunziekten verhogen. Voor een lange tijd, de onderzoekers hebben zich gericht op het ontwikkelen van middelen die dergelijke ongewenste complementactivering voorkomen. Om deze reden, ze ontwikkelden het lama-antilichaam om splitsing van C3 te voorkomen. Lama-antilichamen zijn ook bekend als nanobodies vanwege hun kleine formaat, en vergeleken met normale antilichamen, ze zijn gemakkelijk te ontwikkelen en aanzienlijk goedkoper te produceren.
"De technologie die wordt gebruikt om deze nanobodies te ontwikkelen en te produceren, is al meer dan twee decennia bekend, ", zegt Gregers Rom Andersen. "En daarom, het is enigszins verrassend dat we de eersten ter wereld zijn die een nanobody hebben ontwikkeld die het complementsysteem remt."
Door kristallen bloot te stellen aan röntgenstralen en de resultaten te correleren met gegevens uit elektronenmicroscopie, de onderzoekers hebben tot in detail beschreven hoe hun nanobody C3 bindt.
"De kristalstructuur van ons nanobody gebonden aan C3 ondersteunt onze eerder voorgestelde modellen die beschrijven hoe de complementconvertasen hun substraten herkennen en verklaart daarom duidelijk waarom ons nanobody zijn remmende effect uitoefent op de splitsing van C3. Onze resultaten verbeteren ook het basisbegrip van hoe dit essentieel mechanisme binnen het complementsysteem werkt. Door te vergelijken met eerder gepubliceerde eiwitstructuren, we kunnen bovendien verklaren waarom ons nanobody de vorming van de C3-convertasen remt, ons nanobody heeft als het ware een 'dubbel remmend' effect, " legt Rasmus Kjeldsen Jensen uit.
Naast het werk dat het C3-nanobodycomplex beschrijft, het onderzoeksteam heeft ook verschillende laboratoriumexperimenten uitgevoerd met serum van zowel muizen als mensen. Deze resultaten bevestigen de waarnemingen van de atomaire structuur en onthullen duidelijk dat hun nieuw ontwikkelde nanobody de splitsing van C3 in zowel menselijk als muizenserum remt. Dat laatste is belangrijk, omdat muizen vaak als ziektemodel worden gebruikt.
"Onze experimenten in serum zijn belangrijk omdat ze aantonen dat ons nanobody echt werkt onder fysiologische omstandigheden, waar het complementsysteem van nature zijn functie uitoefent. Deze resultaten geven aan dat ons nanobody kan worden gebruikt bij de behandeling van ziekten die worden veroorzaakt door overactivering van het complementsysteem. Als voorbeeld, een deel van de nier is niet in dezelfde mate beschermd tegen complement als andere weefsels, en in dit geval zou ons nanobody een kandidaat kunnen zijn om complementgestuurde ziekteprogressie te stoppen, ", zegt Gregers Rom Andersen. "Echter, we ontdekten ook dat ons nanobody in staat is om de beschermende effecten te remmen die ons eigen lichaam normaal gesproken heeft tegen complement, en men moet daarom zeer voorzichtig zijn en de mogelijke bijwerkingen van therapeutische behandeling van ziekten met behulp van ons nanobody nauwkeurig beoordelen, " besluit Gregers Rom Andersen.
De basis van dit werk werd gelegd door de twee assistent-hoogleraren Kasper Røjkjær Andersen en Nick Stub Laursen van de afdeling Moleculaire Biologie en Genetica, die de eersten in Denemarken waren die systematisch grootschalige nanobodies ontwikkelden en produceerden. Echter, de drijvende kracht in het project was promovendus Rasmus Kjeldsen Jensen onder supervisie van professor Gregers Rom Andersen, die bij de karakterisering van het nanobody werd bijgestaan door de twee promovendi Trine Amalie Fogh Gadeberg en Rasmus Pihl.
 Hoop op ontwikkeling van materialen voor 3D-displays en medische toepassingen
Hoop op ontwikkeling van materialen voor 3D-displays en medische toepassingen Waarom zijn overgangsmetalen goede katalysatoren?
Waarom zijn overgangsmetalen goede katalysatoren?  De eiwitten die de biosynthese van formicamycine behouden
De eiwitten die de biosynthese van formicamycine behouden Enzymen geschikt maken voor industriële toepassingen
Enzymen geschikt maken voor industriële toepassingen Onderzoekers gebruiken nieuwe tools van datawetenschap om afzonderlijke moleculen in actie vast te leggen
Onderzoekers gebruiken nieuwe tools van datawetenschap om afzonderlijke moleculen in actie vast te leggen
 Onderzoek naar platentektoniek herschrijft de geschiedenis van de continenten van de aarde
Onderzoek naar platentektoniek herschrijft de geschiedenis van de continenten van de aarde Branden woeden in Zuid-Europa, honderden gedwongen te evacueren
Branden woeden in Zuid-Europa, honderden gedwongen te evacueren Verschillende soorten alligators
Verschillende soorten alligators  Snipers om tot 10 te doden, 000 kamelen in het door droogte geteisterde Australië
Snipers om tot 10 te doden, 000 kamelen in het door droogte geteisterde Australië Onderzoeker ziet enorme koolstofput in bodemmineralen
Onderzoeker ziet enorme koolstofput in bodemmineralen
Hoofdlijnen
- Inleiding tot hoe gigantische virussen werken
- De functie van macromoleculen
- Draadtap op het dak is bedoeld om te leren waar kraaien over roddelen in de schemering
- Wie is je vader? De geschiedenis van vaderschapstesten
- Welke effecten kunnen glycolyse remmen?
- Eerste levensvormen op aarde onthuld in hete lente
- Het belang van samengestelde microscopen
- Hoe orchideeën werken
- Zeeslakken weten hoe ze hun huisvestingskosten moeten begroten
- Nieuwe 3D-printtechniek voor biomaterialen
- Van borstimplantaten tot ijsblokjesbakjes - hoe siliconen onze keukens overnamen

- Een nieuwe methode om goedkopere chemicaliën te maken

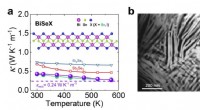
- Extreem lage thermische geleidbaarheid in 1-D zachte kettingstructuur
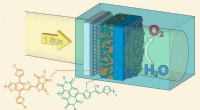
- Een kunstmatig blad gemaakt van halfgeleidende polymeren
 Wat is Ceramide?
Wat is Ceramide?  Een kleine opklapbare joystick brengt haptiek naar draagbare apparaten
Een kleine opklapbare joystick brengt haptiek naar draagbare apparaten UK's favoriete kerstsfeer onthuld met online zoekopdrachten
UK's favoriete kerstsfeer onthuld met online zoekopdrachten Kepler-telescoop dood na ontdekking van duizenden werelden
Kepler-telescoop dood na ontdekking van duizenden werelden Goedkope detector is als klittenband voor kankercellen
Goedkope detector is als klittenband voor kankercellen Hoe ratelslangenschubben hen helpen regenwater uit hun lichaam te zuigen
Hoe ratelslangenschubben hen helpen regenwater uit hun lichaam te zuigen Belangrijke ecosystemen van onderzeese canyons lopen gevaar
Belangrijke ecosystemen van onderzeese canyons lopen gevaar IJsbeerblogs onthullen gevaarlijke kloof tussen feiten en meningen over klimaatverandering
IJsbeerblogs onthullen gevaarlijke kloof tussen feiten en meningen over klimaatverandering
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

