
Wetenschap
Een bijna universele manier om enzymremming te meten
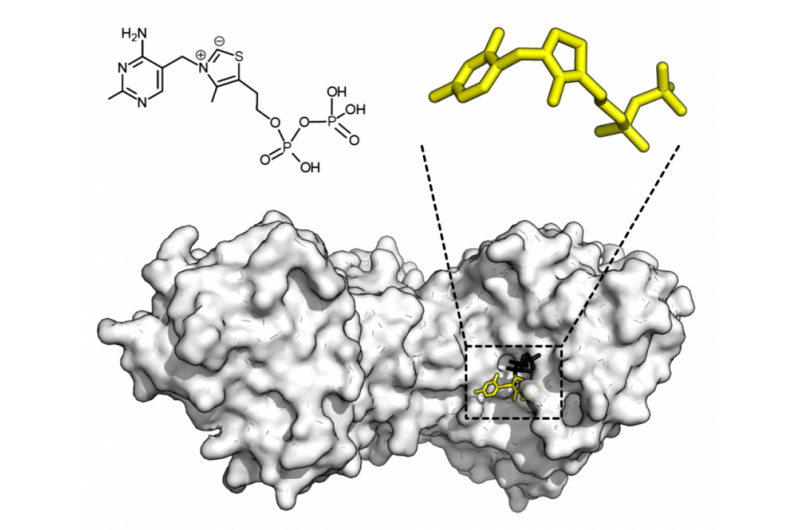
Chemische structuur voor thiaminepyrofosfaat en eiwitstructuur van transketolase. Thiamine pyrofosfaat cofactor in geel en xylulose 5-fosfaat substraat in zwart. Krediet:Thomas Shafee/Wikipedia
Onderzoekers van de McGill University hebben een nieuwe techniek uitgevonden om te meten hoe snel geneesmiddelen interageren met hun moleculaire doelwitten. De ontdekking biedt wetenschappers een nieuwe manier om de effectiviteit van kandidaat-geneesmiddelen te onderzoeken die anders over het hoofd zouden zijn gezien.
De nieuwe methode draait om het principe van enzymremming. Talloze geneesmiddelen, variërend van antibiotica tot medicijnen voor chemotherapie, werken door de werking van enzymen te blokkeren, en de zoektocht naar nieuwe enzymremmende stoffen blijft een belangrijk aandachtspunt bij de ontwikkeling van geneesmiddelen.
In een paper gepubliceerd in Natuurcommunicatie , het McGill-team, onder leiding van de scheikundeprofessoren Nicolas Moitessier en Anthony Mittermaier, demonstreren het gebruik van isothermische titratiecalorimetrie (ITC) om de warmte te meten die wordt gegenereerd door enzymactiviteit en daarmee de snelheden waarmee remmende stoffen die activiteit blokkeerden.
"Een belangrijk verschil tussen ITC en andere methoden is dat ITC de reactiesnelheid direct meet, " legt Mittermaier uit.
Bestaande methoden voor het meten van enzymactiviteit kijken indirect naar die activiteit, door veranderingen in concentratie veroorzaakt door enzymatische katalyse te meten als functie van de tijd. Deze metingen zijn vaak afhankelijk van speciale reagentia die van kleur of fluorescentie veranderen wanneer het enzym erop inwerkt, en vereisen dat een unieke test wordt ontwikkeld voor elk enzym dat wordt bestudeerd.
Omdat ITC de productie van warmte meet - een bijna universeel kenmerk van chemische reacties - kan het op zowat elk enzym worden toegepast.
"ITC komt zo dicht mogelijk bij een universele enzymtest, ', zegt Mittermaïer.
Naast zijn algemeenheid, de ITC-methode geeft een directe uitlezing van de enzymactiviteit omdat deze de warmtestroom in realtime detecteert. Door een direct venster op de reactie te geven, ITC biedt onderzoekers een beter inzicht in de mechanismen waarmee enzymremming verloopt. Het is meestal erg uitdagend, en soms bijna onmogelijk, om deze informatie uit conventionele testen te verkrijgen.
Het realtime karakter van ITC is bijzonder veelbelovend voor onderzoekers die covalente remmers onderzoeken. Deze sterk bindende moleculen hebben potentieel als langwerkende geneesmiddelen, maar waren eerder uit de gratie geraakt bij de ontwikkeling van geneesmiddelen vanwege bezorgdheid over de toxiciteit. Het inzicht dat ITC biedt in de relatie tussen de moleculaire structuur van een remmer en hoe deze reageert met zijn doelwit, zal de hernieuwde belangstelling voor covalente remmers ondersteunen en het werk vergemakkelijken om ze te ontwikkelen tot geneesmiddelen die zowel zeer effectief als veilig zijn.
 India's vuurwerkcentrum getroffen door anti-vervuilingsactie
India's vuurwerkcentrum getroffen door anti-vervuilingsactie Koolstofafvang kan het klimaatprobleem niet oplossen zonder individuele acties
Koolstofafvang kan het klimaatprobleem niet oplossen zonder individuele acties Uitbarsting van de Laacher See-vulkaan redated
Uitbarsting van de Laacher See-vulkaan redated Antarctische Mesoscale Prediction System-precipitatieproducten blijken betrouwbaar te zijn
Antarctische Mesoscale Prediction System-precipitatieproducten blijken betrouwbaar te zijn Onderzoekers zetten nieuwe technologie in om de diepten van de Golf van Mexico te verkennen
Onderzoekers zetten nieuwe technologie in om de diepten van de Golf van Mexico te verkennen
Hoofdlijnen
- Hoe jaloezie werkt
- Deze boom is het oudste levende organisme van Europa - een soort van,
- Verlichting aan het water verstoort de natuur in het omliggende ecosysteem drastisch
- De rol van enzymen bij cellulaire ademhaling
- Wat zijn de 10 Major Body Systems?
- Wat is er met androgyn gebeurd?
- Hoe beïnvloedt stress je hersens?
- Kunstmatige nesten zijn bedoeld om het broedsucces van de schuwe albatros te vergroten
- Combinatie van warmer water, blootstelling aan chemicaliën versterkt schadelijke effecten bij een kustvis
- Video:Wat doen rechercheurs op de plaats delict eigenlijk?

- Chemici gebruiken kunstmatige intelligentie om de toekomst (van chemische reacties) te voorspellen

- Kunnen we kanker genezen door uit te zoeken hoe twee eiwitten op elkaar inwerken?

- Onderzoekers maken in water afbreekbaar plastic dat zetmeel en cellulose combineert
- Virussen onderscheiden, vernietigen E. coli in drinkwater
 Energie in gevaar:de impact van klimaatverandering op aanbod en kosten
Energie in gevaar:de impact van klimaatverandering op aanbod en kosten Onderzoek geeft zekerheid dat de warmtestroom beheersbaar zal zijn in ITER
Onderzoek geeft zekerheid dat de warmtestroom beheersbaar zal zijn in ITER Aankondiging van kwartet draadloze oplaadproducten voor thuis, kantoor, auto
Aankondiging van kwartet draadloze oplaadproducten voor thuis, kantoor, auto Een 40-jarige katalysator onthult zijn geheimen
Een 40-jarige katalysator onthult zijn geheimen Luiheid leidde tot uitsterven van Homo erectus
Luiheid leidde tot uitsterven van Homo erectus De stoffige prehistorie van het zonnestelsel verkennen
De stoffige prehistorie van het zonnestelsel verkennen De meest vluchtige vulkaan van Indonesië barst opnieuw uit
De meest vluchtige vulkaan van Indonesië barst opnieuw uit Nieuw op AI gebaseerd videosysteem helpt senioren veilig en onafhankelijk te blijven
Nieuw op AI gebaseerd videosysteem helpt senioren veilig en onafhankelijk te blijven
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- Italian | Swedish | German | Dutch | Danish | Norway | French | Spanish | Portuguese |

-
Wetenschap © https://nl.scienceaq.com

