
Wetenschap
Nieuwe tool om grotendeels genegeerde risico's in de farmaceutische industrie te beoordelen
Onderzoekers van de Universiteit van Cardiff hebben een nieuwe methode ontwikkeld om de kans te testen dat een medicijn verandert in een potentieel schadelijke versie van zichzelf wanneer het het lichaam binnenkomt.
In samenwerking met Liverpool John Moores University en AstraZeneca, het team heeft een eenvoudige aanpak ontwikkeld om door grote databases van farmaceutische medicijnen te bladeren en het waarschijnlijke risico te beoordelen dat een medicijn racemisatie ondergaat - een proces waarbij een medicijn in een spiegelbeeld van zichzelf verandert en ofwel inert of potentieel gevaarlijk wordt.
Het is voor het eerst dat voor dit proces een kwantitatieve risicobeoordelingstool is ontwikkeld.
Hun nieuwe bevindingen publiceren in het toonaangevende scheikundetijdschrift Angewandte Chemie , het team is van mening dat de nieuwe methode mogelijk kan leiden tot een aanzienlijke vermindering van het financiële risico dat gepaard gaat met de ontwikkeling van geneesmiddelen door vroegtijdige kandidaat-geneesmiddelen in het productieproces te identificeren, uiteindelijk leidend tot de efficiënte ontwikkeling van veilige medicatie.
Geneesmiddelverbindingen bestaan vaak in een rechts- of linkshandige vorm, waarbij beide vormen een identieke chemische samenstelling hebben, maar een structuur die een niet-superponeerbaar spiegelbeeld van elkaar is. Deze verbindingen, bekend als enantiomeren, lijken veel op onze rechter- en linkerhand - ze hebben dezelfde structuur die elkaar volledig spiegelt, maar het is onmogelijk om de een perfect op de ander te passen met beide handpalmen naar boven gericht.
Geneesmiddelen kunnen zowel rechts- als linkse versies van een verbinding bevatten, maar vaak is slechts één van de enantiomeren van een medicijn verantwoordelijk voor de gewenste fysiologische effecten, terwijl de andere enantiomeer minder actief is, inactief, of kan soms nadelige effecten veroorzaken.
Het bekendste voorbeeld hiervan is het kalmerende middel thalidomide, die werd ontdekt door het Duitse bedrijf Chemie Grünenthal en van 1957 tot 1961 in een aantal landen over de hele wereld werd verkocht. Het werd uit de handel genomen toen bleek dat het de oorzaak was van geboorteafwijkingen. Eén enantiomeer veroorzaakte de gewenste kalmerende effecten, terwijl de andere, onvermijdelijk aanwezig, enantiomeer veroorzaakte de geboorteafwijkingen.
Sinds de thalidomidecrisis medicijnontwikkelaars hebben ernaar gestreefd om medicijnen te maken die slechts één enantiomeer bevatten.
Echter, het is mogelijk dat een enkele enantiomeer snel naar het spiegelbeeld van zichzelf kan veranderen wanneer het het lichaam binnenkomt, via een proces dat racemisatie wordt genoemd. Aangenomen wordt dat deze transformatie wordt veroorzaakt door de interactie van het medicijn met basische verbindingen in het water in het lichaam.
In hun studie hebben het team zette experimenten op waarin ze de chemische omstandigheden van het menselijk lichaam simuleerden en een aantal medicijnen in het systeem introduceerden, het volgen van de snelheid waarmee de verschillende geneesmiddelen racemisatie ondergingen. Met behulp van deze resultaten, ze waren in staat om een eenvoudig wiskundig model te genereren dat snel de snelheid van racemisatie in een geneesmiddel kon voorspellen, vervolgens aangeven hoe veilig en productief dat medicijn zou zijn als het zou worden toegediend.
Hoofdauteur van de studie Dr. Niek Buurma, van de School of Chemistry van de Universiteit van Cardiff, zei:"Na de ramp met thalidomide, onderzoekers over de hele wereld hebben zich gericht op het enantioselectief maken van verbindingen, dat wil zeggen met slechts één enantiomeer.
"Echter, terwijl verbindingen routinematig worden getest om er zeker van te zijn dat ze inherent stabiel zijn onder fysiologische omstandigheden, er is niet veel nagedacht over het voorkomen van configuratie-instabiliteit in de ontwerpfase, met behulp van geschikte voorspellende modellen."
"Wij zijn van mening dat deze risicobeoordeling het mogelijk zal maken om veiliger medicijnen te produceren door de farmaceutische industrie te helpen snel medicijnen te herkennen die tijdens de ontwikkeling zullen falen en hun inspanningen te concentreren op verbindingen die waarschijnlijker werken."
 Een nieuw begrip van eiwitbeweging
Een nieuw begrip van eiwitbeweging Heterofase nanostructuren die bijdragen aan efficiënte katalyse
Heterofase nanostructuren die bijdragen aan efficiënte katalyse Het licht zien:onderzoekers bieden oplossing voor efficiëntieprobleem van kunstmatige fotosynthese
Het licht zien:onderzoekers bieden oplossing voor efficiëntieprobleem van kunstmatige fotosynthese Zoekmachine voor slim hout
Zoekmachine voor slim hout Methode om microfluïdische elektrochemische technologieën toe te passen op redox-neutrale reacties met één elektronoverdracht
Methode om microfluïdische elektrochemische technologieën toe te passen op redox-neutrale reacties met één elektronoverdracht
 Snel smelten van 's werelds grootste ijsplaat gekoppeld aan zonnewarmte in de oceaan
Snel smelten van 's werelds grootste ijsplaat gekoppeld aan zonnewarmte in de oceaan Wat zijn de overtuigingen over de oorzaken van ziekte tijdens de Elizabethaanse periode?
Wat zijn de overtuigingen over de oorzaken van ziekte tijdens de Elizabethaanse periode?  Het belang van het broeikaseffect
Het belang van het broeikaseffect  Kosten van overstromingsverliezen in Maritimes kunnen tot 300 procent stijgen
Kosten van overstromingsverliezen in Maritimes kunnen tot 300 procent stijgen Hoe isoleer ik bacteriën van de bodem?
Hoe isoleer ik bacteriën van de bodem?
Hoofdlijnen
- Detectie van nieuwe eiwitten in actieve muizenhersenen
- Onderzoek biedt inzichten voor de bestrijding van verwoestende amfibieënziekte
- Hoe extremofielen werken
- Taxonomie (biologie): definitie, classificatie en voorbeelden
- Roept op tot einde aan Mexico's vangst van bedreigde bruinvis
- 5 waargebeurde verhalen over een bij de geboorte gescheiden tweeling
- Cavendish redden:team kweekt 's werelds eerste ziekteresistente bananen in Panama
- Amerikaanse eiken delen een gemeenschappelijke noordelijke voorouder
- Feiten over osmose voor kinderen
- In het moleculaire oog:vloeibare monsters in realtime onderzoeken
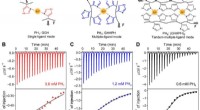
- Moleculaire engineering metaalcoördinatie-interacties voor sterke, moeilijk, snel herstellende hydrogels
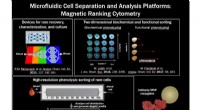
- Eencellige mRNA-cytometrie via sequentiespecifieke clustering en trapping van nanodeeltjes
- Legerwetenschappers ontdekken kracht in urine

- What Dissolves Oil?

 Dodelijke hartblokkades dwarsbomen met organische nanodeeltjes
Dodelijke hartblokkades dwarsbomen met organische nanodeeltjes Het knopen van halfmetalen in topologische elektrische circuits
Het knopen van halfmetalen in topologische elektrische circuits Moeders voelen druk van kookplicht
Moeders voelen druk van kookplicht Orkaandelta teistert Caribische kust van Mexico
Orkaandelta teistert Caribische kust van Mexico Ontbossing Amazone voor januari bereikt record
Ontbossing Amazone voor januari bereikt record Aardbeving biedt nieuwe kansen voor onderzoek, Directeur geologisch onderzoek Idaho zegt:
Aardbeving biedt nieuwe kansen voor onderzoek, Directeur geologisch onderzoek Idaho zegt: CERN splitst zich met wetenschapper over beledigende opmerkingen over vrouwen
CERN splitst zich met wetenschapper over beledigende opmerkingen over vrouwen Corrupte banden cultiveren in post-Mao China
Corrupte banden cultiveren in post-Mao China
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

