
Wetenschap
Goedkoop, energiezuinige en schone reactie om chemische grondstof te maken
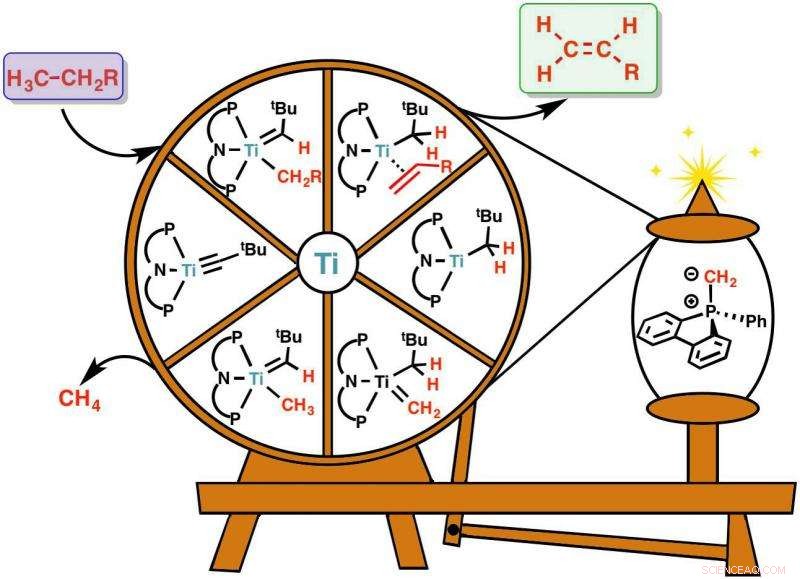
Weergave van de koolstof-waterstof breekreactie met een spindel. Olefinen, dat wil zeggen moleculen met een dubbele binding tussen koolstofatomen (C=C, groene doos) worden gegenereerd uit een niet-reactieve moleculen van aardgas (violette doos). De reactie omvat een zorgvuldig gekozen katalysator op basis van titanium (Ti), vertegenwoordigd door het wiel en een additief molecuul, afgebeeld op de spoel. Het additief helpt het wiel te draaien, om de katalysator terug te brengen naar zijn oorspronkelijke vorm, zodat het opnieuw kan worden gebruikt om een andere reactie te vergemakkelijken. Olefinen zijn de chemische grondstof voor een verscheidenheid aan andere chemicaliën, zoals plastic, geleidende polymeren, medicijnen, enz. Deze reactie kan bij lage temperaturen worden uitgevoerd en het is de eerste keer dat het goedkoop kan worden uitgevoerd. Krediet:Instituut voor Basiswetenschappen
Ze zijn overal om je heen! De meeste kunststoffen, geleidende polymeren, en zelfs medicijnen zijn afgeleid van moleculen met een dubbele binding tussen twee koolstofatomen, C=C. Deze moleculen worden olefinen genoemd en worden voornamelijk geproduceerd uit fossiele brandstoffen via een energie-intensief en vervuilend proces dat bekend staat als stoomkraken. Het vereist temperaturen van 800°C en produceert het broeikasgas koolstofdioxide. Onnodig vandaag, Er wordt veel gezocht naar alternatieven voor dit proces die milieu- en economische voordelen kunnen opleveren.
Een team van onderzoekers van het Center for Catalytic Hydrocarbon Functionalisaties, binnen het Instituut voor Basiswetenschappen (IBS), in samenwerking met Prof. Daniel J. Mindiola van de Universiteit van Pennsylvania, een reactie bewerkstelligd die voorheen niet mogelijk was; ze produceerden alkenen met goedkope, gemakkelijk verkrijgbare ingrediënten en bij lage temperatuur (75°C). Dit onderzoeksresultaat, gepubliceerd in Natuurchemie , maakt de weg vrij voor een efficiënt gebruik van aardgas om belangrijke chemische producten te synthetiseren.
Natuurlijke gassen, zoals methaan en ethaan, hebben sterke koolstof-waterstof (C-H) bindingen die moeilijk te verbreken zijn. Het onderzoeksteam slaagde erin om dergelijke niet-reactieve moleculen om te zetten in olefinen, de chemische grondstof van een groot aantal producten die we in ons dagelijks leven gebruiken.
Dit type olefineproductiemethode is gebaseerd op dehydrogenering, dat is de verwijdering van waterstofatomen die leidt tot de vorming van de C=C-binding, het kenmerk van olefinen. Omdat de energie die nodig is om de sterke C-H-bindingen te verbreken te hoog is, de reactie kan alleen worden bereikt met behulp van andere moleculen, katalysatoren genoemd. Eerder, dehydrogenering was alleen mogelijk met katalysatoren op basis van dure metalen, zoals iridium.
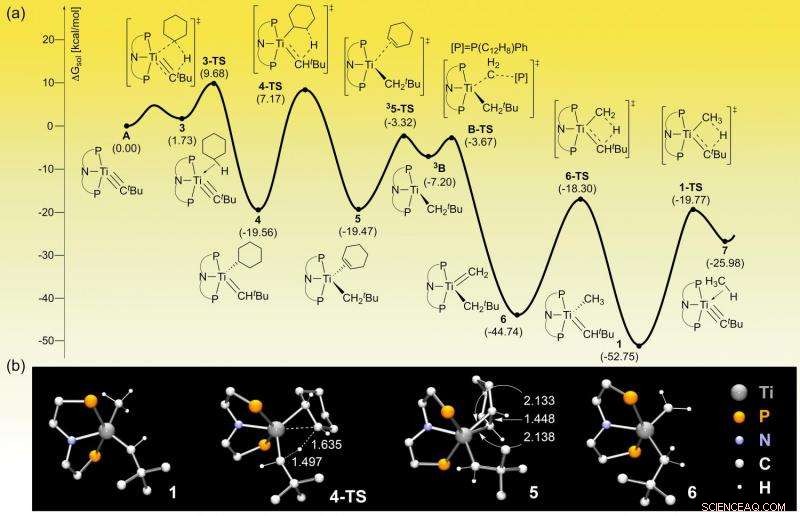
Computer gegenereerd energieprofiel van de reactie. Computersimulaties kunnen de tussencomponenten van de chemische reactie voorspellen en hoeveel energie daarvoor nodig is. Krediet:Instituut voor Basiswetenschappen
De studie bereikte de goedkope productie van olefinen dankzij een synergetisch teamwerk tussen computer- en experimentele chemici. Door het hele chemische proces te simuleren, IBS-computerchemici adviseerden hun collega's van de Universiteit van Pennsylvania over goedkope op titanium gebaseerde katalysatoren om te testen.
"We zijn verhuisd van iridium, dat zo zeldzaam en duur is dat het wordt bestempeld als 'het element van de goden', tot een absoluut goedkoop metaal, titanium; een element dat we allemaal kennen omdat het veel wordt gebruikt als wit pigment voor keramiek, papier, en tandenbleekmiddel, " legt BAIK Mu-Hyun uit, de leidende auteur van IBS. "De computersimulatie voorspelt de beweging van elk elektron en hoe moleculen gaan interageren, dus het stelde ons in staat om de ontwikkelingstijd te verkorten."
Samenvatten, de studie toonde aan dat het maken van olefinen in een goedkope, energiezuinige manier mogelijk. De reactie kan bij lage temperatuur worden uitgevoerd en de titaniumkatalysator kan gedeeltelijk worden gerecycled, zodat het opnieuw kan worden gebruikt om meer aardgas te dehydrogeneren. De volgende uitdaging van het onderzoeksteam is om de op titanium gebaseerde katalysator efficiënter te maken.
 Foto-responsieve eiwithydrogels als middel voor gecontroleerde afgifte van stamcellen/eiwitten
Foto-responsieve eiwithydrogels als middel voor gecontroleerde afgifte van stamcellen/eiwitten Nieuwe SERS-sensor helpt bij het detecteren van aldehydegassen
Nieuwe SERS-sensor helpt bij het detecteren van aldehydegassen Nieuw deactiveringsmechanisme voor gedetecteerde schakeleiwitten
Nieuw deactiveringsmechanisme voor gedetecteerde schakeleiwitten Het verschil tussen gietijzer en gietstaal
Het verschil tussen gietijzer en gietstaal Wetenschappers richten zich op kankerbehandelingen met CRISPR
Wetenschappers richten zich op kankerbehandelingen met CRISPR
 Mineralogen identificeren een groep mineralen die hun bestaan te danken hebben aan menselijke activiteit
Mineralogen identificeren een groep mineralen die hun bestaan te danken hebben aan menselijke activiteit Hoe de rijstproductie in India zich kan aanpassen aan de uitdagingen van de klimaatverandering
Hoe de rijstproductie in India zich kan aanpassen aan de uitdagingen van de klimaatverandering Intensivering van tropische storm Jelawat geëvalueerd door NASA's GPM-satelliet
Intensivering van tropische storm Jelawat geëvalueerd door NASA's GPM-satelliet Waar is je provinciehoofdstad? Een moderne wiskundige methode voor het berekenen van geografische centra
Waar is je provinciehoofdstad? Een moderne wiskundige methode voor het berekenen van geografische centra Wetenschappers vinden een fluctuerende stijgende trend van open landbouwstroverbranding in Noordoost-China
Wetenschappers vinden een fluctuerende stijgende trend van open landbouwstroverbranding in Noordoost-China
Hoofdlijnen
- Laat je huisdier niet per ongeluk dronken worden dit gekke seizoen (sorry Tiddles)
- Wat is het verschil tussen Ribosoom en Ribosomaal DNA?
- Wat doen de Centrioles tijdens de interfase?
Centriolen vormen het microtubulekelet van de cel tijdens de interfase en dupliceren tijdens de S-fase van de interfase, samen met het DNA. Interphase bestaat uit de G1-, S- en G2-fasen. Centriolen komen
- Vier klassen Macromoleculen die belangrijk zijn voor levende wezens
- Waarom stinkt de stinkplant?
- Kan de groei van volwassen hersencellen de manier waarop we denken over veroudering veranderen?
- Wat gebeurt er wanneer glucose een cel binnengaat?
- Maki's zijn raar omdat het fruit van Madagascar raar is
- Wat zijn de stappen in de meiose die de variabiliteit verhogen?
- Hoeveel pot in die brownie? Chocolade kan tests afwerpen

- Parodontitis:onderzoekers zoeken naar een nieuwe werkzame stof
- Morsen in een nucleaire faciliteit toont potentiële brandwondenrisico's van een huishoudelijke chemische stof

- Nieuwe microfluïdische chip verhoogt de gevoeligheid van immunoassays met 1000x

- Onderzoekers ontwerpen sensoren om plantenhormonen snel te detecteren
 Hoe som en verschillen met breuken te schatten
Hoe som en verschillen met breuken te schatten Nieuwe formatietheorie verklaart het mysterieuze interstellaire object Oumuamua
Nieuwe formatietheorie verklaart het mysterieuze interstellaire object Oumuamua NASA's MISR-instrument ziet Californische bosbrandrookpluimen vanuit de ruimte
NASA's MISR-instrument ziet Californische bosbrandrookpluimen vanuit de ruimte Webtool biedt directe toegang tot wereldwijde klimaatgegevens
Webtool biedt directe toegang tot wereldwijde klimaatgegevens Hoe de Mollen van HNO3 te vinden
Hoe de Mollen van HNO3 te vinden  Nieuwe techniek maakt het printen van flexibele, rekbare zilveren nanodraadcircuits
Nieuwe techniek maakt het printen van flexibele, rekbare zilveren nanodraadcircuits De manier waarop we over bodems denken, van de grond af aan transformeren
De manier waarop we over bodems denken, van de grond af aan transformeren Grootste politiemacht in de VS stapt het dronetijdperk in
Grootste politiemacht in de VS stapt het dronetijdperk in
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

