
Wetenschap
Nieuwe therapeutische strategie tegen slaapziekte
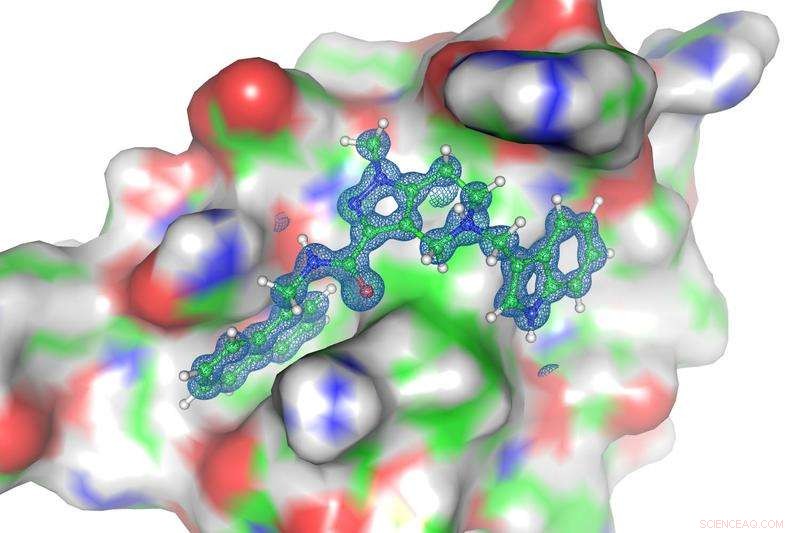
Structuur van de interface van PEX14 en PEX5 (achterkant) inclusief de structuur van de remmer (voorkant). Krediet:Dr. Grzegorz Popowicz, Helmholtz Zentrum München
Een nieuw ontwikkeld klein molecuul doodt selectief de ziekteverwekker die slaapziekte en de ziekte van Chagas veroorzaakt. Wetenschappers van het Helmholtz Zentrum München, samen met collega's van de Technische Universiteit van München en de Ruhr Universiteit Bochum, rapporteer deze bevindingen in Wetenschap . De truc:de onderzoekers konden eerst de achilleshiel van de parasiet bepalen met behulp van moderne structurele biologietechnieken en vervolgens een remmer ontwikkelen met een perfecte pasvorm.
Trypanosomen ontlenen hun naam aan het Griekse trypano- (boorder) en soma (lichaam). De protozoaire parasieten zijn verantwoordelijk voor verschillende ziekten, vooral in Latijns-Amerika en Afrika. Het bekendste voorbeeld is waarschijnlijk slaapziekte, die wordt veroorzaakt door trypanosomen en overgedragen door tseetseevliegen. In de eindfase, patiënten lijden aan oncontroleerbare slaap, waaraan de ziekte zijn naam ontleent.
"Tot nu, er zijn slechts een paar medicijnen tegen trypanosomen geweest. Deze medicijnen hebben veel ongewenste bijwerkingen, en de eerste gevallen van resistentie verspreiden zich al, " legt Prof. Dr. Michael Sattler uit, Directeur van het Instituut voor Structurele Biologie aan het Helmholtz Zentrum München en hoogleraar Biomoleculaire NMR-spectroscopie aan de Technische Universiteit van München. Samen met Dr. Grzegorz Popowicz (ook Helmholtz Zentrum München) en de groep onder leiding van Prof. Dr. Ralf Erdmann aan de Ruhr Universiteit Bochum, het onderzoeksteam zocht naar nieuwe mogelijkheden om de ziekteverwekker te deactiveren. "We concentreerden ons vooral op de zogenaamde PEX-eiwitten, die al enige tijd ter discussie staan als mogelijke doelwitten voor farmacologische interferentie, ', zegt Sattler.
PEX-eiwitten zijn de sleutel
De PEX-eiwitten spelen een cruciale rol in de functie van de zogenaamde glycosomen. Dit zijn kleincellige organellen die belangrijk zijn voor het in stand houden van het suikermetabolisme van de parasiet. "Het idee was om de interactie tussen twee essentiële eiwitten te voorkomen, PEX14 en PEX5, en bijgevolg het trypanosoommetabolisme zo effectief te verstoren dat de parasieten niet kunnen overleven, " legt Grzegorz Popowicz uit. In het Beierse NMR-centrum, een gezamenlijke onderzoeksinfrastructuur van het Helmholtz Zentrum en TU München, de onderzoekers gebruikten daarom eerst nucleaire magnetische resonantie (NMR) om de structuur van de twee doeleiwitten te onderzoeken.
In de volgende stap, de teams uit München en Bochum gebruikten de aldus bepaalde ruimtelijke structuur om een stof te optimaliseren die specifiek bindt aan PEX14, waardoor de interactie met PEX5 wordt voorkomen, die uiteindelijk de parasiet doodt. Grzegorz Popowicz beschrijft het als, "We hebben min of meer eerst het slot opgemeten en daarna de juiste sleutel ontwikkeld."
Mogelijk ook relevant voor andere parasieten
In de toekomst, de onderzoekers willen deze moleculen verder ontwikkelen met behulp van medicinale chemie, zodat ze kunnen worden getest in klinische studies en, uiteindelijk kan worden goedgekeurd als geneesmiddel. Ze onderzoeken ook in hoeverre de aanpak geschikt is om andere eencellige parasieten te doden die mogelijk afhankelijk zijn van vergelijkbare eiwitten. "Een mogelijkheid zou zijn om de Leishmania-parasiet aan te pakken, " legt Popowicz uit. Toekomstig onderzoek in deze richting zal volgen.
 Het vrijkomen van radioactieve deeltjes in Fukushima was significant, zegt nieuw onderzoek
Het vrijkomen van radioactieve deeltjes in Fukushima was significant, zegt nieuw onderzoek Hoe beïnvloedt de stikstofdynamiek de koolstof- en waterbudgetten in China?
Hoe beïnvloedt de stikstofdynamiek de koolstof- en waterbudgetten in China? Maakt een beperkte ondergrondse waterberging planten minder vatbaar voor droogte?
Maakt een beperkte ondergrondse waterberging planten minder vatbaar voor droogte? Meer redenen voor optimisme over klimaatverandering dan we in decennia hebben gezien
Meer redenen voor optimisme over klimaatverandering dan we in decennia hebben gezien Klimaatverandering zou de rijstopbrengst kunnen verhogen
Klimaatverandering zou de rijstopbrengst kunnen verhogen
Hoofdlijnen
- De fabrieksproductie afremmen kan averechts werken, studie vondsten
- Bedoelden ze dat? Ongeval en opzet in een octopussentuin
- Reproductie van plantaardige cellen
- Hoe vergif Sumac te behandelen?
- Ontrafelen wat genomics kan doen
- Ideeën voor Cookie Science Fair Projects
- Nieuw onderzoek naar speurhonden kan levens redden
- Wetenschappers onderzoeken de gevolgen voor de nationale veiligheid van genbewerking
- Charles Lyell: Biography, Theory of Evolution & Facts
- Nieuwe microscooptechniek onthult interne structuur van levende embryo's
- Lichtgevoelige toplaag van plastic folie zorgt voor beweging

- Innovatieve fotokatalytische materialen van koolstofnanobuisjes voor efficiënte omzetting van zonne-energie en waterstofproductie
- Onderzoekers doen inspanningen om parasitaire rondwormen te bestrijden
- Snelle test om astma te diagnosticeren

 Een lijst met meetinstrumenten
Een lijst met meetinstrumenten Wetenschappers voltooien conserveringspuzzel, begrip van het leven op aarde vormen
Wetenschappers voltooien conserveringspuzzel, begrip van het leven op aarde vormen Technologische vooruitgang en het effect op het ecosysteem
Technologische vooruitgang en het effect op het ecosysteem Hoe gender en stereotypen onze relatie met honden kunnen bepalen
Hoe gender en stereotypen onze relatie met honden kunnen bepalen Studie werpt licht op waarom een warmere wereld gelijk kan zijn aan een natter Arctisch gebied
Studie werpt licht op waarom een warmere wereld gelijk kan zijn aan een natter Arctisch gebied Astronomen ontdekken duister verleden van planeetetende Death Star
Astronomen ontdekken duister verleden van planeetetende Death Star Hoe de perimeter van verschillende vormen te vinden
Hoe de perimeter van verschillende vormen te vinden Koelende rol van fijnstof bij opwarming aarde sterker dan eerder gedacht
Koelende rol van fijnstof bij opwarming aarde sterker dan eerder gedacht
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Portuguese | Swedish | German | Dutch | Danish | Norway | Spanish |

-
Wetenschap © https://nl.scienceaq.com

