
Wetenschap
Onderzoekers onderzoeken systematisch de werkzaamheid van CRISPR-antimicrobiële middelen
Het antimicrobiële potentieel van CRISPR-Cas-systemen is veelbelovend, maar hoe CRISPR-nucleasen het beste kunnen worden ontworpen of geïmplementeerd, blijft nog steeds slecht begrepen. Een internationaal team onder leiding van het Helmholtz Instituut voor RNA-gebaseerd Infectieonderzoek (HIRI) in Würzburg heeft deze kenniskloof nu aangepakt.
De onderzoekers hebben de eerste systematische ondervraging van CRISPR-antimicrobiële stoffen uitgevoerd met behulp van multiresistente en hypervirulente bacteriën als casestudy's, waarbij grote variaties in de werkzaamheid aan het licht kwamen die konden worden voorspeld via high-throughput screening en machinaal leren. Hun bevindingen zijn gepubliceerd in het tijdschrift Nucleic Acids Research .
De ontdekking van antimicrobiële verbindingen zoals conventionele antibiotica heeft de geneeskunde getransformeerd, waardoor de behandeling van infecties mogelijk is geworden die ooit als onbehandelbaar werden beschouwd. De ontwikkelingspijplijn voor nieuwe middelen is echter vertraagd, terwijl het oneigenlijke gebruik van bestaande antibiotica de opkomst van antibioticaresistentie heeft aangewakkerd. Bijgevolg is er een groeiende behoefte aan nieuwe middelen om ziekteverwekkers uit te roeien.
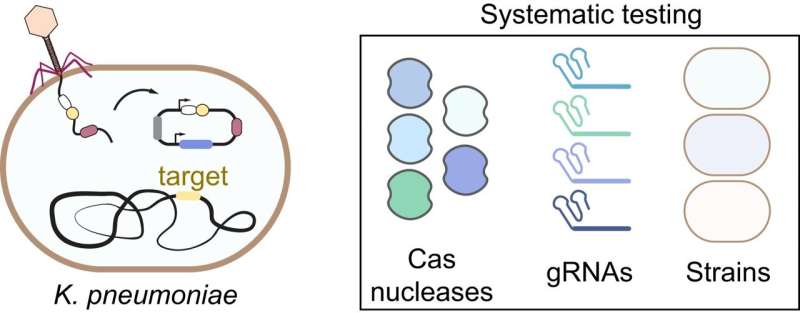
CRISPR-Cas-systemen, adaptieve immuunmechanismen die bacteriën gebruiken om zich te verdedigen tegen virale invasie, bieden een onderscheidende oplossing door hun vermogen om microben selectief te elimineren, uitsluitend op basis van genetische sequenties. Tot nu toe ontbreken systematische onderzoeken om de werkzaamheid van deze CRISPR-antimicrobiële stoffen te beoordelen, vooral voor verschillende nucleasen, doellocaties en bacteriestammen.
Om deze leemte aan te pakken heeft een internationaal team onder leiding van het Helmholtz Institute for RNA-based Infection Research (HIRI), een locatie van het Braunschweig Helmholtz Center for Infection Research (HZI) in samenwerking met de Julius-Maximilians-Universität Würzburg (JMU), nu de eerste uitgebreide ondervraging van deze nieuwe agenten ondernomen. Hun onderzoek richt zich op Klebsiella pneumoniae, een bacterie die berucht is vanwege zijn associatie met antibioticaresistentie.
"Klebsiella pneumoniae biedt een bijzonder overtuigende casestudy, aangezien het talrijke stammen omvat met verschillende virulentie- en resistentiekenmerken", zegt Chase Beisel, hoofd van de afdeling RNA Synthetische Biologie van het HIRI en professor aan de Medische Faculteit van JMU. Hij leidde het internationale onderzoek in samenwerking met onderzoekers van het Institut Pasteur in Parijs, Frankrijk, de Universiteit van Tel Aviv in Israël, HZI en de Universiteit van Toronto in Canada.
Het team combineerde expertise op het gebied van CRISPR-technologieën, Klebsiella-bacteriën, de levering van bacteriofagen, schermen met hoge doorvoer en machinaal leren die nodig zijn om een onderzoek van deze omvang uit te voeren.
Een andere soort, (soms) een ander effect
CRISPR-Cas-systemen maken gebruik van een geavanceerd verdedigingsmechanisme:een CRISPR-ribonucleïnezuur (RNA) helpt regio's van een vreemd genoom, zoals DNA of RNA, te detecteren voor gerichte splitsing. Vervolgens knipt het CRISPR-geassocieerde (Cas)-nuclease zijn doelwit door, vergelijkbaar met een moleculaire schaar.
De wetenschappers ontdekten dat verschillende CRISPR-nucleasen sterk uiteenlopende werkzaamheid vertonen. In hun experimenten vertoonden nucleasen die zich op DNA richtten superieure prestaties vergeleken met nucleasen die zich op RNA richtten.
Bovendien vertoonden verschillende typen K. pneumoniae variatie in hun gevoeligheid voor een CRISPR-antimicrobieel middel, ondanks het gebruik van identieke nucleasen om zich op identieke plaatsen te richten. Elena Vialetto, de eerste auteur van het onderzoek en voormalig Ph.D. student in het Beisel-lab zegt:"De variabele antimicrobiële activiteit tussen verwante bacteriën was verrassend gezien het gebruik van dezelfde CRISPR-constructen. We schreven dit verschil toe aan de vouwing van de CRISPR-RNA's die de DNA-targeting begeleiden."
Beisel voegt hieraan toe:"Deze studie is de eerste die aantoont dat de antibacteriële effectiviteit zelfs tussen verwante stammen kan variëren."
Om kenmerken te onderzoeken die de targeting over verschillende stammen zouden kunnen verbeteren, voerden de onderzoekers een genoombrede screening uit bij verschillende K. pneumoniae-typen. Deze inspanning leverde ontwerpprincipes en parameters op voor mogelijke CRISPR-antimicrobiële stoffen en vergemakkelijkte de training van een algoritme om de efficiëntie ervan te voorspellen.
Fagen als Trojaanse paarden
Het team waagde zich ook aan de volgende fase van actieve agentontwikkeling, namelijk levering. De onderzoekers gebruikten bacteriofagen als vehikels voor de CRISPR-antimicrobiële stoffen, die ze uitrustten met gemodificeerde staartvezels om het bereik van de CRISPR-lading te vergroten.
Deze studie legt de basis voor de verdere ontwikkeling van CRISPR als middel om antibioticaresistente infecties te voorkomen of te behandelen.
"We hopen dat dit werk een grotere zichtbaarheid zal geven aan het gebruik van CRISPR als antimicrobieel middel op maat in de voortdurende strijd tegen antibioticaresistentie", besluit Beisel.