Wetenschap
Inzicht in het mechanisme van schade door ultraviolet licht en kankerlaesies kan bijdragen aan antikankertherapie
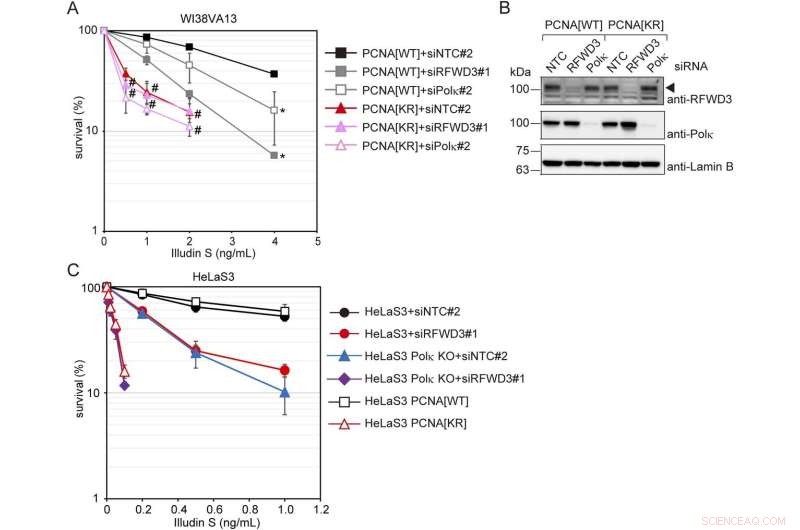
RFWD3- en Polκ-gemedieerde DNA-schadetolerantieroutes zijn onafhankelijk van elkaar, maar beide zijn afhankelijk van PCNA-modificaties op K164. (A) PCNA [WT] en [KR] cellen werden getransfecteerd met siRFWD3#1, siPolκ#2 of siNTC#2. Cellen werden gedurende 4 d blootgesteld aan illudine S en geanalyseerd met MTS-assay. Gegevens worden weergegeven als gemiddelden ± SD van n =4 onafhankelijke experimenten. *P <0,05 versus siNTC#2; #, niet significant versus siNTC#2. (B) Whole-cell lysaten van de cellen met behulp van (A) werden bereid en geanalyseerd door immunoblotting met behulp van anti-RFWD3, anti-Polκ en anti-Lamin B1-antilichamen. De pijlpunt toont het RFWD3-signaal. (C) HeLaS3- en HeLaS3 Polκ KO-cellen werden getransfecteerd met siRFWD3 # 1 of siNTC # 2 en gedurende 4 dagen blootgesteld aan illudin S. HeLaS3 PCNA [WT] of PCNA [KR] cellen werden gedurende 4 dagen blootgesteld aan illudine S. Cellulaire overleving werd geëvalueerd door MTS-assay. Gegevens worden weergegeven als gemiddelden ± SD van n =4 (HeLaS3+siNTC#2, HeLaS3+siRFWD3#2 en HeLaS3 Polκ KO+siNTC#2) of n =3 (HeLaS3 Polκ KO+siRFWD3#1, HeLaS3 PCNA[WT ] en PCNA[KR]) onafhankelijke experimenten. Statistische significantie werd geëvalueerd door middel van een tweezijdige t-test. Krediet:Life Science Alliance (2022). DOI:10.26508/lsa.202201584
Een team onder leiding van onderzoekers van de Nagoya University in Japan heeft nieuwe paden ontdekt die cellen gebruiken om zichzelf te herstellen na blootstelling aan ultraviolet (UV) licht, en een nieuw middel dat bij deze paden betrokken is, bekend als RFWD3. Dit zou kunnen leiden tot toekomstige behandelingen voor mensen met lichtgevoelige ziekten en zou kunnen leiden tot de ontwikkeling van betere geneesmiddelen tegen kanker. "Wij geloven dat onze bevindingen een nieuw perspectief bieden op het gebied van DNA-schaderespons en ook op celbiologie", zegt hoofdauteur, Chikahide Masutani. Ze publiceerden hun onderzoek in het tijdschrift Life Science Alliance .
Net zoals ons lichaam tijdens het leven snij- en schaafwonden krijgt, kan DNA ook kleine stukjes cumulatieve schade oplopen. Een veel voorkomende vorm van dergelijke schade is een DNA-laesie. Blootstelling aan UV-licht kan er bijvoorbeeld voor zorgen dat een deel van het DNA een beschadigde plek bevat of een van de paren verandert. Anders gezegd, we kunnen DNA zien als een geschreven zin. In een zin zou een DNA-laesie zijn als een verkeerd gedrukt woord, waardoor het onleesbaar wordt. Op dezelfde manier dat het afdrukken van een reeks boeken inclusief verkeerd gedrukte woorden alle boeken onleesbaar maakt, kan een DNA-laesie het hele genoom onstabiel maken of permanente mutaties veroorzaken wanneer het wordt gekopieerd. Deze laesies zijn belangrijk omdat ze in verband worden gebracht met vele vormen van kanker.
Om de effecten van een DNA-laesie tegen te gaan, hebben menselijke lichamen meerdere routes voor DNA-schadetolerantie. Deze routes maken replicatie mogelijk, zelfs in de aanwezigheid van laesies. Dienovereenkomstig hebben biologen getracht de factoren te identificeren die betrokken zijn bij niet-geïdentificeerde tolerantiemechanismen voor DNA-schade.
Een dergelijke factor is in het bijzonder het prolifererende celkernantigeen (PCNA). PCNA activeert trans-laesie-DNA-synthese, die laesies herstelt met behulp van het enzym DNA-polymerase eta (Pol-eta). Hoewel deze route interessant is omdat het cellen weerstand biedt tegen UV-straling en sommige DNA-beschadigende middelen, kunnen andere routes ook belangrijk zijn, vooral die routes die onafhankelijk zijn van Pol-eta.
Een groep onderzoekers van de Universiteit van Nagoya, onder leiding van Rie Kanao en Chikahide Masutani van het Research Institute of Environmental Medicine, heeft nieuwe middelen ontdekt door opzettelijk laesies te creëren met illudin S, een paddenstoelentoxine en zijn afgeleide irofulven. De onderzoekers ontdekten dat cellen zonder PCNA-modificatie gevoelig waren voor deze verbindingen en laesies veroorzaakten. Aan de andere kant waren die zonder Pol-eta dat niet. Daarom konden ze de PCNA-modificatie-afhankelijke route van laesieherstel analyseren, onafhankelijk van de Pol-eta-route.
Kanao en Masutani hebben vastgesteld dat de middelen in de PCNA-modificatie-afhankelijke route RFWD3, een eiwitcoderend gen, omvatten. RFWD3 is gemeenschappelijk voor beide routes, daarom suggereert dit dat de twee belangrijkste takken van de route Pol-eta en RFWD3 zijn voor laesies veroorzaakt door UV-licht, en polymerase kappa en RFWD3 voor die veroorzaakt door illudin S. "Het kan een algemeen kenmerk zijn dat verschillende DNA-polymerasen worden gebruikt, afhankelijk van het type DNA-laesie", legt Masutani uit. "Onze bevindingen suggereren dat RFWD3 bijdraagt aan PCNA-modificatie-afhankelijke DNA-schadetolerantie. Dit is de eerste beschrijving van de betrokkenheid van RFWD3 bij UV-overleving in menselijke cellen."
Een veelbelovend gebruik van dit onderzoek is voor de behandeling van kanker, omdat het mogelijk kan worden om de tolerantieroutes voor DNA-schade te remmen. Hoewel DNA-schadetolerantie zou moeten helpen bij het herstellen van laesies, gebruiken kankers soms de middelen om hen te helpen DNA-beschadigende geneesmiddelen tegen kanker te verdragen. "Wij geloven dat het onderzoek kan bijdragen aan kankertherapie," zei Masutani. "Er is steeds meer bewijs dat we kankercellen kunnen sensibiliseren voor conventionele chemotherapeutische middelen door het remmen van DNA-schadetolerantieroutes. Meer onderzoek naar nieuwe therapieën op dit gebied zou uiteindelijk kunnen leiden tot de ontwikkeling van een nieuwe klasse van kankertherapeutische middelen die de respons op behandeling verbeteren. conventionele chemotherapie gebruiken." + Verder verkennen
DNA-replicatie onder de microscoop
 Onderzoekers ontrafelen de actieve fase in katalytische reductie van kooldioxide tot methanol
Onderzoekers ontrafelen de actieve fase in katalytische reductie van kooldioxide tot methanol Hoe de hoeveelheid vrijgekomen warmte te berekenen
Hoe de hoeveelheid vrijgekomen warmte te berekenen  San Antonio-onderzoekers proberen storingen in de ruimtevaart en rampen met olielozingen te voorkomen
San Antonio-onderzoekers proberen storingen in de ruimtevaart en rampen met olielozingen te voorkomen Verband tussen het atoomgetal en de chemische reactiviteit van alkali-metalen
Verband tussen het atoomgetal en de chemische reactiviteit van alkali-metalen Onderzoekers rapporteren een eenvoudigere methode voor het veilig omgaan met methaanthiol bij chemische synthese
Onderzoekers rapporteren een eenvoudigere methode voor het veilig omgaan met methaanthiol bij chemische synthese
Hoofdlijnen
- Wetenschappers volgen aseksuele kleine wormen - waarvan de afstamming 18 miljoen jaar teruggaat
- Meerdere stressoren kunnen interactief leiden tot verslechtering van aquatische ecosystemen
- Voordelen en nadelen van XRD en XRF
- Onderzoek toont aan dat het verwijderen van invasieve planten de biodiversiteit in beekwateren kan vergroten
- Waar wordt de kern in de cel gevonden en waarom?
- Onderzoekers creëren nieuwe letters om DNA-functies te verbeteren
- Oudste ontdekking tot nu toe van fysogastrische insecten
- Ideeën voor wetenschapsbeurzen Projecten met honden
- Wat is de meest logische volgorde van stappen voor het splitsen van vreemd DNA?
 NRL-onderzoekers volgen het veranderende Noordpoolgebied met geluid
NRL-onderzoekers volgen het veranderende Noordpoolgebied met geluid Hoog, niet plat:nanodraden voor een nieuwe chiparchitectuur
Hoog, niet plat:nanodraden voor een nieuwe chiparchitectuur Nieuwe studie verdrievoudigt schatting van red snapper in Golf van Mexico
Nieuwe studie verdrievoudigt schatting van red snapper in Golf van Mexico Wat hangt er in de lucht? Er komt meer bij kijken dan we dachten
Wat hangt er in de lucht? Er komt meer bij kijken dan we dachten Nieuw bewijs toont aan dat de crash met Antlia 2 de Melkweg de rimpelingen in de buitenste schijf gaf
Nieuw bewijs toont aan dat de crash met Antlia 2 de Melkweg de rimpelingen in de buitenste schijf gaf Nieuwe roofzuchtige dinosaurus toegevoegd aan de prehistorie van Australië
Nieuwe roofzuchtige dinosaurus toegevoegd aan de prehistorie van Australië Afvoer van fosfor verminderen
Afvoer van fosfor verminderen De spin van een zwart gat meten
De spin van een zwart gat meten
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com