
Wetenschap
Onderzoek identificeert mechanismen die bacteriële overleving bevorderen
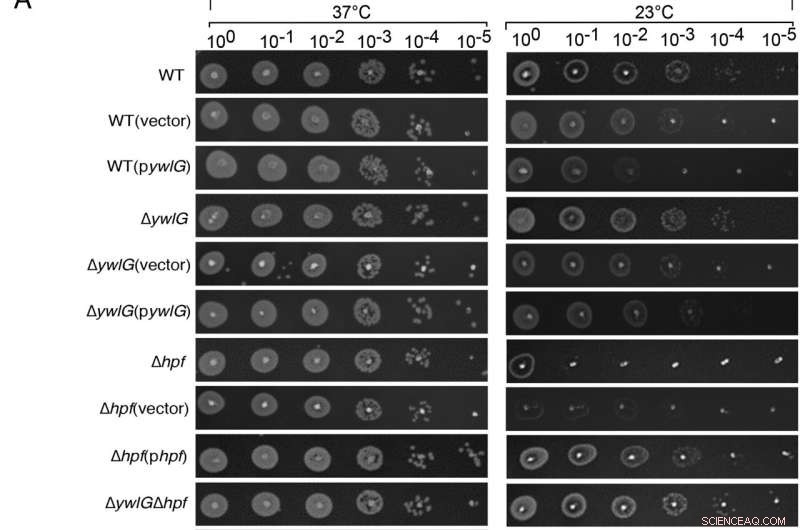
Het inactiveren van ywlG onderdrukt de koudegevoeligheid van een Δhpf-null-mutant op een mediumafhankelijke manier. Complementatie met plasmide-gecodeerde ywlG en hpf bevestigde de YwlG-gemedieerde onderdrukking en HPF-afhankelijke koude respons. Seriële verdunningsvlektesten werden uitgevoerd op (A) op lysogeniebouillon (LB) gebaseerde of (B) op tryptische sojabouillon (TSB) gebaseerde agarplaten. Exponentieel groeiende cellen (OD600 =0,6) in TSB werden aangepast tot OD600 =0,2 na twee wasbeurten in 1xPBS. Na seriële verdunningen werd 2 µL van elke verdunning op de agarplaten gespot. De resultaten werden geregistreerd na 24 uur en 48 uur incubatie bij respectievelijk 37°C en 23°C. De afbeeldingen zijn representatief voor drie onafhankelijke experimenten. Credit:Procedures van de National Academy of Sciences (2022). DOI:10.1073/pnas.2207257119
Onderzoekers van de Northwestern Medicine hebben nieuwe regulerende mechanismen ontdekt die de overleving van bacteriën bevorderen, volgens bevindingen gepubliceerd in de Proceedings of the National Academy of Sciences .
De studie, geleid door M.-N. Frances Yap, Ph.D., universitair hoofddocent Microbiologie-Immunologie, legt ook de basis voor het identificeren van nieuwe therapeutische doelen voor de behandeling van bacteriële infecties.
Ribosoomwinterslaap is een mechanisme dat wordt uitgevoerd door bacteriën en andere organismen, waaronder eukaryoten, om op lange termijn te overleven. Hibernerende 100S-ribosomen in bacteriën bestaan uit twee 70S-complexen die met elkaar zijn verbonden door een hibernation-promoting factor (HPF)-eiwit.
Dit 100S-complex heeft twee hoofddoelen:het voorkomen van de afbraak van eiwitbiosynthesemachines (ribosomen) en het besparen van energie in de cel door mRNA-translatie af te sluiten.
In de huidige studie gebruikte het team van Yap massaspectrometrie om eiwitinteracties te bestuderen in methicilline-resistente Staphylococcus aureus, een bacterie waarvan algemeen bekend is dat ze stafylokokbesmettingen veroorzaakt. Uit deze analyses bleek dat HPF een interactie aangaat met een voorheen niet-geïdentificeerde bindingspartner die zich buiten het ribosoom bevindt, een eiwit genaamd YwlG.
Bovendien, door de atomaire structuur van YwlG op te lossen, ontdekten ze dat dit eiwit betrokken is bij glutamaathydrogenase-activiteit, wat een essentiële metabole route is die nodig is voor het overleven van bacteriën.
"Onder normale omstandigheden is een fractie van het YwlG-eiwit aan de HPF gebonden. Door samen te binden, kan YwlG de glutamaathydrogenase-activiteit niet stimuleren en kan HPF niet aan het ribosoom binden, dus het is 'wederzijdse sekwestratie' van de twee eiwitten om de juiste hoeveelheid te verzekeren van 100S-complexen en cellulair glutamaatdehydrogenase worden geproduceerd," zei Yap.
De bevindingen wijzen op zowel HPF als YwlG als factoren die de bacteriële kolonisatie en de ernst van de infectie beïnvloeden. Het einddoel is volgens Yap om een verbinding te identificeren die de vorming van deze complexen kan verstoren en op zijn beurt de overleving van bacteriën op de lange termijn kan remmen.
"Een belangrijk voordeel is dat eiwit vergelijkbaar met HPF of YwlG niet bestaat bij mensen, dus je zou een HPF- of YwlG-targeting antibacterieel middel kunnen ontwikkelen dat de bacteriegroei remt maar de gastheren niet schaadt," zei Yap. + Verder verkennen
Hibernerende ribosomen helpen bacteriën te overleven
 Krachtige aardbeving schokt Indonesië, veel gebouwen storten in
Krachtige aardbeving schokt Indonesië, veel gebouwen storten in Alaska gaat gebrek aan verse groenten tegen met kasgids
Alaska gaat gebrek aan verse groenten tegen met kasgids VS getroffen door rampen van 18 miljard dollar dit jaar tot nu toe
VS getroffen door rampen van 18 miljard dollar dit jaar tot nu toe Ervaringen zijn niet altijd beter voor de planeet dan producten - zo maak je duurzame herinneringen
Ervaringen zijn niet altijd beter voor de planeet dan producten - zo maak je duurzame herinneringen Wat is het landschap van de toendra?
Wat is het landschap van de toendra?
Hoofdlijnen
- PITT-route:wetenschappers ontdekken hoe cellen een levensduurbevorderend recyclingsysteem repareren
- Voorbij geluid:roodoogboomkikkers gebruiken geluid en trillingen bij het zoeken naar vrienden en agressie
- Daling van huismus in verband met luchtvervuiling en slechte voeding
- Stijgende temperaturen veranderen grote populatie zeeschildpadden vrouw
- Chimpansees die het huis verlaten stellen het ouderschap uit
- Ziekteverwekkers tegen elkaar keren om resistentie tegen geneesmiddelen te voorkomen
- Geluid onthult dat gigantische blauwe vinvissen met de wind dansen om voedsel te vinden
- Hoe succesvol te zijn in de microbiologie
- Planten kunnen kiezen tussen alternatieve reacties op concurrentie
- Microben die gaatjes veroorzaken, kunnen superorganismen vormen die kunnen kruipen en zich op de tanden kunnen verspreiden
- Dichte vloeistofdruppels fungeren als mobiele computers

- Onderzoekers ontdekken dat twee verschillende ecologische mechanismen veerkracht kunnen bieden tegen invasieve soorten

- Houden mannelijke vissen ze liever groot en kleurrijk?

- Studie vertelt over pompoenkleurige zombies

 Kwantumfysica en origami voor de ultieme beterschapskaart
Kwantumfysica en origami voor de ultieme beterschapskaart Oscillerende quasideeltjes:de cyclus van verval en wedergeboorte
Oscillerende quasideeltjes:de cyclus van verval en wedergeboorte Wereldwijde handelsoorlogen riskeren miljoenen banen:WTO-chef
Wereldwijde handelsoorlogen riskeren miljoenen banen:WTO-chef Nieuwe tests van nanogestructureerd materiaal kunnen leiden tot betere bepantsering
Nieuwe tests van nanogestructureerd materiaal kunnen leiden tot betere bepantsering Effecten nadat ze in een kogelvrij vest zijn neergeschoten
Effecten nadat ze in een kogelvrij vest zijn neergeschoten  Detectortechnologie levert ongekende 3D-beelden op, kondigt een veel grotere toepassing aan om neutrino's te bestuderen
Detectortechnologie levert ongekende 3D-beelden op, kondigt een veel grotere toepassing aan om neutrino's te bestuderen Eversource geeft het Northern Pass-waterkrachtproject op
Eversource geeft het Northern Pass-waterkrachtproject op Studie beschrijft cellulaire fabrieken in meer detail
Studie beschrijft cellulaire fabrieken in meer detail
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

