
Wetenschap
Ontdekking helpt de nauwkeurigheid van CRISPR-Cas9-genbewerking te verbeteren
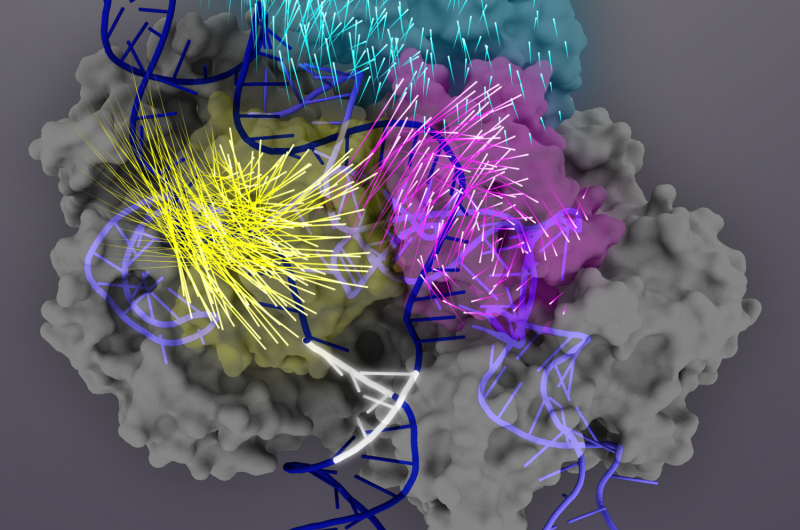
Het Cas9-eiwit (grijs) is een RNA-geleid nuclease dat kan worden geprogrammeerd om elke overeenkomende DNA-sequentie te binden en te knippen (donkerblauwe dubbele helix), waardoor het een krachtig hulpmiddel is voor genoomengineering. Bij doelbinding, Cas9-eiwitdomeinen ondergaan conformationele herschikkingen (de bewegingen van individuele aminozuren worden weergegeven door raketstaarten) om het Cas9-sgRNA-complex te activeren voor doelsplitsing. Het REC3-domein (blauwgroen) is verantwoordelijk voor het detecteren van doelen, die de buitenwaartse rotatie van het REC2-domein (magenta) signaleert om een pad te openen voor het HNH-nucleasedomein (geel). Deze actieve conformatie van Cas9 is dan in staat om een gezamenlijke splitsing van beide strengen van het doel-DNA teweeg te brengen. Credit:Janet Iwasa-afbeelding voor Doudna Lab
Wetenschappers van de Universiteit van Californië, Berkeley en het Massachusetts General Hospital hebben een sleutelgebied binnen het Cas9-eiwit geïdentificeerd dat bepaalt hoe nauwkeurig CRISPR-Cas9 zich in een doel-DNA-sequentie bevindt, en hebben het aangepast om een hypernauwkeurige gen-editor te produceren met het laagste niveau van off-target snijden tot nu toe.
Het eiwitdomein dat de onderzoekers identificeerden als een meester-controller van DNA-knippen, is een duidelijk doelwit voor re-engineering om de nauwkeurigheid nog verder te verbeteren, zeggen de onderzoekers. Deze aanpak zou wetenschappers moeten helpen varianten van Cas9 - het eiwit dat DNA bindt en knipt - aan te passen om de kans te minimaliseren dat CRISPR-Cas9 DNA op de verkeerde plaats bewerkt, een belangrijke overweging bij het doen van gentherapie bij mensen.
Een strategie om verbeterde nauwkeurigheid te bereiken, is het creëren van mutaties in het regerende eiwitdomein, genaamd REC3, en kijk welke de nauwkeurigheid verbeteren zonder de efficiëntie van het snijden op het doel te beïnvloeden.
"We hebben ontdekt dat zelfs kleine wijzigingen in het REC3-domein van Cas9 het verschil tussen on- en off-target editing beïnvloeden, wat suggereert dat dit domein een voor de hand liggende kandidaat is voor diepgaande mutagenese om de targetingspecificiteit te verbeteren. In het verlengde van dit werk, men zou een meer onbevooroordeelde mutagenese binnen REC3 kunnen uitvoeren dan de gerichte mutaties die we hebben gemaakt, " zei co-eerste auteur Janice Chen, een afgestudeerde student in het lab van Jennifer Doudna, mede-uitvinder van de CRISPR-Cas9-tool voor het bewerken van genen.
Co-eerste auteurs Chen, Yavuz Dagdas en Benjamin Kleinstiver, en hun collega's van UC Berkeley, Massachusetts General Hospital en Harvard University rapporteren hun resultaten vandaag online voorafgaand aan publicatie in het tijdschrift Natuur .
Hyper-nauwkeurige Cas9
Sinds 2012, wanneer Doudna, een professor in de moleculaire en celbiologie en een onderzoeker van het Howard Hughes Medical Institute aan de UC Berkeley, en collega Emmanuelle Charpentier van het Max Planck Institute for Infection Biology hergebruikten het Cas9-eiwit om een goedkoop, nauwkeurige en gebruiksvriendelijke gen-editor, onderzoekers hebben geprobeerd de kans op off-target editing te verkleinen. Hoewel verbeterde betrouwbaarheid fundamenteel onderzoek ten goede komt, het is absoluut cruciaal bij het bewerken van genen voor klinische toepassingen, omdat elke DNA-knipbeurt buiten het doelwit belangrijke genen kan uitschakelen en kan leiden tot permanente, onverwachte bijwerkingen.
In de afgelopen twee jaar, twee teams ontwikkelden zeer nauwkeurige Cas9-eiwitten - een verbeterde specificiteit genaamd eSpCas9(1.1) en een high-fidelity genaamd SpCas9-HF1 - en Chen en Doudna probeerden te achterhalen waarom ze met een hogere specificiteit snijden dan het wildtype Cas9-eiwit van Streptococcus pyogenes wordt tegenwoordig veel gebruikt.
Momenteel, onderzoekers die CRISPR-Cas9 gebruiken, creëren een single-guide RNA (sgRNA) - een RNA-molecuul dat een keten van 20 ribonucleïnezuren bevat die een specifieke 20-nucleïnezuur-DNA-sequentie die ze willen targeten aanvult - en deze aan Cas9 koppelen. Dit gids-RNA stelt Cas9 in staat om zich thuis te voelen in het complementaire DNA, bind eraan en knip de dubbelstrengige helix door. Maar het Cas9-sgRNA-complex kan ook binden aan DNA dat niet precies overeenkomt, wat leidt tot ongewenst off-target snijden.
in 2015, Doudna's lab ontdekte een conformationele schakelaar van Cas9 die wordt geactiveerd wanneer de RNA-gids en het DNA-doel overeenkomen. Ze ontdekten dat alleen wanneer het RNA en DNA nauw overeenkomen, de 3D-structuur van Cas9, in het bijzonder de conformatie van het HNH-nucleasedomein, verander en activeer de schaar van Cas9. Echter, het proces dat verantwoordelijk is voor het detecteren van de nucleïnezuren stroomopwaarts van de conformationele switch bleef onbekend.
In de huidige studie, Chen en Dagdas gebruikten een techniek genaamd single-molecule FRET (Förster-resonantie-energieoverdracht) om precies te meten hoe de verschillende eiwitdomeinen in het Cas9-sgRNA-eiwitcomplex - in het bijzonder REC3, REC2 en HNH - bewegen wanneer het complex aan DNA bindt.
Ze stelden eerst vast dat de specificiteitsvoordelen van eSpCas9(1.1) en SpCas9-HF1 konden worden verklaard door het feit dat de drempel voor de HNH-conformationele switch veel hoger was voor deze Cas9-varianten dan voor het wildtype Cas9-eiwit. waardoor de eSpCas9(1.1)- en SpCas9-HF1-varianten minder snel de schaar activeren wanneer ze gebonden zijn aan een off-target sequentie.
Volgende, ze ontdekten dat het REC3-domein verantwoordelijk is voor het detecteren van de nauwkeurigheid van doelbinding, die vervolgens de buitenwaartse rotatie van het REC2-domein signaleert om een pad te openen voor het HNH-nucleasedomein, het activeren van de schaar. Deze actieve conformatie van Cas9 is dan in staat om beide strengen van het doel-DNA te splitsen.
Chen, Dagdas en Kleinstiver toonden vervolgens aan dat door delen van REC3 te muteren, het is mogelijk om de specificiteit van het Cas9-eiwit te wijzigen, zodat het HNH-nuclease niet wordt geactiveerd tenzij het gids-RNA en het doel-DNA heel dicht bij elkaar liggen. Ze waren in staat om een verbeterde hypernauwkeurige Cas9 te ontwikkelen, genaamd HypaCas9, dat zijn efficiëntie op het doel behoudt, maar iets beter is in het onderscheiden tussen on- en off-target-sites in menselijke cellen.
"Als je bepaalde aminozuurresten muteert in REC3, u kunt de balans tussen Cas9-activiteit op het doel en verbeterde specificiteit aanpassen; we hebben de goede plek kunnen vinden waar er voldoende activiteit is op het beoogde doel, maar ook een grote vermindering van off-target-evenementen, ' zei Chen.
Door de relaties tussen structuur, functie en dynamiek van Cas9, Doudna en haar team hopen het eiwit verder te ontwikkelen met een uitstekende gevoeligheid om op betrouwbare en efficiënte wijze een verscheidenheid aan genetische veranderingen uit te voeren.
 Chemici ontwikkelen veilige alternatieven voor ftalaten die in kunststoffen worden gebruikt
Chemici ontwikkelen veilige alternatieven voor ftalaten die in kunststoffen worden gebruikt Biochemici melden een manier om de onsterfelijkheid van kankercellen met oligonucleotiden te stoppen
Biochemici melden een manier om de onsterfelijkheid van kankercellen met oligonucleotiden te stoppen Verklaar de betekenis van de zin kort voor het oplossen van een mengsel van verbindingen
Verklaar de betekenis van de zin kort voor het oplossen van een mengsel van verbindingen  Wetenschappers ontwikkelen nieuw concept van beperkte katalyse onder 2D-materialen
Wetenschappers ontwikkelen nieuw concept van beperkte katalyse onder 2D-materialen Nieuwe ultraresistente en zelfherstellende betonmaterialen
Nieuwe ultraresistente en zelfherstellende betonmaterialen
 Enorm oud meer over prairies dat snel genoeg leegliep om een ijstijd te veroorzaken, studie suggereert:
Enorm oud meer over prairies dat snel genoeg leegliep om een ijstijd te veroorzaken, studie suggereert: Studie onderzoekt hoe gesteente zich uitbreidt in de buurt van het bodemoppervlak in de zuidelijke Sierra Nevada
Studie onderzoekt hoe gesteente zich uitbreidt in de buurt van het bodemoppervlak in de zuidelijke Sierra Nevada Beroemdheden leiden TED wereldwijde oproep om actie te ondernemen tegen klimaatcrisis
Beroemdheden leiden TED wereldwijde oproep om actie te ondernemen tegen klimaatcrisis NASA's infraroodanalyse van tropische storm Sebastien ziet windschering
NASA's infraroodanalyse van tropische storm Sebastien ziet windschering Wat gebeurt er nadat vulkanen uitbarsten?
Wat gebeurt er nadat vulkanen uitbarsten?
Hoofdlijnen
- Diversiteit en immigratie verhogen de productiviteit in microbiële gemeenschappen
- Artefacten suggereren aankomst van mensen in Australië 18,
- Warme wateren in het noordwesten trekken paaiende vissen naar het noorden
- Tropische kevers worden met uitsterven bedreigd
- DNA-bewijs onthult twee vergeten Noord-Amerikaanse migraties
- De bacteriële gemeenschap op het internationale ruimtestation lijkt op huizen
- Een studie schakelt over van genetische naar metabole analyse om het evolutionaire proces te reconstrueren
- Haaien evolueerden vliegtuigachtige attributen om in habitats te passen
- Race om Indonesische krokodil te redden die is getroffen door een bandenketting
- Waarom zijn cellen belangrijk voor levende organismen?
- Niet alle kroontjeskruid is gelijk voor eierleggende monarchen, studie onthult

- De spieren van het menselijk lichaam onthouden
- Celsignalen die wondgenezing in gang zetten zijn verrassend complex
- Killer-tandpijn veroorzaakt waarschijnlijk ellende voor orka's in gevangenschap

 Een getijdenklok instellen
Een getijdenklok instellen Een innovatie die horizonten opent voor monitoring op afstand van broeikasgassen
Een innovatie die horizonten opent voor monitoring op afstand van broeikasgassen Hybride werken voedt de vraag naar meer technologie en grotere huizen, en beide zijn slecht nieuws voor de planeet
Hybride werken voedt de vraag naar meer technologie en grotere huizen, en beide zijn slecht nieuws voor de planeet Monsanto-aandelen springen op rapport van Amerikaanse goedkeuring van Bayer-deal
Monsanto-aandelen springen op rapport van Amerikaanse goedkeuring van Bayer-deal Vervuiling door nutriënten maakt verzuring van de oceaan erger voor koraalriffen
Vervuiling door nutriënten maakt verzuring van de oceaan erger voor koraalriffen Welke organen werken met het oog?
Welke organen werken met het oog?  Het gebruik van verschillende gevormde magneten
Het gebruik van verschillende gevormde magneten  Helder als modder:uitdrogingsscheuren helpen de vorm van water op Mars te onthullen
Helder als modder:uitdrogingsscheuren helpen de vorm van water op Mars te onthullen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

