
Wetenschap
Wetenschappers pionieren met nieuw chemisch conversieproces bij lage temperatuur
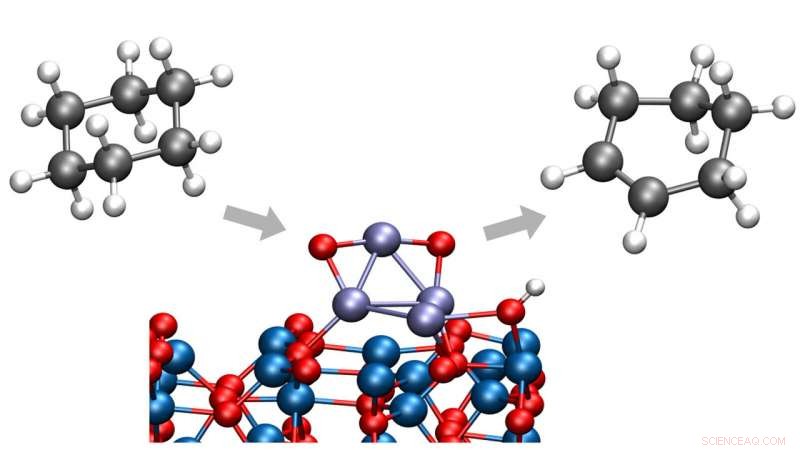
Argonne-chemici hebben een manier gevonden om cyclohexaan om te zetten in cyclohexeen of cyclohexadieen, beide belangrijke chemicaliën in een breed scala van industriële processen. Het nieuwe proces vindt plaats bij lage temperaturen, het elimineren van het ontstaan van ongewenste bijproducten. Krediet:Argonne National Laboratory
Chemici besteden veel tijd en energie aan het op gang brengen of versnellen van chemische reacties, maar soms kan het net zo belangrijk zijn om ze te stoppen voordat ze te ver gaan.
In een recente studie van het Argonne National Laboratory van het Amerikaanse Department of Energy (DOE), scheikundigen hebben een manier gevonden om cyclohexaan om te zetten in cyclohexeen of cyclohexadieen, belangrijke chemicaliën in een breed scala van industriële processen. belangrijk, dit proces vindt plaats bij lage temperaturen, het elimineren van de vorming van koolstofdioxide die het gevolg zou zijn van een ongewenste verbreking van koolstof-koolstofbindingen.
Cyclohexaan is een belangrijk startmolecuul in een breed scala aan chemische reacties, volgens Argonne-chemicus Stefan Vajda, nu aan het J. Heyrovský Instituut voor Fysische Chemie in Praag. Echter, zonder een geschikte katalysator om de reactie te starten, het omzetten van cyclohexaan in bruikbare producten vereist typisch verhoogde temperaturen die worden gegenereerd door het verbruik van veel energie, en het proces kan ook lijden aan een slechte selectiviteit.
In de studie, Vajda en Argonne chemicus Larry Curtiss en hun internationale team van medewerkers onderzochten een soort reactie genaamd oxidatieve dehydrogenering, waarin waterstofmoleculen worden ontdaan van een groter molecuul. Door een beperkt aantal waterstof-koolstofbindingen te verbreken, de reactie kan cyclohexeen en cyclohexadieen produceren voordat verbranding tot kooldioxide plaatsvindt.
Het werk verbeterde ten opzichte van eerdere studies door het Argonne-team over de dehydrogenering van cyclohexaan en cyclohexeen door twee belangrijke componenten te introduceren:een kobaltoxidekatalysator van sub-nanometerformaat op een aluminiumoxidedrager en een gecontroleerde zuurstofomgeving.
De onderzoekers gebruikten röntgenverstrooiingstechnieken bij Argonne's Advanced Photon Source (APS), een DOE Office of Science gebruikersfaciliteit, om de aard en stabiliteit van de katalysatoren tijdens het katalytisch testen van de clusters in realtime te volgen. Ze ontdekten dat de clusters gedeeltelijke dehydrogenering van het cyclohexaan uitvoerden bij temperaturen rond de 100 graden Celsius - veel lager dan eerder was waargenomen voor dit soort reacties, en de clusters behielden hun geoxideerde aard en stabiliteit bij reactietemperaturen tot 300°C.
"Het feit dat we deze omzetting bij lagere temperaturen kunnen laten plaatsvinden, beschermt de intermediaire dehydrogeneringsproducten cyclohexeen en cyclohexadieen tegen verdere omzetting in ongewenste producten, ' zei Vajda.
Vajda en Curtiss merkten op dat de zeer selectieve katalysator lang meegaat en niet vergiftigd of afgebroken wordt door de reactie. Bij theoretisch en experimenteel onderzoek naar de grootte van de katalysator, de onderzoekers ontdekten dat clusters van grootte vier en zevenentwintig atomen ongeveer even efficiënt waren in het uitvoeren van de reactie. "Het lijkt erop dat zolang de katalysator kleiner is dan ongeveer een nanometer, deze samenstelling werkt goed - een belangrijke factor voor de mogelijke opschaling van deze klasse van katalysatoren door meer traditionele, hoewel minder selectief op maat, syntheseroutes." zei Vajda.
Om de basismechanismen achter de activiteit en selectiviteit van de kobaltkatalysatoren beter te begrijpen, de onderzoekers gebruikten berekeningen van de dichtheidsfunctionaaltheorie om de reactieroutes te modelleren. "De uitstekende prestaties van de kobaltclusters kunnen worden verklaard door theoretische berekeningen, die zeer actieve kobaltatomen in de clusters onthullen en aantonen dat de geoxideerde aard van de clusters de vorming van het product bij lage temperatuur veroorzaakt, ' legde Curtiss uit.
 Noodmaatregelen door droogte voor wilde paarden in het westen van de VS
Noodmaatregelen door droogte voor wilde paarden in het westen van de VS Waarom koralen niet altijd symbionten doorgeven aan hun nakomelingen
Waarom koralen niet altijd symbionten doorgeven aan hun nakomelingen Wetenschappers naderen bron van tsunami's in Shetland
Wetenschappers naderen bron van tsunami's in Shetland Science Fair Project voor het testen van verschillende bodems met plantengroei
Science Fair Project voor het testen van verschillende bodems met plantengroei Implementatie van no-till en cover crops in katoensystemen in Texas
Implementatie van no-till en cover crops in katoensystemen in Texas
Hoofdlijnen
- De jacht op een van de Top 50 meest gezochte schimmels is voorbij
- Native Plants & Animals of France
- Drie manieren waarop genetische diversiteit optreedt tijdens meiose
- Nieuwe gorilla in Audubon Zoo mag nog even binnen blijven
- Saguaro en andere torenhoge cactussen hebben een roerige geschiedenis
- Leef snel, sterf jong:signaaldetectietheorie bijwerken
- Sociale omgeving is belangrijk voor de grootte van de eendenpenis
- Een flitsende gele keelzanger? Daar zijn genen voor
- Wetenschappers rapporteren chemische basis van de celdelingstimer, een mogelijk doelwit tegen kanker
- Nieuw materiaal maakt de weg vrij voor ademtestsensoren om chronische ziekten te detecteren

- Teamwetenschap leidt tot doorbraak in kooldioxideomzetting

- Polymeerbeweging:sleutel tot coatings van de volgende generatie

- Onderzoekers stellen nieuwe lat voor watersplitsing, CO2-splitsingstechnieken
- Nieuwe materialen:een tuimelschakelaar voor katalyse

 Ingrediënten in Fingerprinting Powder
Ingrediënten in Fingerprinting Powder  Hoe zal Canada zijn bosbranden in de toekomst beheren?
Hoe zal Canada zijn bosbranden in de toekomst beheren? Team ontwikkelt een familie van bio-geïnspireerde kunstmatige houtsoorten van traditionele harsen
Team ontwikkelt een familie van bio-geïnspireerde kunstmatige houtsoorten van traditionele harsen Mysterie van groene ijsbergen kan binnenkort worden opgelost
Mysterie van groene ijsbergen kan binnenkort worden opgelost De impact van consumentenonderzoek in de wereld vergroten
De impact van consumentenonderzoek in de wereld vergroten Boven-Nijl zal meer waterschaarste ervaren door warmere, drogere periodes
Boven-Nijl zal meer waterschaarste ervaren door warmere, drogere periodes Science Fair Project: Hoe een ei in een fles te krijgen
Science Fair Project: Hoe een ei in een fles te krijgen  Transistor zet een nieuwe standaard voor energie-efficiëntie
Transistor zet een nieuwe standaard voor energie-efficiëntie
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- Italian | Spanish | Portuguese | German | French | Swedish | Dutch | Norway | Danish |

-
Wetenschap © https://nl.scienceaq.com

