
Wetenschap
Op weg naar een biologisch alternatief
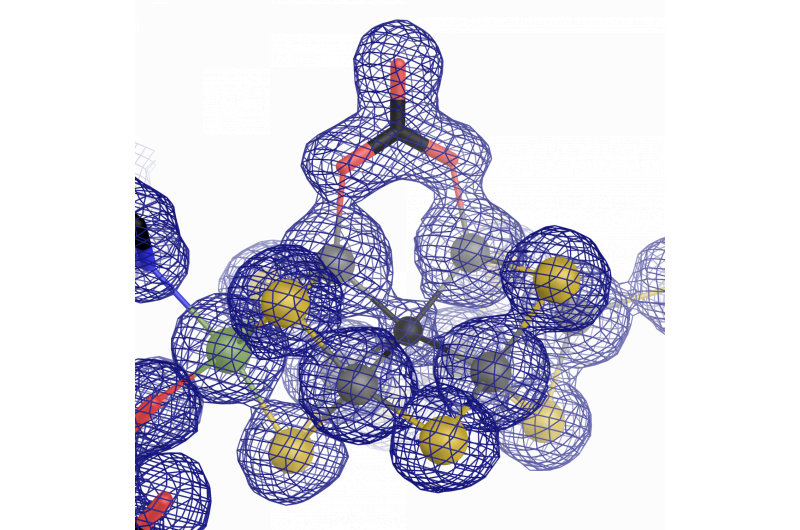
Het katalytische centrum van vanadium-stikstofase:een ijzer-vanadium-cofactor met een ongebruikelijk carbonaatligand. Krediet:Oliver Einsle
Het onderzoeksteam van Prof. Dr. Oliver Einsle van het Instituut voor Biochemie van de Universiteit van Freiburg heeft lang de werking van stikstofase onderzocht. Nu introduceert de groep de eerste driedimensionale structurele analyse van de enzymvariant die vanadium bevat. In het kader van de voorbereiding van zijn proefschrift, Daniel Sippel slaagde erin om vanadium-stikstofase te produceren en te kristalliseren. Dit als uitgangspunt nemend, hij gebruikte röntgendiffractie-experimenten om de ruimtelijke structuur op het niveau van atomaire resolutie op te helderen. Het langetermijndoel van het team is om stikstofase biotechnologisch bruikbaar te maken om alternatieven voor industriële chemische processen te ontwikkelen. De onderzoekers hebben hun bevindingen gepresenteerd in het wetenschappelijke tijdschrift Natuur Chemische Biologie .
Het element stikstof (N) is een sleutelcomponent van alle organische macromoleculen. De beschikbaarheid ervan in de biosfeer wordt beperkt door het feit dat het wereldwijde voorkomen van stikstof grotendeels beperkt blijft tot het gas N2 in de atmosfeer. De stabiliteit van N2 maakt het bovendien ontoegankelijk voor bijna alle organismen. Biologisch beschikbare stikstof voor landbouwmest wordt sinds 1906 gemaakt met behulp van het Haber-Bosch-proces. Dit industriële proces zet atmosferische stikstof (N2) om in ammoniak door een reactie met waterstof. Het belang ervan is tegenwoordig zo belangrijk omdat de voedselproductie voor meer dan de helft van de wereldbevolking alleen kan worden gegarandeerd met behulp van stikstofmeststoffen. In de natuur, slechts één enzym - bacteriële stikstofase - kan dezelfde reactie bereiken, maar zonder overtollige stikstofverbindingen in het milieu uit te stoten, of met andere woorden, uitspoeling van nitraten naar het grondwater. Maar tot nu toe, de functie van dit complex, metaalbevattend enzymsysteem dat metaal bevat, is slechts gedeeltelijk verklaard.
Het team van Einsle heeft al een belangrijke stap gezet in de richting van een beter begrip van stikstofase. Met het giftige gas koolmonoxide (CO) konden de onderzoekers de activiteit van het enzym remmen en laten zien hoe de remmer zich bindt aan de ijzer-molybdeen-cofactor (FeMoco). Bekend als de kern van stikstofase, het is genoemd naar de elementen die het bevat. FeMoco kan de reactie van stikstof en waterstof katalyseren in een natuurlijke versie van het Haber-Bosch-proces. Tegelijkertijd was het bekend dat een variant van stikstofase die vanadium in plaats van molybdeen in zijn actieve centrum bevat en daarom FeVco wordt genoemd, ook koolmonoxide kan omzetten. De producten van deze reactie zijn gereduceerde koolstofverbindingen in de vorm van korte koolstofketens. Deze reactie is de enzymatische versie van een tweede belangrijk chemisch proces - Fischer-Tropsch-synthese van koolwaterstoffen die op grote schaal kan worden gebruikt om brandstoffen uit industriële afvalgassen te synthetiseren, bijvoorbeeld.
Vanadium-stikstofstikstofase dat in bodembacteriën wordt aangetroffen, kan in zijn natuurlijke omgeving dezelfde synthese uitvoeren die alleen mogelijk is in industriële processen met behulp van extreme drukken en hoge temperaturen. De Haber-Bosch- en Fischer-Tropsch-processen worden jaarlijks gebruikt om honderden miljoenen tonnen van de respectieve gassen - N2 en CO - om te zetten, waardoor een duurzame, biologisch alternatief van groot wetenschappelijk belang.
Tijdens het onderzoekswerk, het werd duidelijk dat de meeste delen van de architectuur van het enzym vergelijkbaar waren met het "originele" dat molybdeen bevat. Hoe dan ook, er is een belangrijk onderscheid dat hen onderscheidt - de atomaire structuur van de katalytische cofactor. Sippel en Einsle ontdekten dat een vanadium-ion het molybdeen-ion in FeVco vervangt, en omvat een extra vervanging van een overbruggend sulfide-ion door een chemisch heel ander carbonaatanion (μ-1, 3 carbonaat-overbruggende ligand). Wat in eerste instantie een klein verschil lijkt, heeft verstrekkende gevolgen voor de geometrische en elektronische structuur van de cofactor.
Het onderzoek wordt gefinancierd door de European Research Council (ERC) en de German Research Foundation (DFG) in het kader van de onderzoekstrainingsgroep 1976 "Functional Diversity of Cofactors" van de Universiteit van Freiburg en het prioriteitsprogramma "Iron-Sulphur for Leven."
 Wat zijn enkele veel voorkomende huishoudelijke zuren en basen?
Wat zijn enkele veel voorkomende huishoudelijke zuren en basen?  Wetenschappers onthullen verborgen katalytisch oppervlak van Ni-Au-kernschil in kooldioxidehydrogenering
Wetenschappers onthullen verborgen katalytisch oppervlak van Ni-Au-kernschil in kooldioxidehydrogenering Industrieklaar proces maakt kunststoffen chemisch uit plantensuikers
Industrieklaar proces maakt kunststoffen chemisch uit plantensuikers Organische kation-intercalatie:een effectieve strategie voor het manipuleren van bandtopologie en supergeleiding
Organische kation-intercalatie:een effectieve strategie voor het manipuleren van bandtopologie en supergeleiding Hoe is polyurethaanschuim gemaakt?
Hoe is polyurethaanschuim gemaakt?
 Hectische strijd om de kust te beschermen terwijl de verslechterende olieramp in Orange County de stranden besluipt
Hectische strijd om de kust te beschermen terwijl de verslechterende olieramp in Orange County de stranden besluipt Lokaal weer beïnvloedt het smelten van een van de snelst terugtrekkende gletsjers van Antarctica
Lokaal weer beïnvloedt het smelten van een van de snelst terugtrekkende gletsjers van Antarctica Beschermen we rivieren en beken echt tegen vervuiling? Het is moeilijk te zeggen, en dat is een probleem
Beschermen we rivieren en beken echt tegen vervuiling? Het is moeilijk te zeggen, en dat is een probleem Wat kan ervoor zorgen dat de Mississippi-bocht hypoxisch wordt?
Wat kan ervoor zorgen dat de Mississippi-bocht hypoxisch wordt? De auto en New York City
De auto en New York City
Hoofdlijnen
- Studie van gierende kraanvogels onthult een band tussen paren zelfs voordat ze de paringsleeftijd hebben bereikt
- Spin eet spin:wetenschappers ontdekken 18 nieuwe op spinnen jagende pelikaanspinnen in Madagaskar
- Grote bedreigingen voor bodemecosystemen door een combinatie van invasieve soorten en klimaatverandering
- Onder het zee-ijs, aanschouw de oude Arctische kwallen
- Drone-foto's bieden snellere, goedkopere gegevens over de belangrijkste Antarctische soorten
- Golgi-apparaat: functie, structuur (met analogie en diagram)
- Onderzoekers ontdekken hoe cellen decennia later infecties onthouden
- Onderzoek bevestigt het:we worden echt dommer
- Hoe een 3D-diercelmodel te maken
- Kijken naar een medicijn in actie:precieze werking antikankermedicijnen in de cel opgehelderd
- Veel kleine verschillen dragen bij aan een grote variatie
- Wetenschappers lossen een magnesiummysterie op in de prestaties van oplaadbare batterijen

- Onderzoeksteam vindt mogelijke nieuwe aanpak voor medicijnen tegen slaapziekte
- Video:Hoe rubber sporten mogelijk maakt

 Wat eet regenwormen?
Wat eet regenwormen?  Zodra Starship-prototypes niet meer exploderen, we konden dit jaar een orbitale lancering zien
Zodra Starship-prototypes niet meer exploderen, we konden dit jaar een orbitale lancering zien IAEA dringt aan op snel plan voor opruiming van radioactief water in Fukushima
IAEA dringt aan op snel plan voor opruiming van radioactief water in Fukushima Langverwachte recensie onthult reis van water van interstellaire wolken naar bewoonbare werelden
Langverwachte recensie onthult reis van water van interstellaire wolken naar bewoonbare werelden Enorme tweelingster ontdekt knuffelend dicht bij zijn stellaire broer of zus in zijn wieg
Enorme tweelingster ontdekt knuffelend dicht bij zijn stellaire broer of zus in zijn wieg Hoe offshore boren werkt
Hoe offshore boren werkt  Hoe de ruimterace werkte
Hoe de ruimterace werkte  Wat betekent ion?
Wat betekent ion?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

