
Wetenschap
Blauwe fosfor:hoe een halfgeleider metaal wordt
Fosfor is een chemisch element met het symbool P en atoomnummer 15. Fosfor, een niet-metaal uit de stikstofgroep, wordt vaak aangetroffen in anorganische fosfaatgesteenten en in biologische moleculen zoals DNA en RNA. In zijn elementaire vorm is fosfor een wasachtige, witte vaste stof die zeer reactief is en gemakkelijk vlam kan vatten.
Wanneer fosfor tot een hoge temperatuur wordt verwarmd, ondergaat het een faseovergang en wordt het een halfgeleider. Halfgeleiders zijn materialen met een elektrische geleidbaarheid tussen die van een geleider en een isolator. Dit maakt ze bruikbaar voor een verscheidenheid aan elektronische toepassingen, zoals transistors en zonnecellen.
Wanneer fosfor echter tot een nog hogere temperatuur wordt verwarmd, ondergaat het een nieuwe faseovergang en wordt het een metaal. Metalen zijn materialen met een hoge elektrische geleidbaarheid. Dit maakt ze nuttig voor een verscheidenheid aan toepassingen, zoals draden en elektrische contacten.
Het vermogen van fosfor om van een halfgeleider in een metaal te veranderen is een unieke eigenschap die niet door veel andere elementen wordt gedeeld. Deze eigenschap maakt fosfor een veelbelovend materiaal voor een verscheidenheid aan elektronische toepassingen.
Toepassingen van blauwe fosfor
Blauwe fosfor heeft een aantal potentiële toepassingen op het gebied van elektronica. Deze toepassingen omvatten:
* Transistors: Blauwe fosfor kan worden gebruikt om transistors te maken die kleiner en sneller zijn dan traditionele siliciumtransistors. Dit zou kunnen leiden tot verbeteringen in de prestaties van computers en andere elektronische apparaten.
* Zonnecellen: Blauwe fosfor kan worden gebruikt om zonnecellen te maken die efficiënter zijn dan traditionele siliciumzonnecellen. Dit zou kunnen leiden tot een verlaging van de kosten van zonne-energie.
* Lichtgevende diodes (LED's): Blauwe fosfor kan worden gebruikt om LED's te maken die efficiënter en helderder zijn dan traditionele LED's. Dit zou kunnen leiden tot verbeteringen in de verlichting van woningen en kantoren.
Uitdagingen
Er zijn een aantal uitdagingen die moeten worden overwonnen voordat blauwe fosfor in commerciële toepassingen kan worden gebruikt. Deze uitdagingen omvatten:
* Synthese: Blauwe fosfor is moeilijk in grote hoeveelheden te synthetiseren. Dit komt omdat het een metastabiel materiaal is, wat betekent dat het niet de meest stabiele vorm van fosfor is.
* Stabiliteit: Blauwe fosfor is niet stabiel bij kamertemperatuur. Dit betekent dat het in een koude omgeving moet worden bewaard om te voorkomen dat het terugkeert naar zijn stabielere vorm.
* Doping: Blauwe fosfor is moeilijk te doteren, wat betekent dat de elektrische geleidbaarheid ervan moeilijk te controleren is. Dit is een uitdaging die overwonnen moet worden om blauwe fosfor in elektronische apparaten te kunnen gebruiken.
Conclusie
Blauwe fosfor is een veelbelovend materiaal met een aantal potentiële toepassingen op het gebied van elektronica. Er zijn echter een aantal uitdagingen die moeten worden overwonnen voordat blauwe fosfor in commerciële toepassingen kan worden gebruikt.
 Gecontroleerde afgifte van kunstmest met behulp van biopolymeerchips
Gecontroleerde afgifte van kunstmest met behulp van biopolymeerchips Wat is het verschil tussen koolstof-4-oxide en dioxide?
Wat is het verschil tussen koolstof-4-oxide en dioxide?  Wat is de pH-waarde van handdesinfecterend middel?
Wat is de pH-waarde van handdesinfecterend middel?  Hoe kunnen we zout-alkalibodems effectief verbeteren en gebruiken om de voedselzekerheid te garanderen?
Hoe kunnen we zout-alkalibodems effectief verbeteren en gebruiken om de voedselzekerheid te garanderen?  Een element heeft een atoomnummer van 30. Hoeveel protonen en elektronen zitten er in een neutraal atoom?
Een element heeft een atoomnummer van 30. Hoeveel protonen en elektronen zitten er in een neutraal atoom?
 Indringende vraag:Wat maakt een nummer pakkend?
Indringende vraag:Wat maakt een nummer pakkend?  Kunnen klimaatachterblijvers veranderen? Rusland moet, net als Australië, eerst aanzienlijke binnenlandse weerstand overwinnen
Kunnen klimaatachterblijvers veranderen? Rusland moet, net als Australië, eerst aanzienlijke binnenlandse weerstand overwinnen Prognoses met imperfecte gegevens en imperfect model
Prognoses met imperfecte gegevens en imperfect model Hoe Charles Darwin werkte
Hoe Charles Darwin werkte  Irma verloor wat macht over Cuba voor de aanval op Florida
Irma verloor wat macht over Cuba voor de aanval op Florida
Hoofdlijnen
- Parasitaire mieren veranderen de manier waarop gevangenen nestgenoten herkennen
- Hoe reist voedsel door je lichaam?
- Decodering van hondencognitie:machine learning geeft een glimp van hoe het brein van een hond vertegenwoordigt wat het ziet
- Hoe kan een verandering in het polypeptide de celactiviteit beïnvloeden?
- Hoe goed worden alternatieve eiwitbronnen ontvangen door de eindconsument?
- Studie:Hoe roodrot suikerriet aantast
- Waarom diepe oceanen leven gaven aan de eerste grote, complexe organismen
- Eencellig onderzoek belicht de rol van DNA-methylatie bij beslissingen over het lot van cellen
- Schooner water gekoppeld aan kleinere kokkels die jonger afsterven
- Wetenschappers ontwikkelen nieuw magnetisch nanomateriaal om vals geld te voorkomen

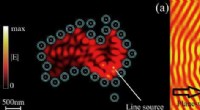
- Optische metacage blokkeert het binnendringen of ontsnappen van licht
- Groei van nanobuisjes gaat de goede kant op

- 3D-grafeen:zonnecellen nieuw platina?
- Phonon-tunneling verklaart de warmtestroom over nanometer-brede gaten, studie vondsten

 Nieuwe dieptekaart van de Noordelijke IJszee
Nieuwe dieptekaart van de Noordelijke IJszee Welke aanpassingen hebben wolven?
Welke aanpassingen hebben wolven?  Verhuurders spelen een cruciale rol bij het helpen van huurders bij het creëren van een huis, zeggen experts
Verhuurders spelen een cruciale rol bij het helpen van huurders bij het creëren van een huis, zeggen experts Afbeeldingen en gebaren zijn effectieve ondersteuningsmethoden bij het lesgeven in vreemde talen aan kinderen
Afbeeldingen en gebaren zijn effectieve ondersteuningsmethoden bij het lesgeven in vreemde talen aan kinderen Natuurkundigen ontwerpen een experiment om de oorsprong van de elementen vast te stellen
Natuurkundigen ontwerpen een experiment om de oorsprong van de elementen vast te stellen NASA lanceert delicate opslag van OSIRIS-REx-asteroïdemonsters
NASA lanceert delicate opslag van OSIRIS-REx-asteroïdemonsters Hier leest u hoe u opiniepeilingen representatiever en eerlijker kunt maken
Hier leest u hoe u opiniepeilingen representatiever en eerlijker kunt maken  Hoe zuur bier zo... zuur wordt
Hoe zuur bier zo... zuur wordt
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

