
Wetenschap
Deep learning lost al lang bestaande uitdagingen op bij het identificeren van de vorm van nanodeeltjes
Innovation Center of NanoMedicine heeft samen met de Universiteit van Tokio aangekondigd dat een groep onder leiding van prof. Takanori Ichiki, onderzoeksdirecteur van iCONM, een nieuwe methode voor de evaluatie van eigenschappen van de vormanisotropie van nanodeeltjes heeft voorgesteld, die al lang bestaande problemen in de evaluatie van nanodeeltjes oplost die teruggaan tot Einsteins tijd.
Het artikel, getiteld "Analysis of Brownian motion trajectories of non-spherical nanoparticles Using deep learning" werd online gepubliceerd in APL Machine Learning .
In dit tijdperk waarin nieuwe medische behandelingen en diagnostische technologieën waarbij gebruik wordt gemaakt van extracellulaire blaasjes en kunstmatige nanodeeltjes de aandacht trekken, zijn nanodeeltjes nuttige materialen op medisch, farmaceutisch en industrieel gebied. Vanuit materiaalperspectief is het noodzakelijk om de eigenschappen en agglomeratietoestand van elk nanodeeltje te evalueren en kwaliteitscontrole uit te voeren. Er wordt vooruitgang verwacht in de evaluatietechnologie voor nanodeeltjes die de veiligheid en betrouwbaarheid ondersteunt.
Eén manier om nanodeeltjes in vloeistof te evalueren is door het traject van de Brownse beweging te analyseren. Het heet NTA en berekent de diameter van een deeltje met behulp van een theoretische formule die Einstein meer dan 100 jaar geleden ontdekte. Hoewel het wordt gebruikt als een eenvoudige methode om afzonderlijke deeltjes van micro- tot nanogrootte te meten, bestaat er al lang een probleem dat het de vorm van nanodeeltjes niet kan beoordelen.
Het traject van de Brownse beweging weerspiegelt de invloed van de deeltjesvorm, maar het is moeilijk om extreem snelle bewegingen daadwerkelijk te meten. Bovendien zijn conventionele analysemethoden, zelfs als het deeltje niet-bolvormig is, niet nauwkeurig, omdat ze onvoorwaardelijk aannemen dat het deeltje bolvormig is en voor analyse de vergelijking van Stokes-Einstein gebruiken.
Met behulp van deep learning, dat goed is in het vinden van verborgen correlaties in grootschalige gegevens, is het echter mogelijk om verschillen te detecteren die worden veroorzaakt door verschillen in vorm die kunnen worden gedetecteerd, zelfs wanneer meetgegevens worden gemiddeld of fouten bevatten die niet van elkaar kunnen worden gescheiden.
P>De onderzoeksgroep van prof. Takanori Ichiki is erin geslaagd een diepgaand leermodel te bouwen dat vormen identificeert uit gemeten Brownse bewegingstrajectgegevens zonder de experimentele methode te veranderen. Om niet alleen rekening te houden met veranderingen in de tijdreeksen in gegevens, maar ook met de correlatie met de omgeving, integreerden ze een eendimensionaal CNN-model dat goed is in het extraheren van lokale kenmerken door middel van convolutie, en een bidirectioneel LSTM-model dat temporele gegevens kan accumuleren. dynamiek.
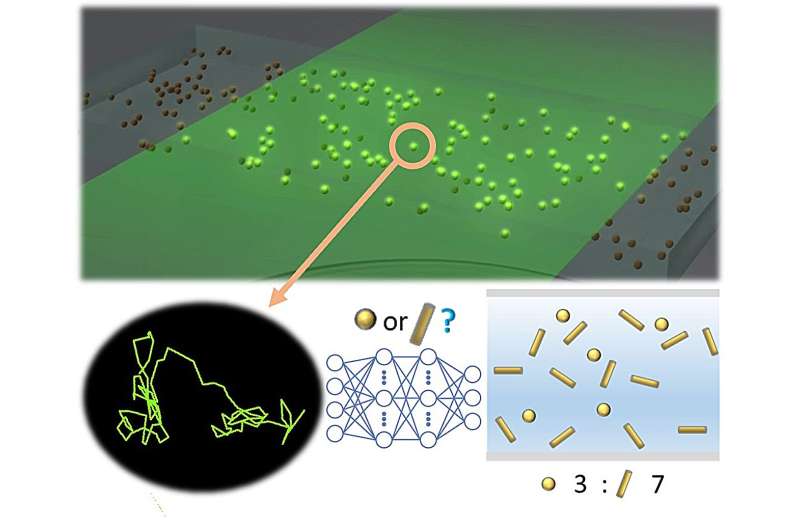
Door trajectanalyse met behulp van het geïntegreerde model konden ze een classificatienauwkeurigheid van ongeveer 80% bereiken op basis van één deeltje voor twee soorten gouden nanodeeltjes die ongeveer even groot zijn maar verschillende vormen hebben, die niet kunnen worden onderscheiden met alleen conventionele NTA.
Een dergelijke hoge nauwkeurigheid geeft aan dat de vormclassificatie van afzonderlijke nanodeeltjes in vloeistof met behulp van deep learning-analyse voor het eerst een praktisch niveau heeft bereikt. Bovendien is in het artikel een ijkcurve gemaakt om de mengverhouding van een gemengde oplossing van twee soorten nanodeeltjes (bolvormig en staafvormig) te bepalen. Gezien de vormtypen van nanodeeltjes die in de wereld beschikbaar zijn, wordt aangenomen dat deze methode de vorm voldoende kan detecteren.
Met conventionele NTA-methoden kan de vorm van de deeltjes niet direct worden waargenomen en was de verkregen karakteristieke informatie beperkt. Hoewel het traject van de Brownse beweging (tijdreekscoördinatengegevens) gemeten door het NTA-apparaat informatie bevat over de vorm van de nanodeeltjes, was het, omdat de relaxatietijd extreem kort is, moeilijk om de vormanisotropie van nanodeeltjes daadwerkelijk te detecteren. Bovendien is het bij conventionele analysemethoden, zelfs als het deeltje niet-bolvormig is, niet nauwkeurig omdat de vormfactor niet wordt toegepast, omdat wordt aangenomen dat het bolvormig is en wordt geanalyseerd met behulp van de Stokes-Einstein-vergelijking.
De onderzoekers streefden naar een nieuwe methode die iedereen kan implementeren, en konden een al lang bestaand probleem in de Brownse bewegingsanalyse oplossen door deep learning, dat goed is in het vinden van verborgen correlaties in grootschalige data, te introduceren in data-analyse zonder eenvoudige wijzigingen aan te brengen. experimentele methoden.
In dit artikel probeerden ze de vormen van twee soorten deeltjes te bepalen, maar gezien de soorten vormen van in de handel verkrijgbare nanodeeltjes denken ze dat deze methode kan worden gebruikt in praktische toepassingen zoals de detectie van vreemde stoffen in homogene systemen. Uitbreiding van NTA zal niet alleen leiden tot toepassingen in onderzoek, maar ook op industriële en industriële gebieden, zoals het evalueren van de eigenschappen, de agglomeratietoestand en de uniformiteit van nanodeeltjes die niet noodzakelijkerwijs bolvormig zijn, en kwaliteitscontrole.
Er wordt met name verwacht dat het een oplossing zal zijn voor het evalueren van de eigenschappen van diverse biologische nanodeeltjes, zoals extracellulaire blaasjes, in een omgeving die vergelijkbaar is met die van levende organismen. Het heeft ook het potentieel om een innovatieve benadering te zijn in fundamenteel onderzoek naar de Brownse beweging van niet-sferische deeltjes in vloeistoffen.
Meer informatie: Analyse van Brownse bewegingstrajecten van niet-sferische nanodeeltjes met behulp van deep learning, APL Machine Learning (2023). DOI:10.1063/5.0160979
Aangeboden door Innovation Center of NanoMedicine
 Efficiënte synthese van een fotosynthetisch pigment in zoogdiercellen voor optogenetica
Efficiënte synthese van een fotosynthetisch pigment in zoogdiercellen voor optogenetica Biasverdeling en regulatie in foto-elektrochemische algemene watersplitsende cellen
Biasverdeling en regulatie in foto-elektrochemische algemene watersplitsende cellen  Wat zijn de effecten van koken en vriezen op enzymactiviteit?
Wat zijn de effecten van koken en vriezen op enzymactiviteit?  De architecturen van binnenste mitochondriale membraaneiwitten begrijpen
De architecturen van binnenste mitochondriale membraaneiwitten begrijpen Hoe maak je een model van zuurstof voor school
Hoe maak je een model van zuurstof voor school
 Planten koloniseerden de aarde 100 miljoen jaar eerder dan eerder werd gedacht
Planten koloniseerden de aarde 100 miljoen jaar eerder dan eerder werd gedacht Zwaartekrachtgolfinzichten van internetstralende ballonnen
Zwaartekrachtgolfinzichten van internetstralende ballonnen Biden richt zich op de energiesector op fossiele brandstoffen met strenge nieuwe koolstofregels
Biden richt zich op de energiesector op fossiele brandstoffen met strenge nieuwe koolstofregels  Inheemse landbouw heeft het potentieel om bij te dragen aan de voedselbehoeften onder klimaatverandering
Inheemse landbouw heeft het potentieel om bij te dragen aan de voedselbehoeften onder klimaatverandering Methaanniveaus zijn gestegen in de regio Marcellus Shale ondanks een dip in de installatie van een put
Methaanniveaus zijn gestegen in de regio Marcellus Shale ondanks een dip in de installatie van een put
Hoofdlijnen
- Een modelhart maken met materialen uit uw huis
- Onderzoekers schijnen de schijnwerpers op illegale handel in wilde orchideeën
- Waarom hebben plantencellen zowel celwanden als celmembranen?
- Slapen wolven als honden?
- Epitheliale cellen: definitie, functie, typen en voorbeelden
- Slagen, grote oceaanreservaten moeten zowel het zeeleven als de mensen ten goede komen
- Identificatie van een nieuwe familie van op licht reagerende eiwitten
- Waarom ernstig bedreigde vrouwelijke walvissen moeite hebben om zich voort te planten
- Een technische verhoging van de mesofylgeleiding verbetert de fotosynthese-efficiëntie in veldproeven
- Verbazingwekkende resultaten uitgelegd - een multiband-benadering van Coulomb-weerstand en indirecte excitonen
- Hybride membraan zorgt voor opschudding op de wereldmarkt

- Methode om groot grafeen met één kristal te laten groeien, kan schaalbare 2D-materialen bevorderen

- Nieuwe methode voor het maken van kleine katalysatoren belooft veel voor luchtkwaliteit

- DNA-stenen maken zelfassemblage mogelijk van 3D-nanostructuren van 10, 000 unieke componenten

 Stoffig stervormend sterrenstelsel MAMBO-9 in detail onderzocht
Stoffig stervormend sterrenstelsel MAMBO-9 in detail onderzocht Hoe Lux-niveaus te berekenen
Hoe Lux-niveaus te berekenen Nieuw curriculum combineert nanotechnologie en skiën (met video)
Nieuw curriculum combineert nanotechnologie en skiën (met video) Een deel van je zonnebrand komt van verre sterrenstelsels
Een deel van je zonnebrand komt van verre sterrenstelsels  Arctische opwarming drie keer sneller dan de planeet, rapport waarschuwt
Arctische opwarming drie keer sneller dan de planeet, rapport waarschuwt Geen El Niño? Geen probleem. Aarde sist tot bijna recordhitte
Geen El Niño? Geen probleem. Aarde sist tot bijna recordhitte Donorincentives zijn niet altijd gelijk aan meer liefdadigheidsgiften, studie vondsten
Donorincentives zijn niet altijd gelijk aan meer liefdadigheidsgiften, studie vondsten ALMA onthult de zon in nieuw licht
ALMA onthult de zon in nieuw licht
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

