
Wetenschap
Door nanodeeltjes geleverd RNA vermindert neuro-ontsteking in laboratoriumtests
Langer Lab-student Jason Andresen en voormalig Tsai Lab-postdoc William Ralvenius leidden het werk en zijn de co-hoofdauteurs van het onderzoek. Owen Fenton, een voormalige postdoc van Langer Lab en nu assistent-professor aan de Eshelman School of Pharmacy van de Universiteit van North Carolina, is samen met Tsai en Langer een co-corresponderend auteur. Langer is hoogleraar chemische technologie, biologische technologie en het Koch Institute for Integrative Cancer Research.
Een deeltje perfectioneren
De eenvoudigste manier om te testen of siRNA de PU.1-expressie therapeutisch zou kunnen onderdrukken zou zijn geweest om gebruik te maken van een reeds beschikbaar toedieningsapparaat, maar een van de eerste ontdekkingen in het onderzoek is dat geen van de acht in de handel verkrijgbare reagentia gekweekte bacteriën veilig en effectief kan transfecteren menselijke microglia-achtige cellen in het laboratorium.
In plaats daarvan moest het team een LNP optimaliseren om de klus te klaren. LNP's hebben vier hoofdcomponenten, en door de structuren van twee ervan te veranderen en de verhouding tussen lipiden en RNA te variëren, konden de onderzoekers zeven formuleringen bedenken om te proberen. Belangrijk is dat hun tests onder meer bestonden uit het uitproberen van hun formuleringen op gekweekte microglia die ze in een ontstekingstoestand hadden gebracht. Die toestand is immers de toestand waarin de voorgestelde behandeling nodig is.
Van de zeven kandidaten viel er één op, het team genaamd "MG-LNP", vanwege de bijzonder hoge leveringsefficiëntie en veiligheid van een test-RNA-lading.
Wat in een gerecht werkt, werkt soms niet in een levend organisme, dus testte het team vervolgens de effectiviteit en veiligheid van hun LNP-formuleringen bij muizen. Door twee verschillende injectiemethoden te testen, in het lichaam of in het hersenvocht, ontdekten ze dat injectie in het hersenvocht een veel grotere werkzaamheid garandeerde bij het aanpakken van microglia zonder de cellen in andere organen te beïnvloeden.
Van de zeven formuleringen bleek MG-LNP opnieuw het meest effectief bij het transfecteren van microglia. Langer zei dat hij gelooft dat dit op een dag mogelijk nieuwe manieren zou kunnen openen om bepaalde hersenziekten met nanodeeltjes te behandelen.
Een gerichte therapie
Toen ze eenmaal wisten dat MG-LNP een testlading aan microglia kon leveren, zowel in menselijke celculturen als in muizen, testten de wetenschappers vervolgens of het gebruik ervan om een PU.1-onderdrukkend siRNA af te leveren de ontstekingen in microglia kon verminderen. In de celculturen bereikte een relatief lage dosis een vermindering van 42 procent van de PU.1-expressie (wat goed is omdat microglia op zijn minst een beetje PU.1 nodig hebben om te leven).
MG-LNP-transfectie veroorzaakte inderdaad geen enkele schade aan de cellen. Het verminderde ook aanzienlijk de transcriptie van de genen die de PU.1-expressie verhogen in microglia, wat aangeeft dat het meerdere ontstekingsmarkers kan verminderen.
Bij al deze en andere metingen presteerde MG-LNP beter dan een in de handel verkrijgbaar reagens genaamd RNAiMAX, dat de wetenschappers parallel testten.
"Deze bevindingen ondersteunen het gebruik van MG-LNP-gemedieerde anti-PU.1 siRNA-afgifte als een potentiële therapie voor neuro-inflammatoire ziekten", schreven de onderzoekers.
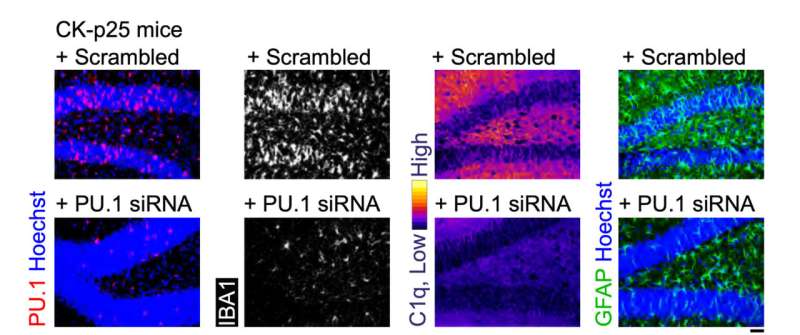
De laatste reeks tests evalueerde de prestaties van MG-LNP en leverde het siRNA op in twee muismodellen van ontstekingen in de hersenen. In één daarvan werden muizen blootgesteld aan LPS, een molecuul dat een infectie simuleert en een systemische ontstekingsreactie stimuleert. In het andere model vertonen muizen ernstige neurodegeneratie en ontstekingen wanneer een enzym genaamd CDK5 hyperactief wordt door een eiwit genaamd p25.
In beide modellen verminderde de injectie van MG-LNP's met het anti-PU.1-siRNA de expressie van PU.1 en ontstekingsmarkers, net zoals in gekweekte menselijke cellen.
"MG-LNP-afgifte van anti-PU.1-siRNA kan mogelijk worden gebruikt als een ontstekingsremmend therapeutisch middel bij muizen met systemische ontstekingen en in het CK-p25-muismodel van AD-achtige neuro-inflammatie", concludeerden de wetenschappers en noemden de resultaten een ‘proof-of-principle’. Er zullen meer tests nodig zijn voordat het idee bij menselijke patiënten kan worden uitgeprobeerd.
Meer informatie: William T. Ralvenius et al, Door nanodeeltjes gemedieerde toediening van anti-PU.1-siRNA via gelokaliseerde intracisternale toediening vermindert neuro-inflammatie, Geavanceerde materialen (2023). DOI:10.1002/adma.202309225
Journaalinformatie: Geavanceerde materialen
Aangeboden door Massachusetts Institute of Technology
 IJsbestendige coating voor grote constructies is afhankelijk van een prachtige demonstratie van mechanica
IJsbestendige coating voor grote constructies is afhankelijk van een prachtige demonstratie van mechanica Hoe de enzymactiviteit verandert als de enzymconcentratie afneemt
Hoe de enzymactiviteit verandert als de enzymconcentratie afneemt  Hoe scheikundigen moleculaire assemblagelijnen bouwen
Hoe scheikundigen moleculaire assemblagelijnen bouwen De hoogste hittebestendige kunststof ooit is ontwikkeld uit biomassa
De hoogste hittebestendige kunststof ooit is ontwikkeld uit biomassa Science Fair Projects & Ideas on Art
Science Fair Projects & Ideas on Art
 Microscopische planten in de oceanen - diatomeeën - vangen koolstofdioxide op via biofysische paden
Microscopische planten in de oceanen - diatomeeën - vangen koolstofdioxide op via biofysische paden Stadstuinen om luchtvervuiling te monitoren
Stadstuinen om luchtvervuiling te monitoren Experts:overstromingen in Europa tonen noodzaak om emissies te beteugelen, aanpassen
Experts:overstromingen in Europa tonen noodzaak om emissies te beteugelen, aanpassen Het aanpassen van de CO2-uitstoot aan de verplichtingen van Parijs zou hittegerelateerde sterfgevallen voorkomen
Het aanpassen van de CO2-uitstoot aan de verplichtingen van Parijs zou hittegerelateerde sterfgevallen voorkomen Is er fossiel bewijs voor de menselijke evolutie?
Is er fossiel bewijs voor de menselijke evolutie?
Hoofdlijnen
- Nieuwe studie onthult mechanisme voor hoe ziekteverspreidende prionen van de ene soort naar de andere kunnen springen
- T. rex niet zo slim als eerder werd beweerd, vinden wetenschappers
- Hoe een biologisch diagram te tekenen
- Sour Patch-volwassenen:1 op de 8 volwassenen houdt van extreme zuurheid, blijkt uit onderzoek
- Nadat de dinosauriërs waren verdwenen, werden zoogdieren sneller groter en stierven ze jong
- Pas op voor de huisdieren bij het hanteren van de Halloween-snoepvangst
- Een biobank van omkeerbare mutante embryonale stamcellen
- Welk bewijs is aanwezig Prokaryoten bestonden vóór eukaryoten?
- Onderzoekers ontdekken hoe gelei-zeedieren moderne robotica kunnen vormen
- DNA-nanotechnologie plaatst enzymkatalyse binnen een armlengte

- SMART ontdekt baanbrekende manier om naar het oppervlak van nanodeeltjes te kijken het versnellen van nano-engineering van materialen
- Coatings van professoren kunnen medische implantaten helpen beter te functioneren

- Memtransistor brengt wereld dichter bij hersenachtig computergebruik

- Lab maakt van moeilijk te verwerken plastic afval een meester voor het opvangen van koolstof
 Wat is het verschil tussen wespen en horzels?
Wat is het verschil tussen wespen en horzels?  Nissans No.3 stopt als klap op de vuurpijl voor opwekkingspogingen
Nissans No.3 stopt als klap op de vuurpijl voor opwekkingspogingen Knijpen van blaasjes door nauwe vernauwingen toont belofte voor gerichte medicijnafgifte
Knijpen van blaasjes door nauwe vernauwingen toont belofte voor gerichte medicijnafgifte Wetenschappers vinden oplossing om schadelijke plastic deeltjes in menselijk afvalwater te meten
Wetenschappers vinden oplossing om schadelijke plastic deeltjes in menselijk afvalwater te meten Kuikenembryo's leveren waardevolle genetische gegevens voor het begrijpen van de menselijke ontwikkeling
Kuikenembryo's leveren waardevolle genetische gegevens voor het begrijpen van de menselijke ontwikkeling Wat zou er nodig zijn om elke bedreigde diersoort te redden?
Wat zou er nodig zijn om elke bedreigde diersoort te redden?  Bitcoin-walvissen trekken aan de touwtjes van cryptocurrency
Bitcoin-walvissen trekken aan de touwtjes van cryptocurrency Een vreemd fenomeen ontrafelen dat zowel de prestaties van lithium-ionbatterijen helpt als schaadt
Een vreemd fenomeen ontrafelen dat zowel de prestaties van lithium-ionbatterijen helpt als schaadt
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

