
Wetenschap
Nanobiotica:nieuw machine learning-model voorspelt hoe nanodeeltjes interageren met eiwitten
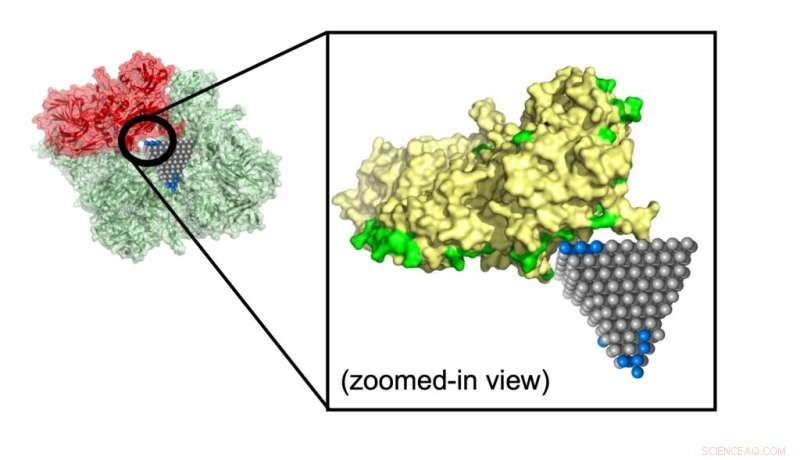
Het model voorspelde hoe een zinkoxide-nanopyramide een eiwit onderbreekt dat bijdraagt aan het metabolisme in MRSA (methicilline-resistente Staphylococcus aureus), een veel voorkomende stam die antibioticaresistente infecties veroorzaakt. Krediet:Minjeong Cha en Emine Sumeyra Turali Emre, Kotov Lab
Met antibioticaresistente infecties in opkomst en een voortdurend veranderend pandemisch virus, is het gemakkelijk in te zien waarom onderzoekers kunstmatige nanodeeltjes willen kunnen ontwerpen die deze infecties kunnen stoppen.
Een nieuw machine learning-model dat interacties tussen nanodeeltjes en eiwitten voorspelt, ontwikkeld aan de Universiteit van Michigan, brengt ons een stap dichter bij die realiteit.
"We hebben nanodeeltjes opnieuw uitgevonden om meer te zijn dan alleen vehikels voor medicijnafgifte. We beschouwen ze als actieve medicijnen op zichzelf", zegt J. Scott VanEpps, assistent-professor spoedeisende geneeskunde en een auteur van de studie in Nature Computational Wetenschap .
Het ontdekken van medicijnen is een langzaam en onvoorspelbaar proces, daarom zijn zoveel antibiotica variaties op een eerder medicijn. Geneesmiddelenontwikkelaars willen medicijnen ontwerpen die bacteriën en virussen kunnen aanvallen op manieren die zij kiezen, gebruikmakend van de 'lock-and-key'-mechanismen die de interacties tussen biologische moleculen domineren. Maar het was onduidelijk hoe we konden overstappen van het abstracte idee om nanodeeltjes te gebruiken om infecties te verstoren naar de praktische implementatie van het concept.
"Door wiskundige methoden toe te passen op eiwit-eiwitinteracties, hebben we het ontwerp van nanodeeltjes gestroomlijnd die een van de eiwitten in deze paren nabootsen", zegt Nicholas Kotov, de Irving Langmuir Distinguished University Professor of Chemical Sciences and Engineering en corresponderende auteur van de studie .
"Nanodeeltjes zijn stabieler dan biomoleculen en kunnen leiden tot geheel nieuwe klassen van antibacteriële en antivirale middelen."
Het nieuwe machine learning-algoritme vergelijkt nanodeeltjes met eiwitten op drie verschillende manieren om ze te beschrijven. Terwijl de eerste een conventionele chemische beschrijving was, bleken de twee die betrekking hadden op de structuur het belangrijkst te zijn voor het maken van voorspellingen over de vraag of een nanodeeltje een lock-and-key match zou zijn met een specifiek eiwit.
Tussen hen vingen deze twee structurele beschrijvingen het complexe oppervlak van het eiwit en hoe het zichzelf zou kunnen herconfigureren om lock-and-key-passingen mogelijk te maken. Dit omvat zakken waar een nanodeeltje in zou kunnen passen, samen met de grootte die zo'n nanodeeltje zou moeten hebben. De beschrijvingen omvatten ook chiraliteit, een draaiing met de klok mee of tegen de klok in die belangrijk is om te voorspellen hoe een eiwit en nanodeeltje zal insluiten.
"Er zijn veel eiwitten binnen en buiten bacteriën waarop we ons kunnen richten. We kunnen dit model gebruiken als een eerste screening om te ontdekken welke nanodeeltjes met welke eiwitten zullen binden", zegt Emine Sumeyra Turali Emre, een postdoctoraal onderzoeker in chemische technologie en co-first auteur van het artikel, samen met Minjeong Cha, een Ph.D. student materiaalkunde en techniek.
Emre en Cha legden uit dat onderzoekers overeenkomsten die door hun algoritme zijn geïdentificeerd, kunnen opvolgen met meer gedetailleerde simulaties en experimenten. Een dergelijke match zou de verspreiding van MRSA, een veel voorkomende antibioticaresistente stam, kunnen stoppen met behulp van zinkoxide-nanopyramiden die metabolische enzymen in de bacteriën blokkeren.
"Machine learning-algoritmen zoals de onze zullen een ontwerptool bieden voor nanodeeltjes die in veel biologische processen kunnen worden gebruikt. Remming van het virus dat COVID-19 veroorzaakt, is een goed voorbeeld", zei Cha. "We kunnen dit algoritme gebruiken om efficiënt nanodeeltjes te ontwerpen die een breed-spectrum antivirale activiteit hebben tegen alle varianten."
Deze doorbraak werd mogelijk gemaakt door het Blue Sky Initiative van het U-M College of Engineering, dat ondersteuning bood aan het interdisciplinaire team dat de fundamentele verkenning uitvoerde van de vraag of een machine learning-aanpak effectief kan zijn wanneer gegevens over de biologische activiteit van nanodeeltjes zo schaars zijn.
"De kern van het Blue Sky-idee is precies wat dit werk omvat:een manier vinden om eiwitten en nanodeeltjes in een uniforme benadering weer te geven om nieuwe klassen medicijnen te begrijpen en te ontwerpen die meerdere manieren hebben om tegen bacteriën te werken", zegt Angela Violi, een Arthur F. Thurnau Professor, hoogleraar werktuigbouwkunde en leider van het nanobiotische Blue Sky-project.
Medewerkers van de University of California, Los Angeles hebben ook bijgedragen aan het machine learning-algoritme. + Verder verkennen
Nieuwe tool maakt ongekende modellering van magnetische nanodeeltjes mogelijk
 Insectenwerende middelen van de volgende generatie om door muggen overgedragen ziekten te bestrijden
Insectenwerende middelen van de volgende generatie om door muggen overgedragen ziekten te bestrijden Naar hoogwaardige mangaanoxidekatalysatoren met grote oppervlakten
Naar hoogwaardige mangaanoxidekatalysatoren met grote oppervlakten Onderzoekers creëren onmogelijke eiwitkooien van nanoformaat met behulp van goud
Onderzoekers creëren onmogelijke eiwitkooien van nanoformaat met behulp van goud Kation-geïnduceerde vormprogrammering en morphing in op eiwit gebaseerde hydrogels
Kation-geïnduceerde vormprogrammering en morphing in op eiwit gebaseerde hydrogels Wetenschappers leren meer over de eerste uren van de levensduur van lithium-ionbatterijen
Wetenschappers leren meer over de eerste uren van de levensduur van lithium-ionbatterijen
 Amerikaanse rechter verwerpt rechtszaken over klimaatverandering tegen grote olie
Amerikaanse rechter verwerpt rechtszaken over klimaatverandering tegen grote olie Giftige lucht verscheurt families in Mongolië
Giftige lucht verscheurt families in Mongolië Vliegenlarven bleken bij te dragen aan atmosferische methaanvervuiling
Vliegenlarven bleken bij te dragen aan atmosferische methaanvervuiling Voor een groenere toekomst, we moeten accepteren dat er niets inherent duurzaams is aan digitaal gaan
Voor een groenere toekomst, we moeten accepteren dat er niets inherent duurzaams is aan digitaal gaan Spanje, Portugal zet zich schrap voor natuurbranddreiging terwijl de uitzendkrachten stijgen
Spanje, Portugal zet zich schrap voor natuurbranddreiging terwijl de uitzendkrachten stijgen
Hoofdlijnen
- Deskundigen adviseren om benchmarking te gebruiken om bedrijven met een hoog antibioticagebruik te identificeren
- Supermensen creëren door middel van genmanipulatie en meer
- Decoderen hoe bacteriën met elkaar praten
- Wanneer en waar bossen beschermen
- Burgerwetenschap kan de betrokkenheid en het begrip bij niet-gegradueerde biologielessen vergroten
- Biologische experimenten op de gisting van gist
- Moleculaire mechanismen van paaigewoonten voor adaptieve straling van endemische Oost-Aziatische karperachtigen
- Cladistics: Definitie, methode en voorbeelden
- Hoe Rigor Mortis te onderscheiden van een Cadaveric Spasm
- Re-jigged kathode recept geeft nieuwe hoop aan solid-state batterijen voor elektrische voertuigen
- Spuiten van kleine gouddeeltjes kan mogelijk hartaandoeningen behandelen, suggereert onderzoek
- Laser-geactiveerde zijdeafdichtmiddelen presteren beter dan hechtingen voor weefselherstel
- Nanothermometrie om strategieën tegen kanker te verbeteren
- Kleine transporters kunnen behandeling bieden aan patiënten met een beroerte
 Nieuwe satellieten tonen verontrustend beeld van droogte en ijsverlies
Nieuwe satellieten tonen verontrustend beeld van droogte en ijsverlies Bewolkt met kans op straling:NASA bestudeert gesimuleerde straling
Bewolkt met kans op straling:NASA bestudeert gesimuleerde straling Hoe halen we energie uit aardgas?
Hoe halen we energie uit aardgas?  Brussels Airlines schort alle vluchten een maand op
Brussels Airlines schort alle vluchten een maand op Een percentage verdelen met een calculator
Een percentage verdelen met een calculator Een metaal dat zich gedraagt als water
Een metaal dat zich gedraagt als water Racisme te midden van de COVID-19-pandemie:een weg vooruit
Racisme te midden van de COVID-19-pandemie:een weg vooruit Hoe u een back-up kunt maken van het leven op aarde voorafgaand aan een doemscenario?
Hoe u een back-up kunt maken van het leven op aarde voorafgaand aan een doemscenario?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

