
Wetenschap
Volgende generatie patiëntavatars:uitbreiding van de mogelijkheden met micro-organosferen

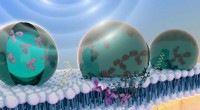
Afbeelding van micro-organosferen (MOS) die primaire weefselafgeleide cellen inkapselen voorafgaand aan demulgering. Credit:Terasaki Instituut voor Biomedische Innovatie
Een team van wetenschappers, geleid door Xiling Shen, Ph.D., Chief Scientific Officer en professor aan het Terasaki Institute for Biomedical Innovation (TIBI), heeft nieuwe niveaus bereikt in de ontwikkeling van patiëntmodellen. Ze hebben verbeterde methoden ontwikkeld voor het genereren van micro-organosferen (MOS) en hebben aangetoond dat deze MOS superieure mogelijkheden hebben voor een verscheidenheid aan klinische toepassingen. Zoals gedocumenteerd in een recente publicatie in Stamcelrapporten , kunnen hun MOS worden gebruikt als patiëntavatars voor onderzoeken met directe virale infectie, penetratie van immuuncellen en screening van therapeutische geneesmiddelen met hoge doorvoer, iets dat niet kan worden verkregen met conventionele patiënt-afgeleide modellen.
Het team van Dr. Shen heeft microfluïdische emulsietechnologie ontwikkeld voor het maken van MOS, dit zijn minuscule druppeltjes van basaalmembraanextract (BME) ter grootte van een nanoliter die zijn samengesteld uit weefselcelmengsels die in een snel tempo kunnen worden gegenereerd vanuit een geautomatiseerd apparaat. Nadat de druppeltjes zijn gemaakt, wordt overtollige olie verwijderd door een innovatief membraandemulgeringsproces, waardoor duizenden viskeuze druppeltjes van uniforme grootte achterblijven die kleine 3D-weefselstructuren bevatten.
Het team demonstreerde vervolgens unieke MOS-mogelijkheden en functies in verschillende eerste-van-hun-soort experimenten. Ze waren in staat om aan te tonen dat de MOS kon worden gemaakt uit een verscheidenheid aan verschillende weefselbronnen en de resulterende MOS had behoud van histopathologische morfologie, capaciteit voor differentiatie en genetische expressie, en het vermogen om te worden ingevroren en sub-gecultiveerd, zoals in conventionele organoïden .
Er werden experimenten uitgevoerd om het vermogen te testen om MOS met virussen te infecteren. In tegenstelling tot conventionele organoïden, kan MOS direct worden geïnfecteerd met virussen zonder de verwijdering en opschorting van cellen uit de omringende BME-steiger, waardoor het proces van virale infectie van het gastheerweefsel wordt herhaald. Het team van Dr. Shen was in staat om een MOS-atlas te maken van menselijke ademhalings- en spijsverteringsweefsels van autopsies van patiënten en deze te infecteren met SARS-COV-2-virussen, gevolgd door screening van geneesmiddelen om medicijnen te identificeren die virale infectie en replicatie binnen die weefsels blokkeren.
MOS biedt ook een uniek platform voor het bestuderen en ontwikkelen van immuunceltherapie. Binnen de natuurlijke diffusielimiet van gevasculariseerd weefsel, liet tumor-afgeleide MOS voldoende penetratie toe door therapeutische immuun-T-cellen zoals CAR-T, waardoor een nieuwe T-celpotentietest mogelijk werd om tumordoding door de gemanipuleerde T-cellen te beoordelen. Een dergelijk model zou zeer nuttig zijn bij het onderzoeken van de respons van tumoren en bij het ontwikkelen van anti-tumor immuunceltherapieën.
MOS zou verder kunnen worden geïntegreerd met diepgaande beeldvormingsanalyse voor snelle medicijntesten van kleine en heterogene klinische tumorbiopten. Bovendien was het algoritme in staat om onderscheid te maken tussen cytotoxische versus cytostatische medicijneffecten en medicijnresistente klonen die aanleiding zullen geven tot latere terugval. Dit baanbrekende vermogen zal de weg vrijmaken voor MOS die in de kliniek kan worden gebruikt om therapeutische beslissingen te nemen.
"Dr. Shen en zijn team blijven de MOS-technologie verfijnen en verbeteren en de veelzijdigheid ervan onder de aandacht brengen, niet alleen als een fysiologisch model voor het screenen van potentiële gepersonaliseerde behandelingen, maar ook voor ziektestudies en een verscheidenheid aan andere toepassingen," zei Ali Khademhosseini, Ph.D., directeur en CEO van TIBI. "Het lijkt de golf van de toekomst te zijn voor precisiegeneeskunde." + Verder verkennen
Van de patiënt afgeleide micro-organosferen maken geavanceerde precisie-oncologie mogelijk
 Wat is het resultaat van het toevoegen van loodnitraat aan kaliumjodide?
Wat is het resultaat van het toevoegen van loodnitraat aan kaliumjodide?  How is Helium Mined?
How is Helium Mined?  Nooit meer met vuur spelen:onderzoek biedt inzicht in veiligere oplaadbare batterijen
Nooit meer met vuur spelen:onderzoek biedt inzicht in veiligere oplaadbare batterijen Nieuwe nanosheetcoating kan niet-recyclebare gemetalliseerde films in voedselverpakkingen vervangen
Nieuwe nanosheetcoating kan niet-recyclebare gemetalliseerde films in voedselverpakkingen vervangen Samenwerking levert ontdekking van 12-zijdige silica kooien op
Samenwerking levert ontdekking van 12-zijdige silica kooien op
 Bezorgdheid over klimaatverandering niet beïnvloed door pandemie, studie toont
Bezorgdheid over klimaatverandering niet beïnvloed door pandemie, studie toont De natuur signaleert SOS - langetermijnonderzoek, extremen op korte termijn onthullen aanwijzingen om te overleven
De natuur signaleert SOS - langetermijnonderzoek, extremen op korte termijn onthullen aanwijzingen om te overleven Wat veroorzaakte de Dust Bowl?
Wat veroorzaakte de Dust Bowl?  Terugkijkend op een decennium:Satellietbeelden vertellen de verhalen
Terugkijkend op een decennium:Satellietbeelden vertellen de verhalen Het Zwarte Woud en klimaatverandering
Het Zwarte Woud en klimaatverandering
Hoofdlijnen
- Twee nieuwe Engelhardia-soorten van de walnootfamilie gemeld
- De terugkeer van wolven naar Oregon brengt conflicten en kansen
- Moleculaire markers onderzoeken de natuurlijke populatiestructuur en eigenschapgerelateerde loci van kiwibes
- Een 3D-model plantencel maken zonder voedsel
- Onderzoekers ontdekken de onverwachte atomaire structuur van koude- en mentholsensor TRPM8
- Hoe een moleculaire schaar op de juiste plaats knipt
- Make-up & Science Fair Ideas
- Wetenschappers hebben ontdekt welke genen onkambaar haarsyndroom veroorzaken
- Door het uitbreiden van het DNA-alfabet kunnen cellen nieuwe eiwitten produceren
- Kwantumstralers:meer dan kristalhelder tot puur enkelfoton

- Gedraagt zich als een spier, apparaat van nanoformaat tilt 165 keer zijn eigen gewicht op
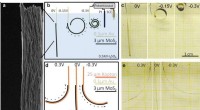
- Veelbelovende strategieën om de scheidingsselectiviteit van nanofiltratie te verbeteren

- Eiwitten gevangen in glas kunnen nieuwe medicinale ontwikkelingen opleveren

- Een nieuwe methode om therapieën precies in het lichaam af te leveren
 SLAP-microscoop breekt snelheidsrecords
SLAP-microscoop breekt snelheidsrecords Natuurkundigen benutten verwaarloosde eigenschappen van licht
Natuurkundigen benutten verwaarloosde eigenschappen van licht NASA-NOAA-satelliet vindt ontheemde kracht in tropische cycloon Kalmaegi
NASA-NOAA-satelliet vindt ontheemde kracht in tropische cycloon Kalmaegi Myanmar-onderneming probeert afval trendy te maken
Myanmar-onderneming probeert afval trendy te maken Gigantische intrinsieke chiraliteit van vlakke diëlektrische nanostructuren
Gigantische intrinsieke chiraliteit van vlakke diëlektrische nanostructuren Oude quids onthullen aanwijzingen over genetische voorouders van vroege bewoners van het Great Basin
Oude quids onthullen aanwijzingen over genetische voorouders van vroege bewoners van het Great Basin Hoe zijn planten en dieren afhankelijk van elkaar?
Hoe zijn planten en dieren afhankelijk van elkaar?  Ik stop ermee:hoe slechte behandeling door klanten leidt tot een hoog verloop in de dienstverlenende sector
Ik stop ermee:hoe slechte behandeling door klanten leidt tot een hoog verloop in de dienstverlenende sector
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

