
Wetenschap
Nanobiomateriaal stimuleert neuronale groei bij muizen met ruggenmergletsel
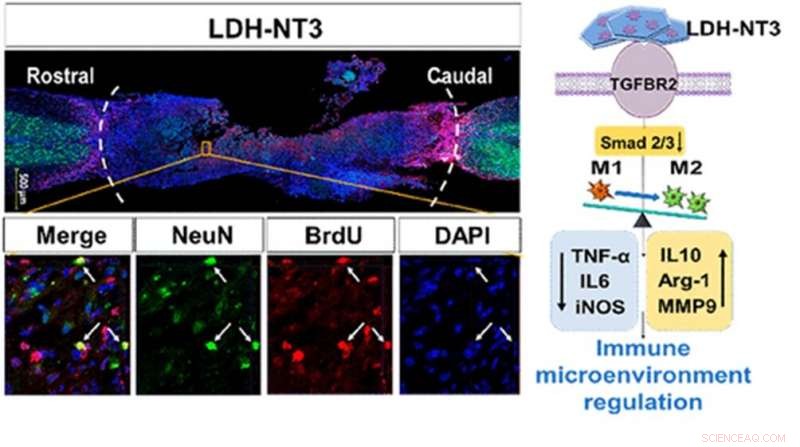
Onderzoekers van de afdeling Orthopedie van het Tongji-ziekenhuis hebben met succes een nanobiomateriaal genaamd gelaagd dubbel hydroxide (LDH) gebruikt om de inflammatoire omgeving rond ruggenmergletsels bij muizen te remmen, versnellende regeneratie van neuronen en reconstructie van het neurale circuit in de wervelkolom. Krediet:Liming Cheng, Rongrong Zhu, Afdeling Orthopedie, Tongji-ziekenhuis van de Tongji-universiteit
Onderzoekers van de afdeling Orthopedie van het Tongji-ziekenhuis aan de Tongji-universiteit in Shanghai hebben met succes een nanobiomateriaal genaamd gelaagd dubbel hydroxide (LDH) gebruikt om de inflammatoire omgeving rond ruggenmergletsels bij muizen te remmen, versnellende regeneratie van neuronen en reconstructie van het neurale circuit in de wervelkolom. De onderzoekers konden ook het onderliggende genetische mechanisme identificeren waarmee LDH werkt. Dit begrip zou een verdere aanpassing van de therapie mogelijk moeten maken die, in combinatie met andere elementen, kon eindelijk een alomvattende, klinisch toepasbaar systeem voor verlichting van ruggenmergletsel bij mensen.
Het onderzoek verscheen in het tijdschrift American Chemical Society ACS Nano op 2 februari.
Er is geen effectieve behandeling voor ruggenmergletsels, die altijd gepaard gaan met het afsterven van neuronen, breuk van axonen of zenuwvezels, en ontsteking. Ook al blijft het lichaam nieuwe neurale stamcellen aanmaken, deze inflammatoire micro-omgeving (de onmiddellijke, kleinschalige omstandigheden op de plaats van de verwonding) belemmert de regeneratie van neuronen en axonen ernstig. Nog steeds slechter, de langdurige activering van immuuncellen in dit gebied resulteert ook in secundaire laesies van het zenuwstelsel, op hun beurt voorkomen dat de stamcellen zich differentiëren tot nieuwe celtypen.
Als deze agressieve immuunrespons op de plaats van de verwonding kan worden gematigd, er is de mogelijkheid dat neurale stamcellen differentiatie kunnen beginnen en neurale regeneratie zou kunnen optreden.
In recente jaren, een reeks nieuwe biomaterialen op nanoschaal - natuurlijke of synthetische materialen die interageren met biologische systemen - zijn ontworpen om de activering van neurale stamcellen te ondersteunen, samen met hun mobilisatie en differentiatie. Sommige van deze "nanocomposieten" zijn in staat medicijnen af te geven op de plaats van de verwonding en de neuronale regeneratie te versnellen. Deze nanocomposieten zijn vooral aantrekkelijk voor de behandeling van het ruggenmerg vanwege hun lage toxiciteit. Echter, weinigen hebben enig vermogen om de immuunreactie ter plaatse te remmen of te matigen, en pak zo het onderliggende probleem niet aan. Bovendien, de onderliggende mechanismen van hoe ze werken blijft onduidelijk.
Nanogelaagd dubbel hydroxide (LDH) is een soort klei met veel interessante biologische eigenschappen die relevant zijn voor ruggenmergletsels, inclusief goede biocompatibiliteit (vermogen om afstoting door het lichaam te voorkomen), veilige biologische afbraak (afbraak en verwijdering van de moleculen na toepassing), en uitstekend ontstekingsremmend vermogen. LDH is al uitgebreid onderzocht in de biomedische technologie met betrekking tot de regulering van de immuunrespons, maar vooral op het gebied van antitumortherapie.
"Deze eigenschappen maakten van LDH een echt veelbelovende kandidaat voor het creëren van een veel gunstiger micro-omgeving voor het herstel van ruggenmergletsel, " zegt Rongrong Zhu van de afdeling Orthopedie van het Tongji-ziekenhuis, eerste auteur van de studie.
Onder leiding van Liming Cheng, corresponderende auteur van de studie, het onderzoeksteam transplanteerde de LDH in de verwondingsplaats van muizen, en ontdekte dat het nanobiomateriaal de migratie van neurale stamcellen aanzienlijk had versneld, neurale differentiatie, activering van kanalen voor neuronexcitatie, en inductie van actiepotentiaal (zenuwimpuls) activering. De muizen vertoonden ook een significant verbeterd locomotiefgedrag in vergelijking met de controlegroep muizen. In aanvulling, wanneer de LDH werd gecombineerd met Neurotrophin-3 (NT3), een eiwit dat de groei en differentiatie van nieuwe neuronen stimuleert, de muizen genoten zelfs betere hersteleffecten dan de LDH alleen. In essentie, de NT3 stimuleert de neuronale ontwikkeling, terwijl de LDH een omgeving creëert waar die ontwikkeling kan gedijen.
Vervolgens, via transcriptionele profilering, of analyse van genexpressie van duizenden genen tegelijk, de onderzoekers konden achterhalen hoe de LDH haar hulpverlening uitvoert. Ze ontdekten dat als LDH eenmaal aan celmembranen is gehecht, het veroorzaakt een grotere activering van het "transforming growth factor-β receptor 2" (TGFBR2) gen, afnemende productie van de witte bloedcellen die ontstekingen versterken en toenemende productie van witte bloedcellen die ontstekingen remmen. Bij toepassing van een chemische stof die TGFBR2 remt ze ontdekten dat de gunstige effecten waren omgekeerd.
Het begrip van hoe LDH deze effecten uitvoert, zou de onderzoekers nu in staat moeten stellen de therapie aan te passen om de prestaties te verbeteren en uiteindelijk een uitgebreid therapeutisch systeem voor ruggenmergletsels te creëren - door deze biomaterialen te combineren met neurotrofe factoren zoals NT3- die kunnen worden gebruikt in klinische toepassingen op mensen.
 Terwijl een watercrisis opdoemt in Kaapstad, zou het in Canada kunnen gebeuren?
Terwijl een watercrisis opdoemt in Kaapstad, zou het in Canada kunnen gebeuren? De Oostzee als tijdmachine
De Oostzee als tijdmachine Robotachtige afdaling naar een bevroren onderwereld
Robotachtige afdaling naar een bevroren onderwereld Nieuwe definitie van duurzaamheid overwint tekortkoming die wereldwijde transformatie-inspanningen belemmert
Nieuwe definitie van duurzaamheid overwint tekortkoming die wereldwijde transformatie-inspanningen belemmert Community helpt wetenschappers rookvoorspellingen te evalueren
Community helpt wetenschappers rookvoorspellingen te evalueren
Hoofdlijnen
- Chili vecht om een favoriete mossel te redden
- Hoe maak je een modelhart met materialen uit je thuis
- Onderzoekers demonstreren een technische benadering om medicijnen te combineren, controle parasitaire wormen
- Intron: definitie, functie en belang bij RNA-splitsing
- Waarom insecten zich kunnen ontwikkelen uit onbevruchte eicellen
- Darmbacteriën van wilde muizen stimuleren de gezondheid van laboratoriummuizen
- Een enzym dat de vorming van het DNA katalyseert Molecuul
- Lood visgerei kan een bedreiging vormen voor de populaties van duikers
- nieuwe ontdekking, meer bijen markeren Michigans eerst, volledige bijentelling
- Wetenschappers lossen mysterie op van kleurrijke nanobuisjes in fauteuils

- Technologie kan DNA-sequencing op zijn kop zetten voor het diagnosticeren van bepaalde DNA-mutaties

- Absoluut idee voor on-demand nanopatronen

- Eenvoudige grafeencascade biedt ongekende inzichten in nano-ionen

- Shape-shifting engineered nanodeeltjes voor het afleveren van kankermedicijnen aan tumoren

 Onderzoekers voeren eerste wereldwijde beoordeling uit van de uitstoot van broeikasgassen in de levenscyclus van kunststoffen
Onderzoekers voeren eerste wereldwijde beoordeling uit van de uitstoot van broeikasgassen in de levenscyclus van kunststoffen The Mathematikado:een op wiskunde geïnspireerde parodie op een parodie
The Mathematikado:een op wiskunde geïnspireerde parodie op een parodie Menselijke toepassingen voor diatomeeën
Menselijke toepassingen voor diatomeeën Onderzoekers realiseren halfmetalliciteit in antiferromagneten van het A-type met ferro-elektrische controle
Onderzoekers realiseren halfmetalliciteit in antiferromagneten van het A-type met ferro-elektrische controle SpaceX onthult nieuwe Falcon Heavy-raket voor lancering in januari
SpaceX onthult nieuwe Falcon Heavy-raket voor lancering in januari Indonesië annuleert tsunami-alarm na sterke aardbeving
Indonesië annuleert tsunami-alarm na sterke aardbeving Hoe forensische laboratoriumtechnieken werken
Hoe forensische laboratoriumtechnieken werken  Onderzoekers beginnen met testen van veelbelovend nieuw nanomateriaal voor waterstofopslag
Onderzoekers beginnen met testen van veelbelovend nieuw nanomateriaal voor waterstofopslag
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

