
Wetenschap
Nanocontainer brengt gentherapieën en medicijnen ter grootte van titaan in cellen
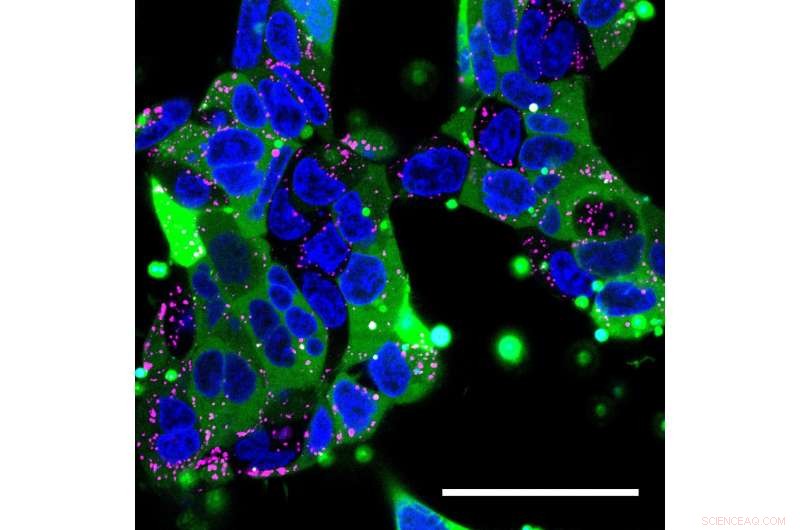
Confocale microscopie opname van menselijke embryonale niercellen. Nanodeeltjes gevuld met humaan immunoglobuline werden aan de cellen afgeleverd. De celkern is blauw, endosomen (die materialen vastleggen die door cellen worden opgenomen) zijn gelabeld in roze, en de immunoglobuline-eiwitten zijn gelabeld met een groen fluorescerend label. De lading van het nanodeeltje heeft zich wijd verspreid door de meeste cellen (groen) zonder dat het vastzit in endosomen. Krediet:Yuan Rui, Johns Hopkins Medicine
Wetenschappers van Johns Hopkins Medicine melden dat ze een kleine, container van nanoformaat die in cellen kan glippen en op eiwitten gebaseerde medicijnen en gentherapieën van elke omvang kan leveren - zelfs forse die zijn gekoppeld aan de genbewerkingstool genaamd CRISPR. Als hun creatie - gemaakt van een biologisch afbreekbaar polymeer - meer laboratoriumtests doorstaat, het zou een manier kunnen zijn om grotere medische verbindingen efficiënt naar specifiek geselecteerde doelcellen te vervoeren.
Een verslag over hun werk verschijnt in het nummer van 6 december van: wetenschappelijke vooruitgang .
"De meeste medicijnen verspreiden zich op willekeurige wijze door het lichaam en richten zich niet op een specifieke cel, " zegt biomedisch ingenieur Jordan Green, doctoraat, leider van het onderzoeksteam. "Sommige medicijnen, zoals antistoffen, vastklampen aan doelen op de celoppervlakreceptoren, maar we hebben geen goede systemen om biologische medicijnen rechtstreeks naar de binnenkant van een cel te brengen, dat is waar therapieën de beste kans hebben om goed te werken en met minder bijwerkingen."
Veel academische en commerciële wetenschappers hebben lang gezocht naar betere transitsystemen voor therapieën, zegt Groen, hoogleraar biomedische technologie, oogheelkunde, oncologie, neurochirurgie, materiaalkunde en techniek, en chemische en biomoleculaire engineering aan de Johns Hopkins University School of Medicine, en lid van het Bloomberg-Kimmel Institute for Cancer Immunotherapy in Johns Hopkins.
Sommige in de handel verkrijgbare technieken gebruiken uitgeklede vormen van virussen - bekend om hun vermogen om cellen rechtstreeks te 'infecteren' - om therapieën af te leveren, hoewel de niet-infectieuze versies van deze toedieningssystemen een ongewenste reactie van het immuunsysteem kunnen ontketenen. Andere therapieën gericht op zieke bloedcellen, bijvoorbeeld, zijn omslachtiger, waarbij het bloed van de patiënt moet worden verwijderd, vervolgens gezapt met een elektrische stroom die poriën in het celmembraan opent om toegang te krijgen.
De container van nanoformaat die Green en zijn team bij Johns Hopkins hebben ontwikkeld, ontleent een idee aan de eigenschappen van virussen, waarvan vele bijna bolvormig zijn en zowel negatieve als positieve ladingen dragen. Met een meer neutrale totale lading, virussen kunnen dicht bij cellen komen. Dat is bij veel biologische medicijnen niet het geval, die bestaan uit sterk geladen, grote eiwitten en nucleïnezuren die de neiging hebben om cellen af te stoten.
Om dit te overwinnen, afgestudeerde student Yuan Rui ontwikkelde een nieuw biologisch afbreekbaar polymeermateriaal. Polymeer is de algemene term voor een stof die uit vele moleculen bestaat. Om het polymeer te maken, Rui aan elkaar geregen - zoals de takken van een boom - vier componenten moleculen die, overuren, afbreken en oplossen in water. De moleculen bevatten zowel positieve als negatieve ladingen.
Met een balans van positieve en negatieve ladingen, de moleculen duwen en trekken volgens hun lading en hun waterstofatomen binden zich met een biologische therapie in de buurt. Het resultaat is een nanostructuur met daarin de biologische therapie.
De positieve ladingen van de container van nanoformaat interageren met het membraan van een cel, en de container is verzwolgen in een cellulair pakket dat een endosoom wordt genoemd.
Eenmaal binnen, de container van nanoformaat breekt het endosoom open, en de polymeren worden afgebroken, het medicijn in de cel laten werken.
Om hun uitvinding te testen, Rui maakte een nanocontainer van een klein eiwit en voerde dat aan muizenniercellen in kweekschalen. Ze bevestigde een groen fluorescerend label aan het kleine eiwit en zag felgroene spatten door de meeste cellen, wat aangeeft dat het eiwit met succes is afgeleverd.
Vervolgens, Rui verpakte een groter eiwit:humaan immunoglobuline, een therapie die doorgaans wordt gebruikt om het immuunsysteem te versterken en een model voor antilichaamtherapieën. Deze keer, ze ontdekte dat 90% van de niercellen die ze behandelde oplichtte met het groene fluorescerende label dat aan het immunoglobuline was bevestigd.
"Als nanodeeltjes een cel binnenkomen, ze worden vaak opgesloten in endosomen, die de inhoud degraderen, maar onze experimenten laten zien dat de eiwitpakketten gelijkmatig over de meeste cellen waren verspreid en niet vastzaten in de endosomen, ' zegt Rui.
Voor een nog grotere uitdaging, Rui creëerde een nanopakket met een op CRISPR gebaseerd eiwit- en nucleïnezuurcomplex dat een groen fluorescentiesignaal kan uitschakelen of de cellen rood kan laten gloeien wanneer de CRISPR-verbinding een deel van het genoom van een cel doorsnijdt. De onderzoekers zagen dat de genbewerking om een gen uit te schakelen werkte in tot 77% van de cellen die in het laboratorium werden gekweekt en om een gen toe te voegen of te repareren in ongeveer 4% van de cellen.
"Dat is behoorlijk effectief gezien, met andere genbewerkingssystemen, u zou in minder dan 10 procent van de gevallen het juiste gen-cutting-resultaat kunnen krijgen, ", zei Rui. Op CRISPR gebaseerde therapieën hebben het potentieel om medicijnen veel nauwkeuriger te maken met hun vermogen om genetische gebreken die bijdragen aan ziekte precies aan te pakken. Sommige CRISPR-therapieën worden getest in klinische onderzoeken.
In een laatste experiment, Rui en haar collega's implanteerden hersenkankercellen in de hersenen van muizen. Ze injecteerde de nanocontainers met componenten voor genbewerking rechtstreeks in de muizenhersenen en analyseerde hun cellen op een rode gloed die op succesvolle genbewerking wijst. Ze vond hersenkankercellen die enkele millimeters rood gloeiden van waar ze ze had geïnjecteerd.
'Toen ik vijf jaar geleden voor het eerst aan dit project begon, wetenschappers dachten niet dat je iets anders dan een virus kon gebruiken om deze therapieën in cellen af te leveren, ", zegt Rui. "Het ontwikkelen van nieuwe technologieën kan ons helpen meer te begrijpen over ziekte, maar ook meer over het maken van nieuwe medicijnen."
Rui en Green proberen de nanocontainers stabieler te maken, zodat ze in de bloedbaan kunnen worden geïnjecteerd en gericht op cellen met bepaalde genetische handtekeningen.
De wetenschappers vragen patenten aan die verband houden met dit werk.
 Team bepaalt eerste structuur met hoge resolutie van dopaminereceptor
Team bepaalt eerste structuur met hoge resolutie van dopaminereceptor Onderzoekers ontwikkelen nieuwe moleculaire ferro-elektrische metamaterialen
Onderzoekers ontwikkelen nieuwe moleculaire ferro-elektrische metamaterialen Wat zijn de reactanten in gisting?
Wat zijn de reactanten in gisting?  Wat zijn waarheidsgetuigingen over een verbinding?
Wat zijn waarheidsgetuigingen over een verbinding?  Moleculaire chirurgie hervormt levend weefsel met elektriciteit maar zonder incisies
Moleculaire chirurgie hervormt levend weefsel met elektriciteit maar zonder incisies
 Indonesië verhoogt alarmniveau voor vulkaan Bali
Indonesië verhoogt alarmniveau voor vulkaan Bali Opnieuw ontwaakte geiser voorspelt geen vulkaanuitbarstingen van Yellowstone, studie toont
Opnieuw ontwaakte geiser voorspelt geen vulkaanuitbarstingen van Yellowstone, studie toont Onderzoek naar de impact van klimaatverandering op energiesystemen op zowel mondiale als regionale schaal
Onderzoek naar de impact van klimaatverandering op energiesystemen op zowel mondiale als regionale schaal Niet aanpassen aan klimaatverandering kost waarschijnlijk minstens vijf keer meer
Niet aanpassen aan klimaatverandering kost waarschijnlijk minstens vijf keer meer Animal Adaptations to Hot Climates
Animal Adaptations to Hot Climates
Hoofdlijnen
- DNA-bewijs zet neushoornstropers achter tralies, studie toont
- Hoe biologie te integreren met chemie en natuurkunde
- Draadtap op het dak is bedoeld om te leren waar kraaien over roddelen in de schemering
- Kerkuilen blijken geen gehoorverlies te hebben naarmate ze ouder worden
- Wat is celcompartimentering en waarom doet het zich voor?
- De voordelen van het gebruik van Sticky End Enzymen
- 7 soorten bindweefsel
- Menselijk genoom DNA-sequentietypen
- Om nieuwe enzymen voor biobrandstoffen te vinden, het kan een microbieel dorp vergen
- Diverse amyloïde structuren en dynamiek onthuld door snelle atoomkrachtmicroscopie
- 3D-printexperts ontdekken hoe ze de technologie van morgen kunnen maken met behulp van inkjet-geprint grafeen

- Ingenieurs van Yale ontwikkelen nieuw type mechanisch geheugen

- Verbetering van de elektrische en mechanische eigenschappen van op koolstof-nanobuis gebaseerde vezels

- Sommige nanodeeltjes die vaak aan consumentenproducten worden toegevoegd, kunnen DNA aanzienlijk beschadigen

 10 manieren waarop de aarde je probeert te vermoorden
10 manieren waarop de aarde je probeert te vermoorden  Kleine korrels kunnen helpen om schone en overvloedige fusiekracht naar de aarde te brengen
Kleine korrels kunnen helpen om schone en overvloedige fusiekracht naar de aarde te brengen Tandenhangers spreken van de prominente status van de eland in het stenen tijdperk
Tandenhangers spreken van de prominente status van de eland in het stenen tijdperk Onderzoekers ontwikkelen nieuwe methode om nanodevices te controleren
Onderzoekers ontwikkelen nieuwe methode om nanodevices te controleren Norwegian Air Shuttle eist Boeing betaling voor aan de grond houden van 737 MAX-vliegtuigen
Norwegian Air Shuttle eist Boeing betaling voor aan de grond houden van 737 MAX-vliegtuigen Grote exponenten oplossen
Grote exponenten oplossen  DeepEyedentification:mensen identificeren op basis van micro-oogbewegingen
DeepEyedentification:mensen identificeren op basis van micro-oogbewegingen Mona Lisa-gast op tv? Onderzoekers werken pratende hoofden uit foto's, kunst
Mona Lisa-gast op tv? Onderzoekers werken pratende hoofden uit foto's, kunst
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- Italian | Spanish | Portuguese | German | Dutch | Danish | Norway | French | Swedish |

-
Wetenschap © https://nl.scienceaq.com

