Wetenschap
Onderzoekers ontdekken waarom niet-containers voor medicijnafgifte vaak mislukken
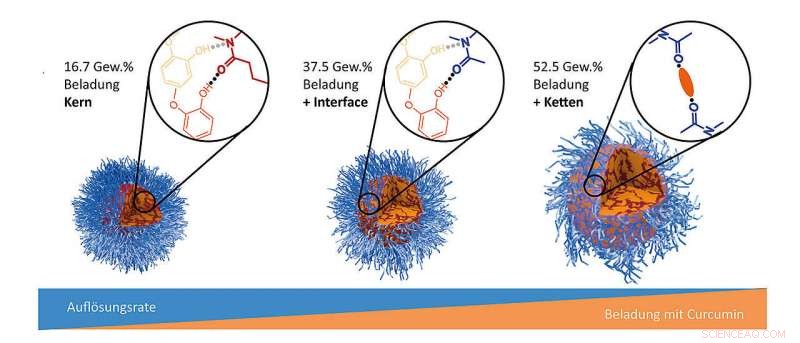
Naarmate de belading met curcumine (geel) toeneemt, de oplossnelheid van de containers gemaakt van polymere micellen (blauw) neemt af. Krediet:Ann-Christin Pöppler / Universität Würzburg
Nanocapsules en andere containers kunnen medicijnen rechtstreeks door het lichaam van een patiënt transporteren naar de oorsprong van de ziekte en ze daar gecontroleerd vrijgeven. Dergelijke geavanceerde systemen worden af en toe gebruikt bij kankertherapie. Omdat ze heel specifiek werken, ze hebben minder bijwerkingen dan medicijnen die door het hele organisme worden verspreid.
Deze methode staat in de wetenschap bekend als medicijnafgifte. Chemie Professor Ann-Christin Pöppler van Julius-Maximilians-Universität (JMU) Würzburg in Beieren, Duitsland, is ervan overtuigd dat deze methode nog een groot ontwikkelingspotentieel heeft. Ze analyseert de moleculaire capsules die medicijnen als een container omsluiten en transporteren naar de plaats van actie:"Mijn fractie wil zo gedetailleerd mogelijk begrijpen hoe de containermoleculen en de actieve stoffen rangschikken en welke eigenschappen daaruit voortvloeien, " ze zegt.
Polymere micellen als onderzoeksobject
De junior professor doet vooral onderzoek naar polymere micellen. Deze bestaan uit vele ketens van moleculen, die samenkomen in bolvormige structuren. Dergelijke micellen zijn al op de markt als medicijncontainers. Ze worden gebruikt bij kankertherapieën en in cosmetische producten zoals lotions voor het verwijderen van make-up. Wanneer ze in contact komen met vetoplosbare stoffen, ze schikken zich op hun oppervlak en omringen ze aan het einde als een vacht. Dit vormt een container met een "waterminnende" buitenschil en een "vetminnende" kern.
"Er is weinig bekend over de moleculaire oorsprong van de eigenschappen van deze structuren, " zegt Pöppler. In het wetenschappelijke tijdschrift Angewandte Chemie , de onderzoeker en co-auteurs van JMU beschreven onlangs een effect dat belangrijk is voor het ontwerp van toekomstige medicijnafgiftesystemen:als toenemende hoeveelheden actieve ingrediënten in de polymere micellen worden verpakt, hun ontbinding lijdt - de afgifte van de actieve ingrediënten wordt dan steeds moeilijker.
Actieve ingrediënten lijmen de micellen aan elkaar
Het onderzoeksteam van Würzburg vond de reden voor de afnemende oplosbaarheid door een reeks verschillende experimenten:naarmate de container meer en meer wordt geladen, de werkzame stoffen bezinken niet meer uitsluitend in de kern maar ook op het containeroppervlak. Daar kunnen ze de afzonderlijke micellaire haren bijna aan elkaar lijmen. Deze moleculaire interacties verminderen de oplosbaarheid van de gehele structuur.
Volgende, het team hoopt uit te vinden of het oplossen van de container kan worden verbeterd door structurele veranderingen aan de micellen. Een van de doelen van medicijnafgifte is ervoor te zorgen dat een container zoveel mogelijk werkzame stof opneemt en zo goed mogelijk oplost in het lichaam.
Polymeerchemie en farmacie betrokken
Ann-Christin Pöppler werkte bij dit werk samen met twee andere JMU-groepen. De polymere micellen werden geproduceerd door Robert Luxenhofer, Hoogleraar Polymere Functionele Materialen. De oplostesten werden uitgevoerd in het team van professor Lorenz Meinel, hoofd van de leerstoel Farmaceutische Technologie en Biofysica.
De gebruikte polymere micellen waren verbindingen uit de stofklassen poly(2-oxazoline)s en poly(2-oxazine)s. Curcumine werd gebruikt als model voor een werkzame stof omdat dit ingrediënt van kurkuma, een kruidenplant, is heel gemakkelijk spectroscopisch te visualiseren. De structuren van de containers geladen met verschillende hoeveelheden curcumine werden bepaald door middel van NMR-spectroscopie in vaste toestand en andere analytische methoden.
 Nieuwe 3D-geprinte technologie verlaagt de kosten van algemene medische tests
Nieuwe 3D-geprinte technologie verlaagt de kosten van algemene medische tests Nieuwe vloeistofmodelleringstechniek voorspelt chemische reacties en verlaagt de ontwikkelingskosten van geneesmiddelen
Nieuwe vloeistofmodelleringstechniek voorspelt chemische reacties en verlaagt de ontwikkelingskosten van geneesmiddelen Conductometrische titratietheorie
Conductometrische titratietheorie  Sensoren ontwerpen om vreemde lichamen in voedsel te detecteren
Sensoren ontwerpen om vreemde lichamen in voedsel te detecteren Een superresolutieweergave van chemische reacties
Een superresolutieweergave van chemische reacties
 Onderzoekers ontdekken 2 nieuwe niet-inheemse soorten in Grote Meren
Onderzoekers ontdekken 2 nieuwe niet-inheemse soorten in Grote Meren Evacueren onder verschrikkelijke natuurbrandscenario's
Evacueren onder verschrikkelijke natuurbrandscenario's Water zorgt voor explosieve uitbarstingen:Magma is natter dan we dachten
Water zorgt voor explosieve uitbarstingen:Magma is natter dan we dachten Colorado River Delta-rapport biedt routekaart voor herstel
Colorado River Delta-rapport biedt routekaart voor herstel Nieuwe schatting van oceaanwarmte vindt meer opwarming
Nieuwe schatting van oceaanwarmte vindt meer opwarming
Hoofdlijnen
- Studie biedt gedetailleerd inzicht in het vroege leven van grijze zeehondenpups op zee
- Cavendish redden:team kweekt 's werelds eerste ziekteresistente bananen in Panama
- Vooruitgang bereikt in droge conservering van spermacellen van zoogdieren
- Aminozuren: functie, structuur, typen
- Het verschil tussen hoe interne en externe regulatoren werken
- Zeldzame zangvogel heeft misschien nooit bestaan
- Fysieke aanpassingen van rondwormen
- Een diercel-diagram maken
- Typen biologie-experimenten
 Empowerment van vrouwen kan helpen de klimaatverandering aan te pakken
Empowerment van vrouwen kan helpen de klimaatverandering aan te pakken Quantum dots met ingebouwde lading verhogen de efficiëntie van zonnecellen met 50%
Quantum dots met ingebouwde lading verhogen de efficiëntie van zonnecellen met 50% Onderzoekers ontdekken dat klimaatverandering het risico op kwikverontreiniging verhoogt
Onderzoekers ontdekken dat klimaatverandering het risico op kwikverontreiniging verhoogt Stamboom van Homo Sapiens blijft evolueren
Stamboom van Homo Sapiens blijft evolueren  Onderzoekers tonen pad naar emissievrije LA
Onderzoekers tonen pad naar emissievrije LA Hoe Tienden te Omzetten in Honderdste punten
Hoe Tienden te Omzetten in Honderdste punten Hoe correlatie te berekenen
Hoe correlatie te berekenen X-Ray Vision:plastic mengsels van binnen en van buiten zien
X-Ray Vision:plastic mengsels van binnen en van buiten zien
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Spanish | Portuguese | Swedish | German | Dutch | Danish | Italian | Norway |

-
Wetenschap © https://nl.scienceaq.com