Wetenschap
Laaggedoseerde bestralingstherapie verbetert de afgifte van therapeutische nanodeeltjes aan hersentumoren
Een nieuwe studie onder leiding van onderzoekers van het Massachusetts General Hospital (MGH) stelt vast dat bestralingstherapie de opname van therapeutische nanodeeltjes door glioblastomen kan verhogen, het verhogen van de mogelijkheid om zowel op groeifactor gerichte als op het immuunsysteem gebaseerde therapieën te gebruiken tegen de dodelijke hersentumor. Het team beschrijft hoe voorbehandeling met laaggedoseerde straling de afgifte aan tumoren van nanodeeltjes die kleine interfererende RNA (siRNA) -moleculen bevatten, verhoogde en de overleving in een muismodel van glioblastoma aanzienlijk verbeterde.
"We ontdekten dat bestralingstherapie hersentumoren stimuleert voor een betere opname van nanotherapeutica, waardoor we een gericht nanodeeltje kunnen ontwikkelen om siRNA's te leveren voor zowel immuuncontrolepunten als gerichte therapie tegen het meest agressieve type hersentumor, " zegt Bakhos Tannous, doctoraat, van de afdeling Neuro-Oncologie van de afdeling Neurologie van MGH, senior auteur van het rapport gepubliceerd in ACS Nano . "Een korte uitbarsting van straling was in staat om de opname van het nanodeeltje te vervijfvoudigen, het versterken van de effecten van gerichte therapie, het activeren van de immuunrespons op de plaats van de tumor en het verlengen van de overleving."
Terwijl tot 60 procent van de glioblastomen de EGFR-groeifactor tot expressie brengen, een molecuul dat wordt gebruikt in gerichte therapieën tegen verschillende soorten kanker, EGFR-gerichte therapieën hebben weinig succes gehad tegen de hersentumoren. Evenzo hebben immuuntherapieën gericht tegen immuuncontrolepunten zoals CTLA-4 en PD-L1 veelbelovende resultaten tegen veel kankers, maar nog niet tegen glioblastoom. Sommige onderzoeken hebben een verband gesuggereerd tussen EGFR-activering en verhoogde PD-L1-expressie, het verhogen van de mogelijkheid dat gerichte beide de antitumoreffecten zouden kunnen vergroten.
Om siRNA's af te leveren die gericht zijn op zowel EGFR als PD-L1 aan hersentumoren, de onderzoekers ontwikkelden een vast lipide nanodeeltje geleid door een tumor-targeting peptide genaamd iRGD, die zich bindt aan een molecuul dat aanwezig is op bloedvaten die de tumor bekleden, waardoor het zowel de bloed-hersenbarrière als de bloedtumorbarrière kan penetreren. Factoren zoals de kleine omvang en positieve lading van dit nanodeeltje zorgen ervoor dat het door de bloed-hersenbarrière kan dringen; en net als andere vaste lipidenanodeeltjes, zijn lage kosten, stabiliteit, biologische afbreekbaarheid en gemakkelijke fabricage maken het een aantrekkelijke optie, legt Gulsah Erel-Akba uit, doctoraat, van MGH Neuro-Oncology en Izmir Katip Celebi University in Turkije, de eerste auteur van de studie.
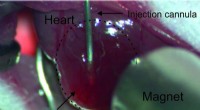
Om te testen of voorbehandeling met laaggedoseerde bestralingstherapie de therapeutische effectiviteit van het nanodeeltje zou vergroten, de onderzoekers vergeleken de resultaten van vier strategieën bij glioomdragende muizen.
- Behandeling met alleen bestraling of met een nanodeeltje met daarin een 'gecodeerd' siRNA-molecuul had geen effect op de tumorgroei of de overleving van de muizen.
- Het toedienen van een iRGD-geleid nanodeeltje met EGFR/PD-L1-targeting siRNA's zonder voorbehandeling door bestraling had een matig effect op de tumorgroei en verhoogde de overleving van 21 tot 24 dagen.
- Stralingsvoorbehandeling plus een siRNA-dragend nanodeeltje zonder een effectief leidend peptide had ook een matig effect op zowel tumorgroei als overleving.
- Stralingsvoorbehandeling plus een iRGD-geleid nanodeeltje dat de EGFR/PD-L1-targeting siRNA's draagt, had het grootste voordeel, overleving verhogen tot 38 dagen.
Onderzoek van weefsel van de tumorlocaties wees uit dat de gecombineerde therapie de expressie van PD-L1 verminderde en de rekrutering van CD8 T-cellen verhoogde, wijst op een verhoogde antitumor immuunrespons.
Een universitair hoofddocent Neurologie aan de Harvard Medical School, Tannous legt uit dat het bekend is dat straling de immunosuppressieve micro-omgeving van glioblastoom op verschillende manieren tegengaat, suggereert een dubbele werking van zowel het verhogen van de afgifte van nanodeeltjes als het verbeteren van de antitumor-immuunrespons. Hoewel aspecten zoals de optimale dosis en timing van de bestralingsvoorbehandeling nog moeten worden bepaald, hij merkt op, dezelfde benadering zou kunnen worden gebruikt om andere agressieve tumoren te behandelen met siRNA's die zich richten op verschillende moleculaire routes.
 Onderzoekers koppelen weesreceptor aan opioïde-geïnduceerde jeuk
Onderzoekers koppelen weesreceptor aan opioïde-geïnduceerde jeuk Ondersteunde vloeibare metaalkatalysatoren - een nieuwe generatie reactieversnellers
Ondersteunde vloeibare metaalkatalysatoren - een nieuwe generatie reactieversnellers Nieuwe stoffenbibliotheek om het zoeken naar actieve stoffen te versnellen
Nieuwe stoffenbibliotheek om het zoeken naar actieve stoffen te versnellen Hoe Calorimeter Constant te berekenen
Hoe Calorimeter Constant te berekenen Intermoleculaire krachten in de structuur van propaan
Intermoleculaire krachten in de structuur van propaan
 Ontbrekende schakel in algenfotosynthese gevonden, biedt de mogelijkheid om de gewasopbrengst te verbeteren
Ontbrekende schakel in algenfotosynthese gevonden, biedt de mogelijkheid om de gewasopbrengst te verbeteren NASA onderzoekt mogelijke tropische of subtropische storm die de Golfstaten treft
NASA onderzoekt mogelijke tropische of subtropische storm die de Golfstaten treft Is het mogelijk om rechtstreeks elektriciteit op te wekken uit warmte?
Is het mogelijk om rechtstreeks elektriciteit op te wekken uit warmte?  Hoe beïnvloedt de zomer het leven van planten en dieren?
Hoe beïnvloedt de zomer het leven van planten en dieren?  Studie zegt dat blauwe waterstof waarschijnlijk slecht is voor het klimaat
Studie zegt dat blauwe waterstof waarschijnlijk slecht is voor het klimaat
Hoofdlijnen
- Waarschijnlijkheden in de genetica: waarom is het belangrijk?
- Verspilde vogelveren veranderd in voedsel
- Hoe de cellen van planten, dieren en eencellige organismen te vergelijken
- Verbeteringen in de cryo-elektronenmicroscopie brengen het leven op atomair niveau duidelijker in beeld
- Hoe evolueert het leven?
- Uit welke elementen bestaat glucose?
- Wormsoorten verloren 7, 000 genen na evolutie om zichzelf te bevruchten
- Behoefte aan snelheid maakt genoombewerking efficiënt, zo niet beter
- Waar is de kern gevonden in de cel en waarom?
 Twee Iraanse hackers aangeklaagd voor Amerikaans ransomware-plan
Twee Iraanse hackers aangeklaagd voor Amerikaans ransomware-plan En de blobs blijven maar komen
En de blobs blijven maar komen Bacteriële enzymen gekaapt om complexe moleculen te maken die normaal door planten worden gemaakt
Bacteriële enzymen gekaapt om complexe moleculen te maken die normaal door planten worden gemaakt Onderzoeken van het skyrmion Hall-effect onthullen verrassende resultaten (update)
Onderzoeken van het skyrmion Hall-effect onthullen verrassende resultaten (update) Onderzoekers ontwerpen katalysatoren voor dinucleaire locaties en onthullen het onderliggende mechanisme
Onderzoekers ontwerpen katalysatoren voor dinucleaire locaties en onthullen het onderliggende mechanisme Twee nieuwe opgeblazen hete Jupiters ontdekt door astronomen
Twee nieuwe opgeblazen hete Jupiters ontdekt door astronomen Mijnbouwtechnieken voor zand en grind
Mijnbouwtechnieken voor zand en grind Weer feiten over Saturnus
Weer feiten over Saturnus
Saturnus is de op een na grootste planeet in het zonnestelsel, rond een baan van ongeveer 900 miljoen mijl van de zon. Een dag op Saturnus duurt 10 uur, maar een van zijn jaren strekt zich uit over 29 aardse jaren. Saturnu
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com