
Wetenschap
Gebruik van licht om chemische reacties aan te sturen

Umar Aslam tuurt in de lichtbron die tijdens de experimenten werd gebruikt en die onthulde hoe de zilveren nanokubussen energie vingen en afleverden aan de platina-schalen. Krediet:Akhil Kantipuly, Michigan Engineering
Een exotische interactie tussen licht en metaal kan worden aangewend om chemische reacties duurzamer te maken, maar de fysica erachter is veel besproken in het veld.
Nutsvoorzieningen, een studie van de Universiteit van Michigan heeft aangetoond hoe een licht oogstend metaal energie overbrengt naar een katalytisch metaal, de weg vrijmaken voor betere katalysatorontwerpen.
Katalysatoren zijn bemiddelaars van chemische reacties:ze kunnen reacties laten plaatsvinden bij lagere temperaturen, het verminderen van de benodigde energie, en ze kunnen ook een voorsprong geven op een gewenst reactiepad, produceren van meer van de beoogde chemische stof en minder afval.
Er kan een nieuw soort katalysator worden gemaakt van zogenaamde plasmonische metalen die goed zijn in het opvangen van licht, maar ze zijn niet geweldig in het sturen van reacties. Om hun effectiviteit te verbeteren, onderzoekers hebben ze gepeperd met materialen die betere katalysatoren zijn, verbetering van reacties gerelateerd aan brandstofproductie en gewone huishoudelijke producten zoals tandpasta, bijvoorbeeld.
"De moeilijkheid met eerdere experimenten was dat er veel verschillende blootgestelde oppervlakken waren, dus het wordt erg moeilijk om je resultaten te interpreteren vanwege de complexiteit van de nanodeeltjes, " zei Umar Aslam, U-M-doctoraatsstudent chemische technologie,
Nutsvoorzieningen, Aslam en zijn collega's in de onderzoeksgroep van Suljo Linic, een professor in chemische technologie en een pionier in plasmonische katalyse, hebben laten zien hoe de energie beweegt. In plaats van energetische elektronen die van de lichtvanger naar de katalysator springen, het plasmonische metaal gedraagt zich meer als een radioantenne, met de katalysator als ontvanger, zei Aslam.
Hun experiment, gepubliceerd in het tijdschrift Natuur Nanotechnologie , was de eerste die overtuigend aantoonde dat dit mechanisme werkt.
"We hebben beschreven hoe plasmonische nanostructuren de energie van licht naar de katalytisch actieve plaatsen verplaatsen, " zei Linic. "We hebben toen aangetoond hoe dit mechanisme kan worden benut om zeer efficiënte en selectieve katalysatoren te ontwerpen."
Selectiviteit wordt gewaardeerd omdat het de ongewenste "nevenreacties" die afval produceren, vermindert.

Met platina gecoate zilveren nanokubussen. Krediet:Umar Aslam
Koper, zilver en goud staan bekend om hun plasmonische eigenschappen, of hun vermogen om de energie van zichtbaar licht in de vorm van golven op te vangen in hun oppervlakte-elektronen, oppervlakteplasmonen genoemd.
In het experiment, Aslam en Steven Chávez, ook een doctoraatsstudent in de chemische technologie, geproduceerde zilveren nanokubussen, ongeveer 75 nanometer (miljoenste van een centimeter) opzij. Die bedekten ze vervolgens met platina van slechts één nanometer dik.
Metaal dat dun is, is in wezen transparant voor licht, dus het gecoate zilver bleef het licht veranderen in oppervlakteplasmonen. Het zilver leidde vervolgens de energie naar de platina-coating door de zee van elektronen die tussen hen werd gedeeld. Het platina produceerde energetische elektronen en positief geladen gaten - ladingsdragers die vervolgens chemische reacties op het oppervlak zouden kunnen veroorzaken.
Platina wordt algemeen beschouwd als "de keizer van alle katalysatoren, " waardoor dit materiaal een voor de hand liggende keuze is voor onderzoekers die geïnteresseerd zijn in plasmonische katalyse, zei Aslam.
Maar dat was nog nooit eerder gelukt, omdat het heel moeilijk is om een dun laagje platina op zilver te krijgen. Onder de meeste omstandigheden, het zilver heeft de neiging om te bezoedelen, zei Aslam. Dus hij en Chavez pasten de reactieomstandigheden aan zodat de platinacoating veel sneller gebeurde dan de aanslag.
De groep toonde aan dat de katalysator bijna de snelheid verdubbelde waarmee koolmonoxideverontreinigingen in waterstof in kooldioxide veranderden wanneer het licht aan was - in vergelijking met de reactie in het donker, die alleen op platina vertrouwt. Deze omzetting is belangrijk bij de productie van waterstof uit methaan, terwijl overgebleven koolmonoxide de katalysatoren in waterstofbrandstofcellen ophoopt.
Ze toonden aan dat noch de zilveren nanokubussen alleen - noch de kubieke platina-omhulsels die overblijven wanneer het zilver door zuur werd verwijderd - konden presteren zoals de met platina gecoate kubussen. Nog altijd, Linic en Aslam waarschuwen dat deze nieuwe katalysatoren nog geen voorbodes zijn van een revolutie in de industriële chemie.
"Direct, plasmonische katalyse is een ontluikend veld, " zei Aslam. "Het kost meer om een dergelijke katalysator te maken in vergelijking met conventionele katalysatoren."
Maar met voortdurende vooruitgang in de synthese van nanodeeltjes en ideeën om de efficiëntieverbeteringen van plasmonische katalysatoren verder te verbeteren, ze kunnen de chemische industrie in de toekomst misschien groener maken.
De studie is getiteld "Controlling energy flow in multimetallic nanostructures for plasmonic catalyse."
 Een op de tien mensen heeft sporen van cocaïne of heroïne op hun vingerafdrukken
Een op de tien mensen heeft sporen van cocaïne of heroïne op hun vingerafdrukken Stabiliserende zwavelkathode door enkelvoudig Li-ionkanaalpolymeerbindmiddel
Stabiliserende zwavelkathode door enkelvoudig Li-ionkanaalpolymeerbindmiddel Chemici maken zelfassemblerend materiaal met een reeks nieuwe eigenschappen
Chemici maken zelfassemblerend materiaal met een reeks nieuwe eigenschappen Nieuwe studie analyseert levensvatbaarheid van duurzame brandstoffen ontwikkeld via nieuw proces
Nieuwe studie analyseert levensvatbaarheid van duurzame brandstoffen ontwikkeld via nieuw proces Hoe een hypothese van magische melk te schrijven voor 5e rang
Hoe een hypothese van magische melk te schrijven voor 5e rang
 Toenemende klimaatangst vormt een aanzienlijke bedreiging voor individuen en de samenleving
Toenemende klimaatangst vormt een aanzienlijke bedreiging voor individuen en de samenleving NASA-infraroodgegevens bevestigen dat depressie tropische storm Elida werd
NASA-infraroodgegevens bevestigen dat depressie tropische storm Elida werd Het probleem van elektronisch afval heroverwegen
Het probleem van elektronisch afval heroverwegen Kleine poliepen redden koralen van roofdieren en ziekten
Kleine poliepen redden koralen van roofdieren en ziekten Protesten verspreiden zich terwijl activisten vechten tegen telescoop op Hawaï
Protesten verspreiden zich terwijl activisten vechten tegen telescoop op Hawaï
Hoofdlijnen
- Hoe BRCA-genen werken
- Het voordeel van het hebben van veel replicatie-origines in een eukaryotisch chromosoom
- Mutualisme (biologie): definitie, types, feiten en voorbeelden
- Omgeving speelt sleutelrol bij veranderend bewegingsgedrag van dieren
- Structurele inzichten in processen op DNA-schadeplekken
- Stiekeme mannetjes nemen vrouwelijke hersens aan om grote bruten voor de gek te houden
- Ambien
- Wat gebeurt er op het chromosomale niveau als een resultaat van bevruchting?
- Sardines nemen ons mee naar de bronnen van biodiversiteit in de Amazone-rivier
- Flexibele batterij, geen lithium vereist

- Ingenieurs ontwikkelen eerste transistors die volledig zijn gemaakt van nanokristalinkten

- Cellulair stof biedt nieuwe hoop voor regeneratieve geneeskunde
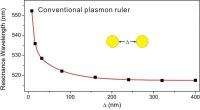
- Kleine linialen om structuren op nanoschaal te meten
- 'S Werelds allereerste grafeen wandelschoenen onthuld

 Gepolijste Chromium-gebaseerde Edge-browser komt in bèta
Gepolijste Chromium-gebaseerde Edge-browser komt in bèta Synthetische organellen laten zien hoe kleine plas-organen in onze cellen werken
Synthetische organellen laten zien hoe kleine plas-organen in onze cellen werken Doorbraak in het begrijpen van warmtetransport met een ketting van goudatomen
Doorbraak in het begrijpen van warmtetransport met een ketting van goudatomen Elektrische transiënten kwantificeren ladingsverlies in zonnecellen
Elektrische transiënten kwantificeren ladingsverlies in zonnecellen Bereken een cirkelvormig gebied
Bereken een cirkelvormig gebied  Onderzoekers hopen dat sommige objecten de brand in het Braziliaanse museum hebben overleefd
Onderzoekers hopen dat sommige objecten de brand in het Braziliaanse museum hebben overleefd Hoe knobbeltjes op de bodem van de zee blijven
Hoe knobbeltjes op de bodem van de zee blijven In robotica lessen, Armeense tieners dromen van hightech toekomst
In robotica lessen, Armeense tieners dromen van hightech toekomst
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

