
Wetenschap
Natuurkundigen meten voor het eerst van der Waals-krachten van individuele atomen

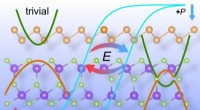
Zeldzame gasatomen afgezet op moleculair netwerk worden onderzocht met een sondeerpunt, die is versierd met een xenon-atoom. De metingen geven informatie over de zwakke van der Waals-krachten tussen deze afzonderlijke atomen. Krediet:Universiteit van Bazel, Afdeling Natuurkunde
Natuurkundigen van het Zwitserse Nanoscience Institute en de Universiteit van Basel zijn er voor het eerst in geslaagd de zeer zwakke van der Waals-krachten tussen individuele atomen te meten. Om dit te doen, ze fixeerden individuele edelgasatomen binnen een moleculair netwerk en bepaalden de interacties met een enkel xenon-atoom dat ze aan het uiteinde van een atoomkrachtmicroscoop hadden geplaatst. Zoals verwacht, de krachten varieerden afhankelijk van de afstand tussen de twee atomen; maar, in sommige gevallen, de krachten waren meerdere malen groter dan theoretisch berekend. Deze bevindingen worden gerapporteerd door het internationale team van onderzoekers in Natuurcommunicatie .
Van der Waals-krachten werken tussen niet-polaire atomen en moleculen. Hoewel ze erg zwak zijn in vergelijking met chemische bindingen, ze zijn enorm belangrijk van aard. Ze spelen een belangrijke rol in alle processen die te maken hebben met cohesie, hechting, wrijving of condensatie en zijn, bijvoorbeeld, essentieel voor de klimvaardigheden van een gekko.
Van der Waals-interacties ontstaan door een tijdelijke herverdeling van elektronen in de atomen en moleculen. Dit resulteert in de occasionele vorming van dipolen, die op hun beurt een herverdeling van elektronen in nauw aangrenzende moleculen induceren. Door de vorming van dipolen, de twee moleculen ervaren een wederzijdse aantrekkingskracht, wat een van der Waals-interactie wordt genoemd. Dit bestaat slechts tijdelijk, maar wordt herhaaldelijk opnieuw gevormd. De individuele krachten zijn de zwakste bindende krachten die in de natuur bestaan, maar ze tellen bij elkaar op om grootheden te bereiken die we heel duidelijk kunnen waarnemen op macroscopische schaal - zoals in het voorbeeld van de gekko.
Vast in de nano-beker
Om de van der Waals-krachten te meten, wetenschappers in Bazel gebruikten een atoomkrachtmicroscoop bij lage temperatuur met een enkel xenon-atoom op de punt. Vervolgens hebben ze het individuele argon gefixeerd, krypton- en xenon-atomen in een moleculair netwerk. Dit netwerk, die onder bepaalde experimentele omstandigheden zelforganiserend is, bevat zogenaamde nanobekers van koperatomen waarin de edelgasatomen als een vogelei op hun plaats worden gehouden. Alleen met deze experimentele opstelling is het mogelijk om de kleine krachten tussen de microscooppunt en het edelgasatoom te meten, omdat een puur metalen oppervlak de edelgasatomen zou laten schuiven.
Vergeleken met theorie
De onderzoekers vergeleken de gemeten krachten met berekende waarden en gaven deze grafisch weer. Zoals verwacht uit de theoretische berekeningen, de gemeten krachten daalden dramatisch naarmate de afstand tussen de atomen groter werd. Hoewel er een goede overeenkomst was tussen gemeten en berekende curvevormen voor alle geanalyseerde edelgassen, de absoluut gemeten krachten waren groter dan uit berekeningen volgens het standaardmodel was verwacht. Vooral voor xenon, de gemeten krachten waren een factor twee groter dan de berekende waarden.
De wetenschappers gaan ervan uit dat, zelfs in de edelgassen, er vindt ladingsoverdracht plaats en daarom worden af en toe zwakke covalente bindingen gevormd, wat de hogere waarden zou verklaren.
Het internationale team van wetenschappers uit Zwitserland, Japan, Finland, Zweden en Duitsland gebruikten de experimentele opstelling hierboven om de kleinste krachten te meten die ooit tussen individuele atomen zijn gedetecteerd. Daarbij, de onderzoekers hebben aangetoond dat ze nog steeds nieuwe gebieden kunnen betreden met behulp van atoomkrachtmicroscopie, die precies 30 jaar geleden werd ontwikkeld.
 Onderzoekssamenwerking maakt gebruik van geavanceerde technologie om nieuw diergeneesmiddel te produceren
Onderzoekssamenwerking maakt gebruik van geavanceerde technologie om nieuw diergeneesmiddel te produceren Wetenschappers bootsen neuraal weefsel na
Wetenschappers bootsen neuraal weefsel na Fysische en chemische eigenschappen van lipiden
Fysische en chemische eigenschappen van lipiden Hoe werkt fractionele destillatie?
Hoe werkt fractionele destillatie?  Boornitride en zilveren nanodeeltjes om de uitstoot van koolmonoxide te verminderen
Boornitride en zilveren nanodeeltjes om de uitstoot van koolmonoxide te verminderen
 Waarom vakantie vieren in een rampgebied niet onredelijk is
Waarom vakantie vieren in een rampgebied niet onredelijk is Wetenschappers zoeken heilige graal van klimaatverandering in heuvels van Oman
Wetenschappers zoeken heilige graal van klimaatverandering in heuvels van Oman Koeler voor delen van Europa, Spanje bestrijdt bosbranden
Koeler voor delen van Europa, Spanje bestrijdt bosbranden Hittestress kan tegen 2100 jaarlijks meer dan 1,2 miljard mensen treffen
Hittestress kan tegen 2100 jaarlijks meer dan 1,2 miljard mensen treffen Koolstofbelastingen kunnen nieuwe winnaars en verliezers tussen landen creëren
Koolstofbelastingen kunnen nieuwe winnaars en verliezers tussen landen creëren
Hoofdlijnen
- Matchmaking met gevolgen
- Waarom stijgt je lichaamstemperatuur als je een virus hebt zoals griep?
- Laat je huisdier niet per ongeluk dronken worden dit gekke seizoen (sorry Tiddles)
- Misplaatste monarchen:clusters van vlinders in het noorden
- Een beetje stress is goed voor de gezondheid van de cellen en een lang leven
- Bang voor spinnen? Het kan in je DNA zitten
- "Fingerprint Experiments
- Hoe de immuunrespons bijdraagt aan Homeostasis
- Differentiëren van RNA- en DNA-virussen
- Ingenieurs ontwikkelen eerste transistors die volledig zijn gemaakt van nanokristalinkten

- Nieuw voorgesteld multifunctioneel nanomateriaal kan zonne-energie verbeteren, kwantumcomputer
- Een zoektocht naar stabiliteit voor platinakatalysatoren
- Onderzoeksteam vindt dat de verhouding van de samenstellende atomen van vitaal belang is voor de prestaties

- Grafeen verdient zijn strepen:nieuwe elektronische toestand op nanoschaal ontdekt op grafeenvellen

 Een diepe duik in onderzeese monitoring:de oceaanbodem in de gaten houden
Een diepe duik in onderzeese monitoring:de oceaanbodem in de gaten houden Astronauten landen vanaf ISS-stint ontsierd door luchtlek, raket mislukking
Astronauten landen vanaf ISS-stint ontsierd door luchtlek, raket mislukking Een emmer water kan de gevolgen van klimaatverandering voor het zeeleven in het noordpoolgebied onthullen
Een emmer water kan de gevolgen van klimaatverandering voor het zeeleven in het noordpoolgebied onthullen Zeespiegel voor Nederlandse kust hoogste ooit gemeten in 2017
Zeespiegel voor Nederlandse kust hoogste ooit gemeten in 2017 Wetenschappers identificeren schadelijke bacteriën op basis van hun DNA tegen zeer lage kosten
Wetenschappers identificeren schadelijke bacteriën op basis van hun DNA tegen zeer lage kosten Sporen van de vroege magma-oceaan van de aarde geïdentificeerd in Groenlandse rotsen
Sporen van de vroege magma-oceaan van de aarde geïdentificeerd in Groenlandse rotsen Chinees vaartuig keert terug naar aarde met maanstenen
Chinees vaartuig keert terug naar aarde met maanstenen Advies:meer hulp aan consumenten dringend nodig
Advies:meer hulp aan consumenten dringend nodig
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Spanish | Swedish | German | Dutch | Danish | Norway | Italian | Portuguese |

-
Wetenschap © https://nl.scienceaq.com

