
Wetenschap
Nieuwe methode voor het versterken van hydrogels kan de groei van stamcellen sturen

Een nieuwe methode voor het manipuleren van de gelachtige omgevingen die stamcellen huisvesten, zou onderzoekers kunnen helpen de groei van deze veelzijdige cellen in bot te sturen, pees, weefsel of andere specifieke geslachten, zegt een biomedisch ingenieur van de Texas A&M University die de aanpak heeft ontwikkeld.
Werken met op collageen gebaseerde hydrogels, dit zijn biologisch afbreekbare gels die in een aantal biomedische toepassingen worden gebruikt vanwege hun compatibiliteit met het lichaam en zijn processen, Akhilesh Gaharwar heeft een methode ontwikkeld om hun stijfheid te moduleren zonder de chemie of structuur te beïnvloeden - een resultaat dat grote implicaties kan hebben voor stamcelonderzoek. Gaharwar, universitair docent bij de faculteit Biomedische Technologie van de universiteit, heeft zijn bevindingen gepubliceerd in het wetenschappelijke tijdschrift ACS Nano . Het volledige artikel is te vinden op pubs.acs.org/doi/abs/10.1021/acsnano.5b03918.
specifiek, Gaharwar is erin geslaagd de stijfheid van een hydrogel 10 keer en de taaiheid 20 keer te vergroten door een proces waarbij hij een kleine hoeveelheid bolvormig, magnetische nanodeeltjes aan de op collageen gebaseerde hydrogels. Het hele proces is binnen enkele seconden voltooid, en het stelt hem in staat om de gel aan te passen aan verschillende gradaties van stijfheid en taaiheid, afhankelijk van de hoeveelheid nanodeeltjes in het materiaal, zegt Gaharwar.
Het proces, hij voegt toe, heeft nog een ander duidelijk voordeel:het is celvriendelijk. Omdat Gaharwar extreem lage concentraties nanodeeltjes gebruikt, zijn proces verandert de chemische samenstelling van de hydrogel niet significant.
Beheersing van de fysieke eigenschappen van hydrogels, Gaharwar legt uit, is essentieel omdat deze gels duurzaam moeten zijn en tegelijkertijd moeten voldoen aan de eigenschappen van de weefsels die ze nabootsen wanneer ze in het lichaam worden ingezet - bijvoorbeeld, wanneer ze fungeren als steigers die helpen bij de genezing van interne verwondingen. Dat is slechts een van de vele biomedische toepassingen die de hydrogel van Gaharwar kan beïnvloeden. Naast tissue engineering toepassingen, Gaharwar's mechanisch verbeterde hydrogel zou de benaderingen voor medicijnafgifte kunnen bevorderen, biosensoren en andere technologieën, maar het zou een nog belangrijkere rol kunnen spelen als hulpmiddel om meer te weten te komen over stamcellen, hij zegt. Het systeem, hij legt uit, zou onderzoekers in staat kunnen stellen beter te begrijpen hoe stamcellen zich gedragen en zelfs bepalen hoe ze differentiëren tot specifieke soorten cellen.
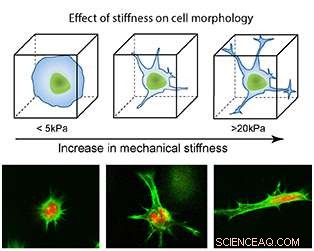
Bekend om hun vermogen om zich te ontwikkelen tot verschillende celtypes – zoals een spier, bloed- of hersencellen – stamcellen kunnen dienen als een intern herstelsysteem, het aanvullen van andere cellen. Sleutel tot deze transformatie, Gaharwar-aantekeningen, is de micro-omgeving rond de stamcellen. Afhankelijk van waar deze stamcellen zich in het lichaam bevinden, deze cellen zullen veranderen in verschillende soorten cellen, hij legt uit. Bijvoorbeeld, stamcellen die in stijvere omgevingen worden uitgerekt, kunnen uiteindelijk uitgroeien tot botcellen, terwijl stamcellen die in zachtere omgevingen rond blijven, zich kunnen ontwikkelen tot kraakbeen. Zie het als een soort domino-effect:de micro-omgeving van de stamcel beïnvloedt de vorm, en de vorm van de stamcel beïnvloedt de ontwikkeling tot een specifiek celtype. Gezien dit feit, Gaharwar gelooft dat het beheersen van de stijfheid van de omgeving van de cel (in dit geval een hydrogel die stamcellen omvat) zou kunnen resulteren in een verhoogde controle van stamceldifferentiatie.

Die omgeving beheersen, Gaharwar zegt, wordt bereikt door een proces dat bekend staat als crosslinking. Verknoping, hij legt uit, omvat het verbinden van de polymere ketens waaruit een hydrogel bestaat, zodat ze een onderling verbonden netwerk vormen dat in feite een ruggengraat voor de gel dient en, als resultaat, verhoogt de stijfheid ervan. Om deze ketens te verbinden zijn Gaharwar's nanodeeltjes nodig, die als een soort mortel dienen door deze ketens op moleculair niveau met elkaar te verbinden. Deze bolvormige, ijzeroxide nanodeeltjes, waarvan de oppervlakken zijn aangepast door Gaharwar en zijn team, meerdere conjugatiepunten hebben waarop de polymere ketens zich hechten door sterke chemische bindingen te vormen, hij zegt. Wanneer dit gebeurt, er wordt een netwerk van ketens gevormd en de hydrogel wordt versterkt, hij zegt.
Andere standaardtechnologieën die gebruik maken van verschillende nanodeeltjes resulteren niet in hetzelfde niveau van mechanische stijfheid omdat de nanodeeltjes geen chemische interactie aangaan met de polymeerketens in de gel; ze zitten gewoon in de val, Gaharwar legt het uit. Bovendien, de benaderingen die enige mate van stijfheid bereiken, produceren vaak een onvriendelijke omgeving voor de cel die resulteert in celdood als gevolg van hoge concentraties van het versterkende middel, hij zegt. De aanpak van Gaharwar overwint die uitdaging door een 10 te gebruiken, 000 keer minder concentratie van nanodeeltjes.
"Door een minieme concentratie nanodeeltjes toe te voegen, we kunnen een drastische toename of afname van de fysieke eigenschappen van de hydrogel krijgen, " zegt Gaharwar. "Door de grootte en concentratie van de nanodeeltjes te veranderen, we kunnen hydrogels krijgen die variëren van één kilopascal tot 200 kilopascal."
Gevoed door de veelbelovende eerste resultaten die hij en zijn team hebben behaald, Gaharwar is van plan om met de verbeterde hydrogel te blijven werken om te bepalen of het inderdaad een differentiatie in stamcellen kan veroorzaken. Deze cellen, hij legt uit, moeten een dynamische omgeving ervaren (zoals ze zouden doen in het lichaam) waar verschillende mate van kracht wordt uitgeoefend door de hydrogel en wordt ervaren door de cellen erin. In de volgende fase van het onderzoek zal het team, hij zegt, hoopt deze externe prikkels met een bioreactor te introduceren, zodat er meer diepgaand onderzoek kan worden gedaan.
 Nabij-infrarood fotoactiveerbare oxygenatiekatalysatoren van amyloïde peptide
Nabij-infrarood fotoactiveerbare oxygenatiekatalysatoren van amyloïde peptide Het gebruik van materiaal met een hoge energiedichtheid in het ontwerp van de elektrode verbetert lithiumzwavelbatterijen
Het gebruik van materiaal met een hoge energiedichtheid in het ontwerp van de elektrode verbetert lithiumzwavelbatterijen Team ontwikkelt innovatieve, ideale vloeistofafstotende oppervlakken
Team ontwikkelt innovatieve, ideale vloeistofafstotende oppervlakken Een nieuw licht schijnen op biomimetische materialen
Een nieuw licht schijnen op biomimetische materialen Compact glasvezelapparaat werpt licht op ademanalyse in realtime
Compact glasvezelapparaat werpt licht op ademanalyse in realtime
 Rook van bosbranden kan blijvende gevolgen hebben voor het klimaat
Rook van bosbranden kan blijvende gevolgen hebben voor het klimaat Soorten aardwetenschappen
Soorten aardwetenschappen
De studie van de aarde, inclusief de formatie, bronnen, natuurlijke processen, geschiedenis en omgevingen, wordt aardwetenschappen of geowetenschap genoemd. Geoscientisten bestuderen ook andere planeten en het zonnestelsel
 Ontdekkingsreiziger Amundsens-schip keert na 100 jaar terug naar Noorwegen
Ontdekkingsreiziger Amundsens-schip keert na 100 jaar terug naar Noorwegen Mauritius roept noodtoestand uit omdat gestrand schip brandstof morst
Mauritius roept noodtoestand uit omdat gestrand schip brandstof morst Rustige storing in Brits-Columbia die grote aardbevingen kan veroorzaken
Rustige storing in Brits-Columbia die grote aardbevingen kan veroorzaken
Hoofdlijnen
- Zeehonden en onze kusten
- Cowpea beschermd tegen een verwoestende plaag, gratis voor kleine Afrikaanse boeren
- Prokaryotische versus eukaryotische cellen: overeenkomsten en verschillen
- Menselijke resten gevonden in grote Australische krokodil
- Wat gebeurt er in de interfase van de celcyclus?
- Welke moleculen kunnen zonder hulp door het plasmamembraan gaan?
- Micro-evolutie: definitie, proces, micro versus macro & voorbeelden
- Kwam Eiwit, DNA of RNA als eerste?
- DNA-modellen maken met behulp van papier
- Composietfilm is veelbelovend als vervanging voor transparante elektrische geleiders in displays

- Grafeen verbetert veel materialen, maar laat ze bevochtigbaar

- Nieuwe productiemethode voor grafeen verbreedt perspectieven voor beter gebruik

- Bionische katalysatoren om schone energie te produceren

- Nanoschakelaars die licht omzetten in macroscopische beweging

 Wijdverbreide verspreiding van gevangenen onthuld in nieuwe gegevens
Wijdverbreide verspreiding van gevangenen onthuld in nieuwe gegevens Hoe het Tornado Intercept Vehicle werkt
Hoe het Tornado Intercept Vehicle werkt  Astronoom onthult nooit eerder geziene details van het centrum van onze melkweg
Astronoom onthult nooit eerder geziene details van het centrum van onze melkweg Onderzoekers vinden eenvoudige, goedkope manier om de efficiëntie van zonnecellen te verhogen
Onderzoekers vinden eenvoudige, goedkope manier om de efficiëntie van zonnecellen te verhogen Berkeley Lab maakt de weg vrij voor realtime ptychografische datastreaming
Berkeley Lab maakt de weg vrij voor realtime ptychografische datastreaming Diesel is nu beter dan benzine, studie zegt:
Diesel is nu beter dan benzine, studie zegt: Natuurkundigen simuleren een systeem waarin fermionen met meerdere smaken zich gedragen als bosonen
Natuurkundigen simuleren een systeem waarin fermionen met meerdere smaken zich gedragen als bosonen Stapsgewijze aanwijzingen voor het maken van een vulkaan voor een schoolproject
Stapsgewijze aanwijzingen voor het maken van een vulkaan voor een schoolproject
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

