
Wetenschap
Nanocontainers voor nanocargo:het leveren van genen en eiwitten voor cellulaire beeldvorming, genetische geneeskunde en kankertherapie

Het van T4-capside afgeleide specifieke exogene DNA plus eiwitverpakking en eukaryote celafgifteschema. (A) DNA dat codeert voor een N-terminaal CTS-peptide van 10 aminozuren, gefuseerd met de faag P1 Cre, maakt de synthese van CTS-Cre en het richten van het enzym in de vroege kern-scaffold van het T4-procapside in vivo mogelijk. Procapside-assemblage en rijpingsspecifieke virale protease stabiliseren de procapside, verwijder het grootste deel van de steigerkern als peptiden, en verwijder het CTS-peptide van Cre. Mutaties in de virale terminase blokkeren DNA-verpakking en zorgen ervoor dat een volwassen maar DNA-leeg groot Cre-bevattend procapside in hoge mate wordt gezuiverd van viraal geïnfecteerde bacteriën. (B) In vitro verpakking in de volwassen capside van plasmide-DNA dat mCherry bevat, aangedreven door een CMV-promotor en twee loxP-sites die een SfiI-restrictie-enzymsite flankeren die de linearisatie mogelijk maken die nodig is voor het verpakken. Het DNA wordt met hoge efficiëntie in het procapside verpakt door het ATP-aangedreven terminase-motoreiwit (gp17). (C) Het verpakte Cre-enzym recirculariseert het verpakte lineaire plasmide-DNA tussen de twee loxP-sites. Het DNA-bevattende capside wordt opgenomen door eukaryote cellen, hier zonder een specifiek peptidedoel weer te geven, of in eukaryote cellen die specifiek Soc en Hoc weergegeven peptiden gebruiken die een hoge affiniteit hebben voor de RP1- en RP2-receptoren, respectievelijk. Krediet:Liu JL, et al. (Online gepubliceerd vóór print 26 augustus, 2014) Viraal nanodeeltjes-ingekapseld enzym en geherstructureerd DNA voor celafgifte en genexpressie. Krediet:Liu JL, et al. (2014) Viraal nanodeeltjes-ingekapseld enzym en geherstructureerd DNA voor celafgifte en genexpressie. Proc Natl Acad Science VS Online gepubliceerd voor print 26 augustus 2014. doi:10.1073/pnas.1321940111
(Phys.org) —Door een specifiek eiwit en nucleïnezuur in een op icosahedral faag T4 capside-gebaseerd nanodeeltje te laden, de liganden van het resulterende celafgiftevehikel kunnen binden aan het oppervlak van specifieke doelweefsels om de eiwit/DNA-lading af te leveren. (Icosahedrale virale nanodeeltjes zijn evolutionaire eiwitschillen die in een hiërarchische volgorde zijn geassembleerd, wat resulteert in een stabiele eiwitlaag en een binnenruimte voor het opnemen van nucleïnezuren en eiwitten; een capside is de eiwitschaal van een virus.) De techniek heeft medicijn- en genen- leveringstoepassingen bij ziekten bij de mens, diagnostische en cellulaire beeldvorming, en andere medische gebieden. Onlangs, wetenschappers van het US Naval Research Laboratory, Washington, DC en University of Maryland in Baltimore verpakte T4-nanodeeltjes in vivo met actieve cyclische recombinatie, of Cre, recombinase (een genetisch recombinatie-enzym dat wordt gebruikt om de genoomstructuur te manipuleren en genexpressie te regelen) en in vitro met fluorescerend mCherry (een fluorescerend eiwit dat wordt gebruikt als een marker wanneer het wordt gelabeld aan moleculen en celcomponenten) expressieplasmide-DNA, en deze nanodeeltjes in kankercellen afleverden:wanneer ze in cellen worden vrijgegeven in aanwezigheid van zowel DNA als eiwit, het recombinase verbetert de mCherry-expressie door circularisatie (dat wil zeggen, veranderen van het verpakte lineaire DNA in een cirkelvormige lus). De onderzoekers stellen dat deze efficiënte en specifieke verpakking in capsiden en het uitpakken van zowel DNA als eiwit met afgifte van de enzymatisch veranderde eiwit/DNA-complexen uit de nanodeeltjes in cellen potentieel hebben in tal van downstream-toepassingen zoals genetische en kankertherapieën.
Dr. Jinny L. Liu besprak het artikel dat zij, Prof. Lindsay W. Black en hun co-auteurs gepubliceerd in: Proceedings van de National Academy of Sciences USA . "Icosahedrale virale nanodeeltjes zijn in wezen 100 nm bij 80 nm nanocontainers waarmee exogeen genetisch materiaal kan worden verpakt in vitro via nucleïnezuurmachines waarmee in het algemeen alleen lineair DNA/RNA via een portaalkanaal kan worden verpakt, " vertelt Liu Phys.org . "Echter, in vitro eiwitverpakking is over het algemeen onmogelijk, omdat er voor de meeste virale nanodeeltjes geen verpakkingsmachine voor eiwitten bestaat die vergelijkbaar is met die voor nucleïnezuurverpakkingsmachines." dit zal naar verwachting leiden tot eiwitdenaturatie en verlies van enzymatische activiteit.
Dat gezegd hebbende, de natuur heeft oplossingen ontwikkeld voor dit raadsel van de eiwitverpakking. Gedurende in vivo virale capside-assemblage, Liu legt uit, sommige bacteriële virussen, of bacteriofagen, doeleiwitten in de procapsiden voordat het nucleïnezuur is zo verpakt dat de eiwitten met het nucleïnezuur worden uitgeworpen, waardoor infectie samen met het nucleïnezuur wordt vergemakkelijkt. (Een procapside, of voorhoofd, is een onvolgroeide virale capsidestructuur gevormd in de vroege stadia van zelfassemblage van sommige bacteriofagen. De productie en assemblage van stabiele proheads is een essentiële voorloper van het verpakken van het bacteriofaaggenoom.) Slechts een paar fagen zijn goed gekarakteriseerd in vivo eiwit verpakkingssystemen, en faag T4 is het best gekarakteriseerd. "Prof. Black's laboratorium aan de UMB en mijn laboratorium aan het NRL hebben aangetoond dat niet alleen een specifiek vreemd enzym - cyclische recombinatie (Cre) recombinase - kan worden verpakt in de capside in vivo , maar ook dat het actief is in de capside." Deze activiteit werd aangetoond door de religatie (het opnieuw verbinden van twee DNA-strengen of andere moleculen door een fosfaatesterbinding) van verpakt lineair DNA geflankeerd met twee Cre-recombinatieplaatsen aan te tonen.
Het artikel laat zien dat de aanzienlijke ruimte in een T4-nanocontainer het actieve Cre-enzym samen met exogeen DNA herbergt. "Voor mogelijke toepassingen, T4 kan tot 50 kb exogeen lineair DNA verpakken dat de gewenste genen van volledige lengte bevat, samen met recombinasen, ofwel Cre of λ-rode eiwitten, voor specifieke homologe recombinatie binnen het chromosoom, "Liu merkt op. ( Homologe recombinatie is een type genetische recombinatie waarbij nucleotidesequenties worden uitgewisseld tussen twee vergelijkbare of identieke DNA-moleculen.) "We verwachten dat het cas9-enzym op een vergelijkbare manier kan worden ingekapseld - en in feite, op deze manier zijn ten minste acht verschillende eiwitten ingekapseld. Door homologe recombinatie, ons systeem kan toestaan dat het gecorrigeerde gen het gemuteerde gen vervangt op zijn oorspronkelijke locatie binnen het chromosoom of door de overactieve genen in stamcellen precies uit te schakelen." Liu wijst erop dat de T4-afgiftevector veiliger en beter gecontroleerd is dan andere virale afleveringsgenen therapie, zoals die welke genen afleveren met behulp van infectieuze dierlijke virale vectoren om het gen willekeurig in het chromosoom in te voegen.
In hun krant de auteurs melden dat het T4-capside-NP-genexpressie- en eiwitafgiftesysteem complementair kan zijn aan of gebruikt kan worden in combinatie met gentherapie op basis van RNA Cas en tarannuclease. (Cas-genen coderen voor eiwitten die verband houden met DNA-loci die korte herhalingen van basensequenties bevatten, bekend als Clustered Regularly Interspaced Short Palindromic Repeats, of CRISPR's.) "Het T4-nanodeeltjesexpressiesysteem kan gemakkelijk Cas9 en op tarannuclease gebaseerde recombinatie aanvullen door de lineaire cas9 te verpakken, doel-sgRNA-plasmide-DNA, en Cre-recombinase – of zelfs ligase, een enzym dat de samenvoeging van DNA-strengen vergemakkelijkt - en de resulterende T4-nanodeeltjes aflevert in de ontvangende eukaryote cellen met een hoge specificiteit door gebruik te maken van SOC en HOC, " vertelt Liu Phys.org . (SOC en HOC zijn overbodige T4-capside-eiwitten.) "Door de targeting-liganden (bindende moleculen) op het oppervlak weer te geven, het T4-capside-genexpressie- en eiwitsysteem zal de Cas9- en sgRNA-plasmiden efficiënt samen in de gewenste ontvangende cellen kunnen leveren. Relevante enzymatisch actieve eiwitten Cas9, lambda exonuclease, lambda-bèta-eiwit en andere kunnen direct tegelijkertijd vanuit het T4-nanodeeltje worden afgeleverd."

Meting van de remming door endocytoseremmers en colokalisatie met lysosomen in A546-T4-behandelde A549-cellen. (A) Voorbehandeling met amantadine, specifiek stabiliseren van de clathrin-gecoate putten, verminderde de opname van A546-T4 NP's door A549-cellen op een concentratieafhankelijke manier. (B) Voorbehandeling met de PI3-kinaseremmer, wortmannine, verminderde ook de opname van A546-T4 op een concentratieafhankelijke manier. (C) Een overlappend confocale celbeeld verkregen met een 60 × objectief met de geïnternaliseerde A546-T4 procapsiden (geel), lysosomen gekleurd met LysoTracker Blue (blauw), en de overlappende vlekken (wit). (Schaalbalk, 10 m.) (D) Een confocale afbeelding toont het brede beeld van behandelde cellen die overlappende delen (witte vlekken) van lysosomen (blauw) met A546-T4 procapsiden (geel) bevatten. Het beeld werd verkregen met behulp van een 20× objectief. (Schaalbalk, 50 m.) Krediet:Liu JL, et al. (Online gepubliceerd vóór print 26 augustus, 2014) Viraal nanodeeltjes-ingekapseld enzym en geherstructureerd DNA voor celafgifte en genexpressie. Krediet:Liu JL, et al. (2014) Viraal nanodeeltjes-ingekapseld enzym en geherstructureerd DNA voor celafgifte en genexpressie. Proc Natl Acad Science VS Online gepubliceerd voor print 26 augustus 2014. doi:10.1073/pnas.1321940111
Liu voegt eraan toe dat haar laboratorium ook celbeeldvorming en medicijn- / genafgifte aan eukaryote cellen heeft bestudeerd met behulp van T4-staartloze nanodeeltjes, waarvan de onderzoekers hebben aangetoond dat ze de eukaryote cellen kunnen binnendringen zonder celdood te veroorzaken.
Een specifiek voorbeeld van potentiële downstream-geneesmiddel- en gentherapeutische toepassingen die het resultaat zijn van de nieuwe benadering, is de levering van het toxische eiwit en het lineaire plasmide dat neutraliserende peptiden of antilichamen produceert in gerichte kankercellen die specifieke kankermarkers vertonen met behulp van SOC + HOC-markerbindende eiwitten met hoge affiniteit op de oppervlak van de capsiden, terwijl een ander voorbeeld is om het systeem te gebruiken voor HIV-gentherapie.
Liu voegt eraan toe dat er verschillende manieren zijn om dit systeem voor gentherapie te gebruiken:
- Levering van T4-nanodeeltjes verpakt met het recombinase (of ligase) en lineair plasmide-DNA om gp120 of interferon te produceren om de immuunrespons bij patiënten te genereren of te versterken
- Levering van T4-nanodeeltjes verpakt met recombinase (ligase) en het lineaire oplosbare CD40-expressieplasmide-DNA in T-lymfocyten of hematopoëtische cellen om de infectie van HIV-1 te blokkeren
- Remming van RNA door het leveren van het gemanipuleerde plasmide-DNA dat lok-RNA kan produceren voor het binden van het virale sense-DNA
- Remming van eiwit door het afleveren van verpakte antivirale antilichamen en anti-hiv-antilichaamplasmide-DNA
Naast diagnostische en cellulaire beeldvorming, het T4-nanodeeltjes-gen-eiwitsysteem kan gerepareerde genen leveren om menselijke genetische ziekten te corrigeren - bijvoorbeeld, het omkeren van adenosinedeaminase (ADA)-deficiëntie door het introduceren van het eiwit-DNA-complex om ADA in stamcellen tot expressie te brengen. Andere brede onderzoeksgebieden die worden beïnvloed door gentherapietechnologieën, zoals genetische defecten, kanker, neurologische aandoeningen bij volwassenen, en zelf ouder worden, kan ook baat hebben bij dit onderzoek.
Vooruit gaan, de wetenschappers willen meer T4-procapsiden ontwikkelen die exonuclease en andere recombinasen verpakken, samen met geconstrueerd doel-DNA om aan te tonen dat de resulterende T4-capsiden het gen kunnen inbrengen in een stamcellijn met een genetische deficiëntie. "In aanvulling, " concludeert Liu, "We werken aan het aanpassen van ons systeem om therapeutische peptiden of antilichamen te leveren aan cellen die zijn blootgesteld aan of geïnfecteerd zijn door biothreat-agentia, zoals eiwittoxines of virussen, efficiënte neutralisatie van toxine-effecten. De behandeling en genezing van cellen en weefsels die aan dergelijke middelen worden blootgesteld, zijn van groot belang voor onze onderzoeksgemeenschap op het gebied van biodefensie."
© 2014 Fys.org
 Neutronen en röntgenstralen gebruiken om de veroudering van lithiumbatterijen te analyseren
Neutronen en röntgenstralen gebruiken om de veroudering van lithiumbatterijen te analyseren Thermische dynamica experimenten voor kinderen
Thermische dynamica experimenten voor kinderen  Nooit meer met vuur spelen:onderzoek biedt inzicht in veiligere oplaadbare batterijen
Nooit meer met vuur spelen:onderzoek biedt inzicht in veiligere oplaadbare batterijen Oogsten van microdeeltjes uit een vloeistofstraal
Oogsten van microdeeltjes uit een vloeistofstraal Wetenschappers hebben voor het eerst excitonen in nikkeloxide gevonden
Wetenschappers hebben voor het eerst excitonen in nikkeloxide gevonden
 Geofysicus:gewicht van Harvey-regens deed Houston zinken
Geofysicus:gewicht van Harvey-regens deed Houston zinken Studie biedt eerste holistische beoordeling van plasticvervuiling in het Caribisch gebied
Studie biedt eerste holistische beoordeling van plasticvervuiling in het Caribisch gebied Planning voor toekomstige waterveiligheid in China
Planning voor toekomstige waterveiligheid in China Het implementeren van koolstofbeprijzing tijdens de pandemie kan landen helpen groener, slimmer
Het implementeren van koolstofbeprijzing tijdens de pandemie kan landen helpen groener, slimmer Welke soorten vissen eten Eendekroos?
Welke soorten vissen eten Eendekroos?
Hoofdlijnen
- Onderzoek biedt inzichten voor de bestrijding van verwoestende amfibieënziekte
- Extra Y-chromosoom bij mannen
- Onderzoekers identificeren gen om hybride tarweveredeling te helpen
- Pompoengenomen gesequenced, ongewone evolutionaire geschiedenis onthullen
- Genomische studie onderzoekt de evolutie van zachte killer-bijen in Puerto Rico
- Kunnen we Neanderthalers terugbrengen?
- Soorten berekenen Evenness
- Het redden van Indonesische paradijsvogels dorp voor dorp
- Is lachen besmettelijk?
- Cornell-wetenschappers beoordelen de toekomst van grafeen

- Kleine nanostructuren beloven een grote impact op high-speed low-power optische apparaten

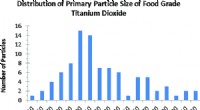
- Kinderen worden mogelijk het meest blootgesteld aan nanodeeltjes van titaniumdioxide
- Draagbare diagnostiek ontworpen om te worden geschud, niet geroerd

- Ultradunne perovskiet nanokristallen geschikt voor gebruik in afstembare en energiezuinige LED's

 Welke faseveranderingen zijn exotherm en endotherm?
Welke faseveranderingen zijn exotherm en endotherm?  Onderzoekers identificeren zeven soorten nepnieuws, helpen bij een betere detectie
Onderzoekers identificeren zeven soorten nepnieuws, helpen bij een betere detectie Team vindt oudste wapens ooit ontdekt in Noord-Amerika
Team vindt oudste wapens ooit ontdekt in Noord-Amerika Milieubeleid heeft vaak ongewenste neveneffecten
Milieubeleid heeft vaak ongewenste neveneffecten Hoe werd het koolstofgehalte in aardse en maanmantels vastgesteld?
Hoe werd het koolstofgehalte in aardse en maanmantels vastgesteld? Herprogrammeerbare satelliet krijgt vorm
Herprogrammeerbare satelliet krijgt vorm Emotioneel welzijn tijdens het tuinieren, vergelijkbaar met andere populaire activiteiten, studie vondsten
Emotioneel welzijn tijdens het tuinieren, vergelijkbaar met andere populaire activiteiten, studie vondsten Klein, pijnvrije vaccinaties - micronaalden en nanodeeltjes
Klein, pijnvrije vaccinaties - micronaalden en nanodeeltjes
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

