Wetenschap
Goede vibraties:licht verwarmd water gebruiken om medicijnen af te geven
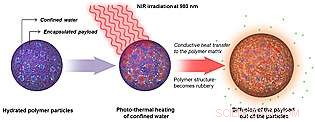
In deze schematische weergave is een gehydrateerd polymeer nanodeeltje wordt blootgesteld aan nabij-infrarood licht. De NIR verwarmt waterzakken in het nanodeeltje, waardoor het polymeer zachter wordt en ingekapselde moleculen in de omgeving kunnen diffunderen. Krediet:UC San Diego School of Medicine
Onderzoekers van de Universiteit van Californië, San Diego Skaggs School of Pharmacy en Farmaceutische Wetenschappen, in samenwerking met materiaalwetenschappers, ingenieurs en neurobiologen, hebben een nieuw mechanisme ontdekt om licht te gebruiken om medicijnafgevende nanodeeltjes en andere gerichte therapeutische stoffen in het lichaam te activeren.
Deze ontdekking vertegenwoordigt een belangrijke innovatie, zei Ada Almutairi, doctoraat, universitair hoofddocent en directeur van het gezamenlijke UC San Diego-KACST Centre of Excellence in Nanomedicine. Tot nu toe, ze zei, slechts een handvol strategieën die gebruik maken van door licht geactiveerde afgifte van nanodeeltjes zijn gemeld.
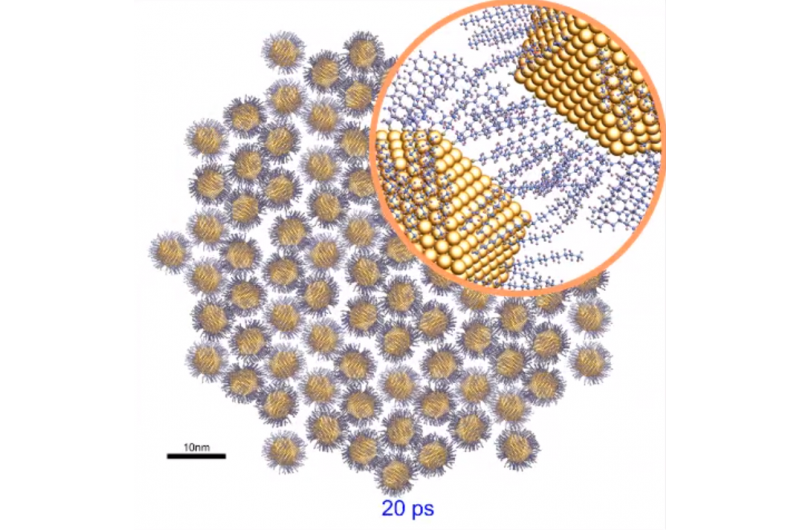
Het mechanisme, beschreven in de 1 april 2014 online uitgave van ACS Nano , maakt gebruik van bijna-infrarood (NIR) licht van een laser met laag vermogen om waterzakken te verwarmen die zijn opgesloten in niet-fotogevoelige polymere nanodeeltjes die zijn doordrenkt met medicijnen. De waterzakken absorberen de lichtenergie als warmte, waardoor het inkapselende polymeer zachter wordt en het medicijn in het omringende weefsel kan worden afgegeven. Het proces kan meerdere keren worden herhaald, met nauwkeurige controle van de hoeveelheid en verspreiding van het medicijn.
"Een belangrijk voordeel van dit mechanisme is dat het compatibel moet zijn met bijna elk polymeer, zelfs die in de handel verkrijgbaar zijn, " zei Mathieu Viger, een postdoctoraal onderzoeker in het laboratorium van Almutairi en co-hoofdauteur van de studie. "We hebben waargenomen dat water wordt vastgehouden in deeltjes die zijn samengesteld uit alle biologisch afbreekbare polymeren die we tot nu toe hebben getest."
De methode, merkte Viger op, zou dus gemakkelijk door veel biologische laboratoria kunnen worden overgenomen.
Het gecombineerde gebruik van gehydrateerde polymeren en nabij-infrarood licht lijkt een groot aantal technologische en gezondheidsbarrières op te lossen die eerdere, vergelijkbare benaderingen. Eerdere pogingen om NIR-getriggerde afgifte te gebruiken, zijn niet op grote schaal benut omdat ze speciale designerpolymeren nodig hadden, dure lasers met hoog vermogen en/of de co-inkapseling van anorganische deeltjes waarvan de veiligheid in het lichaam twijfelachtig blijft.
De nieuwe methode beschreven door Almutairi en collega's van de afdelingen Werktuigbouwkunde en Lucht- en Ruimtevaarttechniek, neurowetenschap, en Scheikunde en Biochemie aan de UC San Diego gebruikt NIR op een trillingsgolflengte die is ingesteld om watermoleculen te exciteren, die de optische energie absorberen en omzetten in warmte. NIR kan biologische weefsels doordringen tot grotere diepten dan zichtbaar of ultraviolet licht.
Co-hoofdauteur Wangzhong Sheng, een afgestudeerde student in de afdeling Werktuigbouwkunde en Luchtvaart- en Ruimtevaarttechniek, verklaarde de selectiviteit van verwarming door het opgesloten water in deeltjes te vergelijken met een glas water en het omringende water in de oplossing of het weefsel met een badkuip. Door het enorme volumeverschil wordt de kleinere hoeveelheid water veel sneller opgewarmd.
Een duidelijk gebruik van de methode, zei Almutairi, is door licht getriggerde medicijnafgifte, maar met meer onderzoek, ze verwacht dat de nieuwe methode een verscheidenheid aan industriële, medische en wetenschappelijke toepassingen, met inbegrip van "elke technologische toepassing die vereist dat de chemie in tijd en in de ruimte wordt gecontroleerd, zoals in katalyse of zelfherstellende materialen of door licht geactiveerde zonnefilters of het doseren van pesticiden."
 Onderzoekers ontwikkelen hybride meta-biomateriaal dat de levensduur van heupimplantaten kan verlengen
Onderzoekers ontwikkelen hybride meta-biomateriaal dat de levensduur van heupimplantaten kan verlengen De geboorte van een nieuw eiwit
De geboorte van een nieuw eiwit Wat kan worden gebruikt om plastic petri-platen in een plastic omhulsel te steriliseren?
Wat kan worden gebruikt om plastic petri-platen in een plastic omhulsel te steriliseren?  Hoe maak je nep sneeuw met bakken Soda
Hoe maak je nep sneeuw met bakken Soda iPhone plus poreus silicium op nanoschaal is goedkoop, eenvoudige thuisdiagnose
iPhone plus poreus silicium op nanoschaal is goedkoop, eenvoudige thuisdiagnose
Hoofdlijnen
- Video van vier bobcats in een buitenwijk toont gezonde populatie
- Wat betekent ion?
- Microbiële ziekten en mutaties: wat is het ?, Lijsten & Oorzaken
- Stappen van DNA-transcriptie
- Your Brain On: Empathy
- Wat gebeurt er met een Zygote na bevruchting?
- Oude levensvorm ontdekt in afgelegen Tasmaanse vallei
- Populatie-ecologie: definitie, kenmerken, theorie en voorbeelden
- 'S Werelds botanische tuinen bevatten een derde van alle bekende plantensoorten, en help de meest bedreigde te beschermen
 NZs-fossielen laten zien dat meer soorten in warmere wateren leefden, maar de huidige opwarmingstrends kunnen dit patroon doorbreken
NZs-fossielen laten zien dat meer soorten in warmere wateren leefden, maar de huidige opwarmingstrends kunnen dit patroon doorbreken Huawei vecht met VS over spionagevrees om mobiele beurs te overtreffen
Huawei vecht met VS over spionagevrees om mobiele beurs te overtreffen Door oorlog verscheurd Zuid-Soedan loopt groot risico op klimaatverandering
Door oorlog verscheurd Zuid-Soedan loopt groot risico op klimaatverandering Bessel,
Bessel,  Hooggekwalificeerd personeel op openbare kleuterscholen overwint personeelsvoordeel in de particuliere sector
Hooggekwalificeerd personeel op openbare kleuterscholen overwint personeelsvoordeel in de particuliere sector Misvattingen in de diepzee veroorzaken onderschatting van de effecten van mijnbouw op de zeebodem
Misvattingen in de diepzee veroorzaken onderschatting van de effecten van mijnbouw op de zeebodem Verborgen symmetrie gevonden in chemische kinetische vergelijkingen
Verborgen symmetrie gevonden in chemische kinetische vergelijkingen Laaggemanipuleerde exfoliatie van grafeen over een groot oppervlak
Laaggemanipuleerde exfoliatie van grafeen over een groot oppervlak
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com