
Wetenschap
Hete nanodeeltjes voor kankerbehandelingen
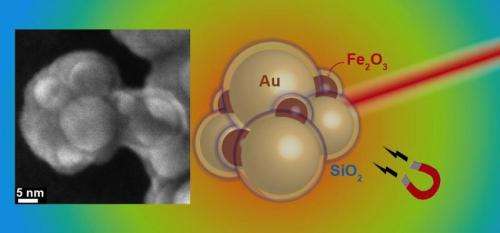
Regeling van goud- en ijzeroxide-aggregaten met silica-schaal. Links:elektronenmicroscopisch beeld van een aggregaat. Krediet:Georgios Sotiriou / ETH Zürich
Nanodeeltjes hebben veel potentie in de geneeskunde:voor diagnostiek, als vehikel voor werkzame stoffen of als middel om tumoren met hitte te doden. Onderzoekers van ETH Zürich hebben nu deeltjes ontwikkeld die relatief eenvoudig te produceren zijn en een breed scala aan toepassingen hebben.
Als je in het donker je hand over een ingeschakelde zaklamp houdt, het lijkt rood te gloeien. Dit komt doordat rode lichtstralen met een lange golflengte effectiever door het menselijk weefsel dringen dan blauw licht met een korte golflengte. ETH Zürich-onderzoekers exploiteren dit feit in een nieuw soort nanodeeltjes:zogenaamde plasmonische deeltjes, die opwarmen wanneer ze nabij-infraroodlicht absorberen. Dit zou hen in staat kunnen stellen om tumorweefsel met hitte te doden, bijvoorbeeld.
Goud is een populair materiaal voor therapeutisch gebruikte nanodeeltjes, omdat het goed wordt verdragen en gewoonlijk geen ongewenste reacties veroorzaakt. In de karakteristieke bol- of bolvorm van nanodeeltjes, echter, goud heeft niet de noodzakelijke eigenschappen om te werken als een plasmonisch deeltje dat voldoende absorbeert in het nabij-infrarode spectrum van licht om op te warmen. Om dit te doen, het moet in een speciale vorm worden gegoten, zoals een staaf of schelp, zodat de goudatomen een configuratie aannemen die bijna-infrarood licht begint te absorberen, waardoor warmte ontstaat. Het produceren van dergelijke nanostaafjes of nanoschillen in voldoende hoeveelheden, echter, is complex en duur.
Aggregaten in plaats van staven
Een team van onderzoekers onder leiding van Sotiris Pratsinis, Hoogleraar deeltjestechnologie aan de ETH Zürich, heeft nu een truc ontdekt om plasmonische gouddeeltjes in grote hoeveelheden te vervaardigen. Ze gebruikten hun bestaande knowhow over plasmonische nanodeeltjes en maakten bolvormige gouden nanodeeltjes die de gewenste nabij-infrarode plasmonische eigenschappen vertonen door ze te laten aggregeren. Elk deeltje is vooraf bedekt met een laag siliciumdioxide, die fungeert als een tijdelijke aanduiding tussen de afzonderlijke sferen in het aggregaat. Door de nauwkeurig gedefinieerde afstand tussen verschillende gouddeeltjes, de onderzoekers transformeren de deeltjes in een configuratie die nabij-infrarood licht absorbeert en zo warmte genereert.
"De schaal van siliciumdioxide heeft nog een ander voordeel", legt Georgios Sotiriou uit, eerste auteur van de studie en, tot voor kort, een postdoc in de onderzoeksgroep van Pratsinis en momenteel een Swiss National Science Foundation Fellow aan de Harvard University:"Het voorkomt dat de deeltjes vervormen wanneer ze opwarmen." Dit is een groot probleem met nanostaafjes. Als de staven hun vorm verliezen tijdens het opwarmen, ze verliezen hun gewenste plasmonische eigenschappen en zijn niet langer in staat om voldoende nabij-infrarood licht te absorberen om warmte te genereren.
De onderzoekers hebben de nieuwe deeltjes al getest op borstkankercellen in een petrischaal en ontdekten dat de nanodeeltjes na blootstelling aan nabij-infrarood licht voldoende werden opgewarmd om de cellen te doden, terwijl cellen overleefden in controle-experimenten (met deeltjes maar zonder straling en met straling maar zonder nanodeeltjes).
Combinatie met groot potentieel
Om de deeltjes gericht naar kankerweefsel te kunnen sturen, de onderzoekers mengden ook superparamagnetische ijzeroxidedeeltjes met de gouddeeltjes, waardoor de nanoaggregaten via magnetische velden kunnen worden gecontroleerd en hun accumulatie in een tumor kan versterken. Bovendien, dit opent de mogelijkheid om de aggregaten te verwarmen in diepe weefsellagen die infrarood licht niet meer kan bereiken via magnetische hyperthermie. Hier, de verwarming van de deeltjes wordt veroorzaakt door een magnetisch veld, waar de plus- en minpool elkaar snel afwisselen.
"Er moeten nog veel vragen worden beantwoord voordat de deeltjes bij mensen kunnen worden gebruikt", zegt Jean-Christophe Leroux, Professor in de formulering en levering van geneesmiddelen aan de ETH Zürich, die ook betrokken was bij het onderzoeksproject. Hoewel goud, siliciumdioxide en ijzeroxide worden goed verdragen, wat er in de loop van de tijd met de deeltjesaggregaten in het lichaam gebeurt - of ze zich nu ophopen in de lever of worden afgebroken en uitgescheiden, bijvoorbeeld – moet nog worden onderzocht.
De hybride ijzeroxide-goud nanodeeltjes zijn niet alleen in staat om tumorcellen door hitte te doden; ze kunnen ook worden gebruikt als contrastmiddel voor beeldvormingsprocessen in de diagnostiek door magnetische resonantiebeeldvorming, zoals onderzocht in samenwerking met het Universitair Ziekenhuis Zürich, of als onderdeel van een vehikel dat werkzame stoffen vervoert. "Je zou de deeltjes zelfs kunnen koppelen aan temperatuurgevoelige medicijndragers, waardoor het medicijn vrij zou kunnen komen als een bepaalde temperatuur werd overschreden", legt Sotiriou uit. Hierdoor zouden ongewenste neveneffecten op de rest van het lichaam kunnen worden verminderd of zelfs vermeden.
 Het fenomeen van polymorfisme in de atomaire structuur van het methylprednisolonaceponaat
Het fenomeen van polymorfisme in de atomaire structuur van het methylprednisolonaceponaat Spiegels regelen de chemische selectiviteit
Spiegels regelen de chemische selectiviteit Extreem hard en toch metaalgeleidend:onderzoekers ontwikkelen nieuw materiaal met hightech-perspectieven
Extreem hard en toch metaalgeleidend:onderzoekers ontwikkelen nieuw materiaal met hightech-perspectieven Morsen in een nucleaire faciliteit toont potentiële brandwondenrisico's van een huishoudelijke chemische stof
Morsen in een nucleaire faciliteit toont potentiële brandwondenrisico's van een huishoudelijke chemische stof Elements in the Biosphere
Elements in the Biosphere
 Tweederde van tropische bossen bedreigd in volgend decennium
Tweederde van tropische bossen bedreigd in volgend decennium Harvey, Irma weegt op september Amerikaans consumentenvertrouwen
Harvey, Irma weegt op september Amerikaans consumentenvertrouwen Weer een dagje aan het werk, in het oog van een orkaan
Weer een dagje aan het werk, in het oog van een orkaan EPA hoort zorgen over klimaat in hart van kolenland
EPA hoort zorgen over klimaat in hart van kolenland NASA identificeert een sterke tropische cycloon in de Arabische Zee Kyarr
NASA identificeert een sterke tropische cycloon in de Arabische Zee Kyarr
Hoofdlijnen
- Stappen van DNA-transcriptie
- Actief transport: een overzicht van primair en secundair
- Hoe slaapwandelen werkt
- Interferentie berekenen
- Federale overheid:geen lijst van bedreigde soorten voor walrus
- Hoe is DNA geordend om in een cel te passen?
- Cellulaire ademhaling: definitie, vergelijking en stappen
- Wat is de fusie van twee gameten om een diploïde zygoot te vormen?
- Stamcelplatform werpt nieuw licht op het begin van menselijke ontwikkeling
- Onderzoekers laten druppeltjes dansen (met video)

- Nieuwe elektronische biosensing-technologie kan een nieuw tijdperk van gepersonaliseerde geneeskunde mogelijk maken

- Moleculen gebruiken om nanodrums te ontstemmen
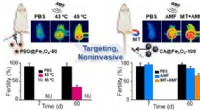
- Een omkeerbaar anticonceptiemiddel voor mannen, gericht op de testikels met magneten
- Het gebruik van perovskiet wordt een belangrijk kenmerk van de volgende generatie elektronische apparaten

 Slecht nieuws:CO2-uitstoot stijgt in 2018, zegt IEA-chef
Slecht nieuws:CO2-uitstoot stijgt in 2018, zegt IEA-chef Het conflict tussen energierenovatie en erfgoedkarakter verminderen
Het conflict tussen energierenovatie en erfgoedkarakter verminderen NASA ontdekt dat nieuwe tropische storm Selma veel regen kan veroorzaken
NASA ontdekt dat nieuwe tropische storm Selma veel regen kan veroorzaken Krachtige cycloon komt aan land in India
Krachtige cycloon komt aan land in India Kleine polymeerveren geven een boost aan het opruimen van het milieu
Kleine polymeerveren geven een boost aan het opruimen van het milieu Astronomen vinden Jupiter-achtige wolkenbanden op de dichtstbijzijnde bruine dwerg
Astronomen vinden Jupiter-achtige wolkenbanden op de dichtstbijzijnde bruine dwerg De geheime taal van olifanten
De geheime taal van olifanten  Oude stenen pilaren bieden aanwijzingen voor een inslag van een komeet die de menselijke geschiedenis heeft veranderd
Oude stenen pilaren bieden aanwijzingen voor een inslag van een komeet die de menselijke geschiedenis heeft veranderd
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

