
Wetenschap
DNA-nanorobots vinden en labelen cellulaire doelen
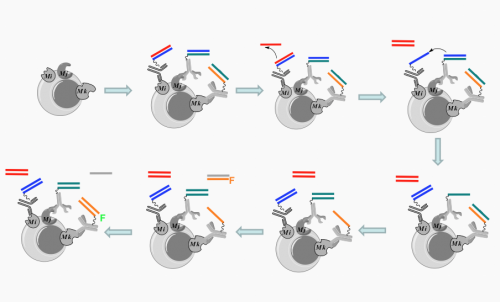
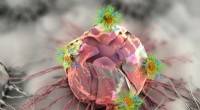
Deze afbeelding toont een moleculaire robot (automaat) in actie. Om cellen (grijze cirkel) te taggen die de Mi weergeven, Mj, en Mk-receptoren, er worden vijf verschillende onderdelen van een moleculaire robot ingezet. Elk van de eerste drie componenten bestaat uit DNA en een antilichaam; één antilichaam bindt aan elke receptor, zijn DNA (weergegeven door de gekleurde lijnen) dicht bij elkaar op de cel te brengen. De vierde DNA-component, weergegeven door de enkele rode lijn, start vervolgens een kettingreactie door de rode DNA-streng weg te trekken van het eerste antilichaam. Dat zorgt ervoor dat de blauwe DNA-streng van positie verandert, gevolgd door de groene DNA-streng. In de laatste stap, het laatste antilichaam trekt een fluorescerende DNA-streng (gelabeld F) van de vijfde component, het voltooien van de actie van de robot. Krediet:Milaan Stojanovic, Ph.D./Columbia Universitair Medisch Centrum
Onderzoekers van het Columbia University Medical Center, werken met hun medewerkers in het Ziekenhuis voor Speciale Chirurgie, hebben een vloot van moleculaire "robots" gecreëerd die zich kunnen richten op specifieke menselijke cellen en deze markeren voor medicamenteuze therapie of vernietiging.
De nanorobots - een verzameling DNA-moleculen, sommige gehecht aan antilichamen — werden ontworpen om een specifieke set menselijke bloedcellen te zoeken en een fluorescerend label aan de celoppervlakken te bevestigen. Details van het systeem werden op 28 juli gepubliceerd, 2013, in de online editie van Natuur Nanotechnologie .
"Dit opent de mogelijkheid om dergelijke moleculen te gebruiken om te richten, traktatie, of specifieke cellen doden zonder vergelijkbare gezonde cellen aan te tasten, " zei de senior onderzoeker van de studie, Milaan Stojanovic, doctoraat, universitair hoofddocent geneeskunde en biomedische technologie aan het Columbia University Medical Center. "Bij ons experiment we hebben de cellen gelabeld met een fluorescerende marker; maar we zouden dat kunnen vervangen door een medicijn of door een toxine om de cel te doden."
Hoewel andere DNA-nanorobots zijn ontworpen om medicijnen aan cellen te leveren, het voordeel van de vloot van Stojanovic is het vermogen om celpopulaties te onderscheiden die geen enkel onderscheidend kenmerk delen.
Cellen, inclusief kankercellen, bezit zelden een enkele, exclusieve functie die hen onderscheidt van alle andere cellen. Dit maakt het moeilijk om medicijnen te ontwerpen zonder bijwerkingen. Geneesmiddelen kunnen worden ontworpen om kankercellen te targeten met een specifieke receptor, maar gezonde cellen met dezelfde receptor zullen ook worden aangevallen.
De enige manier om cellen nauwkeuriger te targeten, is door cellen te identificeren op basis van een verzameling kenmerken. "Als we zoeken naar de aanwezigheid van vijf, zes, of meer eiwitten op het celoppervlak, we kunnen selectiever zijn, " Dr. Stojanovic zei. Grote celsorteermachines hebben het vermogen om cellen te identificeren op basis van meerdere eiwitten, maar tot nu toe, moleculaire therapieën hebben dat vermogen niet gehad.
Hoe het werkt
In plaats van een enkel complex molecuul te bouwen om meerdere kenmerken van een celoppervlak te identificeren, Dr. Stojanovic en zijn collega's van Columbia gebruikten een andere, en mogelijk gemakkelijker, benadering gebaseerd op meerdere eenvoudige moleculen, die samen een robot (of automaat, zoals de auteurs het liever noemen).
Om een cel te identificeren die drie specifieke oppervlakte-eiwitten bezit, Dr. Stojanovic construeerde eerst drie verschillende componenten voor moleculaire robots. Elke component bestond uit een stuk dubbelstrengs DNA dat was vastgemaakt aan een antilichaam dat specifiek was voor een van de oppervlakte-eiwitten. Wanneer deze componenten worden toegevoegd aan een verzameling cellen, de antilichaamdelen van de robot binden aan hun respectievelijke eiwitten (in de figuur, CD45, CD3, en CD8) en werken in overleg.
Op cellen waar alle drie de componenten zijn bevestigd, een robot is functioneel en een vierde component (hieronder aangeduid met 0) zet een kettingreactie op gang tussen de DNA-strengen. Elke component verwisselt een DNA-streng met een andere, tot het einde van de ruil, wanneer het laatste antilichaam een DNA-streng verkrijgt die fluorescent gelabeld is.
Aan het einde van de kettingreactie - die minder dan 15 minuten duurt in een monster van menselijk bloed - worden alleen cellen met de drie oppervlakte-eiwitten gelabeld met de fluorescerende marker.
"We hebben ons concept met bloedcellen gedemonstreerd omdat hun oppervlakte-eiwitten goed bekend zijn, maar in principe kunnen onze moleculen overal in het lichaam worden ingezet, " zei Dr. Stojanovic. Bovendien, het systeem kan worden uitgebreid om er vier te identificeren, vijf, of zelfs meer oppervlakte-eiwitten.
Nu moeten de onderzoekers aantonen dat hun moleculaire robots werken in een levend dier; de volgende stap zijn experimenten met muizen.
 Hoe hebben mensen onze planeten beïnvloed Onze planeten Biodiversiteit op zowel positieve als negatieve manieren?
Hoe hebben mensen onze planeten beïnvloed Onze planeten Biodiversiteit op zowel positieve als negatieve manieren?  Mariene microvezels:minder plastic dan voorspeld
Mariene microvezels:minder plastic dan voorspeld Wetenschappers maken grote doorbraak in omega-3-productie
Wetenschappers maken grote doorbraak in omega-3-productie Je kunt je bord hebben en het ook opeten, zegt Poolse uitvinder
Je kunt je bord hebben en het ook opeten, zegt Poolse uitvinder Waarom we de Groenlandse ijskap misschien kunnen redden
Waarom we de Groenlandse ijskap misschien kunnen redden
Hoofdlijnen
- Rollende dobbelstenen voor specificatie van celgrootte in epidermis van planten
- Glycosylering - onbekend terrein in kaart brengen
- De controverse over de menselijke hersenen die nieuwe cellen maken
- Onderzoek toont aan dat commerciële oogst van brekende schildpadden leidt tot bevolkingsafname
- Anabolisch versus katabolisch (celmetabolisme): definitie en voorbeelden
- Hoe groeit schimmel op brood?
- Biosfeer: definitie, hulpbronnen, cycli, feiten en voorbeelden
- Zelfgemaakte UV-sterilisator
- Genetisch verhogen van de voedingswaarde van maïs kan miljoenen ten goede komen
- Onderzoekers stellen strategie voor om fotothermische therapie van tumoren in realtime te evalueren
- Nieuw onderzoek maakt gebruik van buitengewone eigenschappen van grafeen

- Een high-yieldmethode voor het samenstellen van gerichte nanodeeltjesclusters
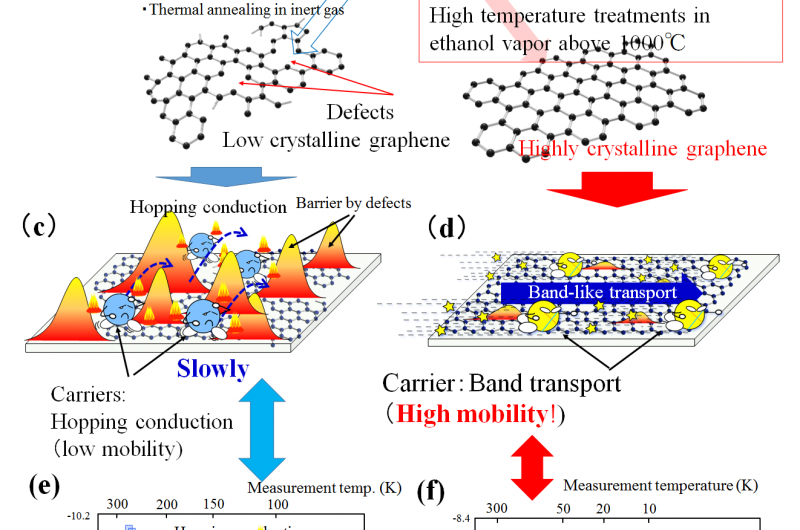
- Een veelbelovende route naar de schaalbare productie van zeer kristallijne grafeenfilms
- Patch levert medicijn, gen, en op licht gebaseerde therapie voor tumorlocaties
 Kosmische lens onthult vaag radiostelsel
Kosmische lens onthult vaag radiostelsel Potentieel voor natuurlijke hergroei van bossen om koolstof vast te leggen
Potentieel voor natuurlijke hergroei van bossen om koolstof vast te leggen Boeing B-17
Boeing B-17  Microfossiele spectroscopie dateert de eerste dieren op aarde
Microfossiele spectroscopie dateert de eerste dieren op aarde Oceaantemperatuur gereconstrueerd in de afgelopen 700, 000 jaar
Oceaantemperatuur gereconstrueerd in de afgelopen 700, 000 jaar Houtdichtheid van Europese bomen neemt sinds 1870 voortdurend af
Houtdichtheid van Europese bomen neemt sinds 1870 voortdurend af Echografie kan kankercellen selectief doden
Echografie kan kankercellen selectief doden Virussen delen genen met organismen in de levensboom
Virussen delen genen met organismen in de levensboom
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

