
Wetenschap
Silicium-koolstofelektroden klikken, zwellen, niet knallen

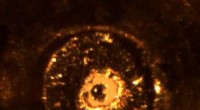
Deze composietafbeelding toont een silicium-koolstof nanovezelelektrode voor (links) en nadat (rechts) wordt geladen met lithiumionen. Krediet:Chongmin Wang
Een studie die een nieuw type silicium-koolstof nanocomposiet-elektrode onderzoekt, onthult details over hoe ze werken en hoe herhaald gebruik ze zou kunnen verslijten. Het onderzoek geeft ook aanwijzingen waarom dit materiaal beter presteert dan alleen silicium. Met een elektrische capaciteit die vijf keer hoger is dan die van conventionele lithiumbatterij-elektroden, silicium-koolstof nanocomposiet-elektroden kunnen leiden tot duurzamere, goedkopere oplaadbare batterijen voor elektrische voertuigen.
Online gepubliceerd in het tijdschrift Nano-letters vorige week, de studie omvat video's van de elektroden die worden opgeladen met een resolutie op nanometerschaal. Door ze in gebruik te bekijken, kunnen onderzoekers de sterke en zwakke punten van het materiaal begrijpen.
"De elektroden zetten uit als ze worden opgeladen, en dat verkort de levensduur van de batterij, " zei hoofdonderzoeker Chongmin Wang van het Pacific Northwest National Laboratory van het Department of Energy. "We willen leren hoe we hun levensduur kunnen verbeteren, omdat silicium-koolstof nanovezelelektroden een groot potentieel hebben voor oplaadbare batterijen."
Plus minus
Silicium heeft zowel voor- als nadelen voor gebruik als batterijmateriaal. Het heeft een hoge capaciteit voor energieopslag, dus het kan een flinke lading krijgen. Het probleem van silicium, Hoewel, is dat het opzwelt wanneer het wordt opgeladen, uitzetten tot 3 keer de ontladen grootte. Als siliciumelektroden stevig in een batterij zijn verpakt, deze uitbreiding kan ervoor zorgen dat de batterijen barsten. Sommige onderzoekers onderzoeken elektroden van nanoformaat die beter presteren in zulke krappe ruimtes.
Een groep met meerdere instellingen onder leiding van Wang van PNNL besloot elektroden van nanoformaat te testen, bestaande uit koolstofnanovezels bedekt met silicium. De hoge geleidbaarheid van de koolstof, die elektriciteit laat stromen, vormt een mooie aanvulling op de hoge capaciteit van silicium, die het opslaat.
Onderzoekers van het Oak Ridge National Laboratory van DOE in Oak Ridge, Tenn., Toegepaste Wetenschappen Inc. in Cedarville, Ohio, en General Motors Global R&D Center in Warren, Mich. creëerde koolstofnanovezels met een dunne laag silicium eromheen. Ze leverden de elektroden aan het team van PNNL om hun gedrag tijdens het functioneren te onderzoeken.
Eerst, Wang en collega's testten hoeveel lithium de elektroden konden bevatten en hoe lang ze meegingen door ze in een kleine testbatterij, een halve cel genaamd, te plaatsen. Na 100 laad-ontlaadcycli, de elektroden behielden nog steeds een zeer goede capaciteit van ongeveer 1000 milliAmp-uur per gram materiaal, vijf tot tien keer de capaciteit van conventionele elektroden in lithium-ionbatterijen.
Hoewel ze goed presteerden, het team vermoedde dat de uitzetting en krimp van het silicium een probleem zou kunnen zijn voor de levensduur van de batterij, omdat rekken de neiging heeft om dingen te verslijten. Om te bepalen hoe goed de elektroden het herhaalde rekken doorstaan, Wang liet een speciaal ontworpen, kleine batterij in een transmissie-elektronenmicroscoop, die objecten nanometers breed kan bekijken, in DOE's EMSL, het Environmental Molecular Sciences Laboratory op de PNNL-campus.
Ze zoomden in op de elektrode van de kleine batterij met behulp van een nieuwe microscopie die werd gefinancierd door de Recovery Act. Met deze microscoop kon het team de gebruikte elektrode bestuderen, en ze maakten foto's en video's terwijl de kleine batterij werd opgeladen en ontladen.
Geen kristalglas
Eerder werk heeft aangetoond dat opladen ervoor zorgt dat lithiumionen in het silicium stromen. In dit onderzoek, de lithiumionen stroomden in de siliciumlaag langs de lengte van de koolstofnanovezel met een snelheid van ongeveer 130 nanometer per seconde. Dit is ongeveer 60 keer sneller dan alleen silicium, wat suggereert dat de onderliggende koolstof de laadsnelheid van silicium verbetert.
Zoals verwacht, de siliciumlaag zwol ongeveer 300 procent op toen het lithium binnenkwam. Echter, de combinatie van de koolstofdrager en de ongestructureerde kwaliteit van het silicium zorgde ervoor dat het gelijkmatig kon zwellen. Dit steekt gunstig af bij silicium alleen, die ongelijkmatig opzwelt, onvolkomenheden veroorzaken.
Naast zwelling, Van lithium is bekend dat het andere veranderingen in het silicium veroorzaakt. De combinatie van lithium en silicium vormt aanvankelijk een ongestructureerd, glasachtige laag. Vervolgens, wanneer de lithium-siliciumverhouding 15 tot 4 bereikt, de glazige laag kristalliseert snel, zoals eerder werk van andere onderzoekers heeft aangetoond.
Wang en collega's onderzochten het kristallisatieproces in de microscoop om het beter te begrijpen. In de microscoopvideo ze konden de kristallisatievooruitgang zien terwijl het lithium het silicium vulde en de 15 tot 4 verhouding bereikte.
Ze ontdekten dat deze kristallisatie anders is dan de klassieke manier waarop veel stoffen kristalliseren, die vanaf een startpunt bouwt. Liever, de lithium- en siliciumlaag knapten in één keer in een kristal toen de verhouding precies 15 tegen 4 bereikte. Computeranalyses van deze kristallisatie bevestigden het pittige karakter ervan, een soort kristallisatie die bekend staat als congruente faseovergang.
Maar de kristallisatie was niet permanent. Bij het lossen, het team ontdekte dat de kristallaag weer glazig werd, terwijl de lithiumconcentratie op zijn weg uit het silicium daalde.
Om te bepalen of herhaald gebruik zijn sporen op de elektrode heeft achtergelaten, het team laadde en ontlaadde de kleine batterij 4 keer. Vergelijking van hetzelfde gebied van de elektrode tussen de eerste en vierde lading, het team zag het oppervlak ruw worden, vergelijkbaar met een weg met kuilen.
De oppervlakteveranderingen waren waarschijnlijk te wijten aan lithiumionen die een beetje schade achterlieten bij het ontladen, zei Wang. "We kunnen zien dat het oppervlak van de elektrode van glad naar ruw gaat terwijl we het opladen en ontladen. We denken terwijl het fietst, kleine defecten optreden, en de gebreken stapelen zich op."
Maar het feit dat de siliciumlaag erg dun is, maakt hem duurzamer dan dikker silicium. In dik silicium, de gaten die lithiumionen achterlaten, kunnen samenkomen om grote holten te vormen. "In het huidige ontwerp omdat het silicium zo dun is, je krijgt geen grotere gaatjes, net zoals kleine gasbelletjes in ondiep water naar de oppervlakte komen. Als het water diep is, de bubbels komen samen en vormen grotere bubbels."
Bij toekomstig werk, onderzoekers hopen de dikte van de siliciumlaag te onderzoeken en hoe goed deze hecht aan de onderliggende koolstof om de prestaties en levensduur van de elektroden te optimaliseren.
 Onderzoek in Hong Kong waarschuwt voor gezondheidsrisico's van zonnebrandcrème
Onderzoek in Hong Kong waarschuwt voor gezondheidsrisico's van zonnebrandcrème NASA analyseert nieuwe tropische depressie in het oosten van de Stille Oceaan 7E
NASA analyseert nieuwe tropische depressie in het oosten van de Stille Oceaan 7E Virtual reality gebruiken om stedelijk groen in kaart te brengen
Virtual reality gebruiken om stedelijk groen in kaart te brengen Grote stormclusters nemen toe - wat dit betekent voor orkaanhotspots
Grote stormclusters nemen toe - wat dit betekent voor orkaanhotspots Holoceentemperatuur op het Iberisch schiereiland gereconstrueerd met subfossielen van insecten
Holoceentemperatuur op het Iberisch schiereiland gereconstrueerd met subfossielen van insecten
Hoofdlijnen
- Wat gebeurt er met een cel als het DNA-chromosomen niet kopieert voordat het zich splitst?
- Uit welke elementen bestaat glucose?
- Het unieke pentraxine-koolzuuranhydrase-eiwit reguleert het vermogen van vissen om te zwemmen
- Hoe beïnvloeden je hersenen je overlevingskansen in de wildernis?
- Definitie van celoppervlakte-eiwitten
- Wat een grote handtekening kan zeggen over je persoonlijkheid
- Opkomende ziekte brengt Noord-Amerikaanse kikkers verder in gevaar
- Sommige lemuren zijn eenlingen, anderen hunkeren naar verbinding
- Soorten organellen
- Roterende nanobuismotoren bieden een glimp van toekomstige nanodevices

- Gekleurde zonnecellen kunnen beeldschermen efficiënter maken

- Elektrisch schakelbare qubit kan afstemmen tussen opslag- en snelle berekeningsmodi

- Diamanten helpen bij het genereren van een nieuw record voor statische druk voor studie
- Onderzoekers stellen structuur vast van nieuwe superharde vorm van koolstof

 De geheime oorsprong van China's 40-jarenplan om een einde te maken aan de CO2-uitstoot
De geheime oorsprong van China's 40-jarenplan om een einde te maken aan de CO2-uitstoot Rotatievorm van spontane kristallografische ordening ontdekt in ferro-materiaal
Rotatievorm van spontane kristallografische ordening ontdekt in ferro-materiaal Woestijnhagedissen gebruiken lichaamstrillingen om in zand te duiken (update)
Woestijnhagedissen gebruiken lichaamstrillingen om in zand te duiken (update) Nintendo-verkopen in de eerste helft stijgen door sterke vraag naar Switch-games
Nintendo-verkopen in de eerste helft stijgen door sterke vraag naar Switch-games Wetenschappers worden gezien als betrouwbare experts wanneer ze hun werk delen in online video's
Wetenschappers worden gezien als betrouwbare experts wanneer ze hun werk delen in online video's Metal Organic Framework (MOF) microkristallen voor meerkleurige breedbandlasing
Metal Organic Framework (MOF) microkristallen voor meerkleurige breedbandlasing Bladverliezende Bos Biome Feiten voor Kids
Bladverliezende Bos Biome Feiten voor Kids NASA's Mars 2020 zal jagen op microscopisch kleine fossielen
NASA's Mars 2020 zal jagen op microscopisch kleine fossielen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

