
Wetenschap
Kan de atomaire massa van een bepaald element ooit veranderen?
* isotopen: De atoommassa op het periodiek systeem is de gemiddelde atoommassa , rekening houdend met de overvloed van alle natuurlijk voorkomende isotopen van dat element. Isotopen zijn atomen van hetzelfde element met verschillende aantallen neutronen en dus verschillende atoommassa's. Koolstof heeft bijvoorbeeld twee hoofdisotopen:koolstof-12 (met 6 neutronen) en koolstof-14 (met 8 neutronen). De atoommassa van koolstof op het periodiek systeem is 12.011 AMU, hetgeen de relatieve overvloed van deze isotopen weerspiegelt.
* Nucleaire reacties: Atomische massa kan veranderen tijdens nucleaire reacties, zoals nucleaire splijting of fusie. Deze reacties omvatten veranderingen in de kern van een atoom, wat kan leiden tot het creëren van nieuwe elementen met verschillende atoommassa's.
* Radioactief verval: Bepaalde isotopen van een element zijn radioactief en ondergaan radioactief verval, wat de atomaire massa kan veranderen. Cool-14 vervalt bijvoorbeeld in stikstof-14, waardoor de atomaire massa van het atoom verandert.
De atomaire massa van een individueel atoom van een specifieke isotoop is echter vast . Een koolstof-12-atoom heeft bijvoorbeeld altijd een atoommassa van 12 AMU, en een koolstof-14-atoom zal altijd een atoommassa van 14 AMU hebben.
Daarom kan de atomaire massa van een bepaald element op macroscopisch niveau veranderen vanwege de aanwezigheid van verschillende isotopen of nucleaire reacties. De atomaire massa van een individueel atoom van een specifieke isotoop is echter gefixeerd.
 Eiwitten als shuttleservice voor gerichte medicatietoediening
Eiwitten als shuttleservice voor gerichte medicatietoediening Goedkoop, energiezuinige en schone reactie om chemische grondstof te maken
Goedkoop, energiezuinige en schone reactie om chemische grondstof te maken Hoe vind je het aantal protrons en elektronen in een atoom?
Hoe vind je het aantal protrons en elektronen in een atoom?  Nieuwe, door licht aangedreven katalysatoren kunnen helpen bij de productie
Nieuwe, door licht aangedreven katalysatoren kunnen helpen bij de productie Elementen zijn samengesteld uit atomen en verbindingen van?
Elementen zijn samengesteld uit atomen en verbindingen van?
 Voor het behoud van koraalriffen zijn nieuwe technologieën nodig
Voor het behoud van koraalriffen zijn nieuwe technologieën nodig Klimaatrecords worden steeds weer verbroken. Dit is wat u moet weten
Klimaatrecords worden steeds weer verbroken. Dit is wat u moet weten  Studie:Bosbranden veroorzaakten tot de helft van de vervuiling in het westen van de VS
Studie:Bosbranden veroorzaakten tot de helft van de vervuiling in het westen van de VS COVID-19 lockdown benadrukt ozonchemie in China
COVID-19 lockdown benadrukt ozonchemie in China Inzicht in alternatieve redenen om klimaatverandering te ontkennen, kan helpen om de kloof te overbruggen
Inzicht in alternatieve redenen om klimaatverandering te ontkennen, kan helpen om de kloof te overbruggen
Hoofdlijnen
- Welk lichaamssysteem trekt lucht in het lichaam?
- Retrovirus versus DNA-virus
- Vijf soorten genverbindingsmechanismen
- Wat was er eerst:twee- of driecellig stuifmeel? Nieuw onderzoek actualiseert een klassiek debat
- Protozoa Welke bewegen door een zweepachtig orgel?
- Hoe een jetlag werkt
- Wat bevat bundels buisachtige cellen die water en voedsel vervoeren?
- Onderzoekers construeren het meest complexe, volledig synthetische microbioom
- Waar verbouw je microben in?
- Uitgebreide tests met levitated force-sensor vinden geen bewijs van vijfde kracht
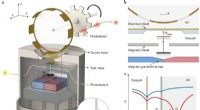
- Een grote uitdaging voor het oogsten van fusie-energie op aarde

- Halfmetalen zijn hoge geleiders

- Uw rijpositie kan u een voordeel geven in een sprint op de weg, uit onderzoek blijkt

- Turbulentie is niet alleen een wetenschappelijk probleem

 Wat zijn de intermoleculaire aantrekkingskrachten binnen pentaan?
Wat zijn de intermoleculaire aantrekkingskrachten binnen pentaan?  Hoe zorgwekkend is het dat vogelgriep overspringt naar melkkoeien? Dit is wat experts zeggen
Hoe zorgwekkend is het dat vogelgriep overspringt naar melkkoeien? Dit is wat experts zeggen  Cataclysmische variabele V1460 Her heeft een snel ronddraaiende witte dwerg die opgroeit van een geëvolueerde donorster, studie vondsten
Cataclysmische variabele V1460 Her heeft een snel ronddraaiende witte dwerg die opgroeit van een geëvolueerde donorster, studie vondsten Waarom zijn planten groen? Model van onderzoeksteams reproduceert fotosynthese
Waarom zijn planten groen? Model van onderzoeksteams reproduceert fotosynthese Demonstranten van de Hawaii-telescoop deinzen niet terug na arrestaties
Demonstranten van de Hawaii-telescoop deinzen niet terug na arrestaties Wetenschappers werpen nieuw licht op hoe zeevogels door lucht en water reizen
Wetenschappers werpen nieuw licht op hoe zeevogels door lucht en water reizen  Redstone-familie blokkeert verhuizing om de stemkracht van CBS af te zwakken
Redstone-familie blokkeert verhuizing om de stemkracht van CBS af te zwakken Sterke aardbeving verwondt 2, slaat dakpannen af in Japan
Sterke aardbeving verwondt 2, slaat dakpannen af in Japan
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

