
Wetenschap
Een membraan met poriën op nanoschaal zorgt voor gecontroleerde afgifte van zweetstimulans
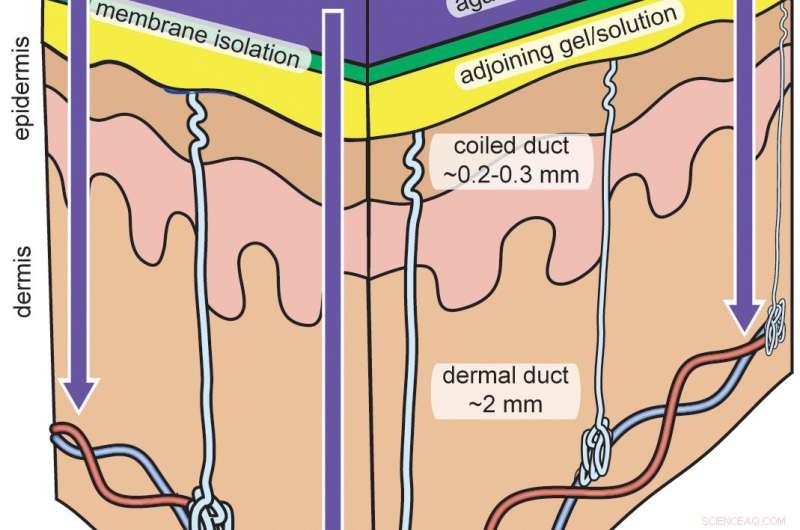
In vivo testen van membraantechnologie met behulp van iontoforese. Krediet:Phillip Simmers, Zachary Sonner en Jason Heikenfeld
Als mensen zweten, ze geven onbewust een breed scala aan chemicaliën vrij die clinici op niet-invasieve wijze kunnen informeren over alles, van stresshormoonspiegels tot glucose. Maar het is moeilijk voor onderzoekers om deze informatie te verzamelen, tenzij je veel zweet. Opkomende draagbare apparaten die stimulerende gels gebruiken, hebben gezorgd voor een manier om lokaal zweet op het lichaam te induceren. Echter, zweet kan deze gels verdunnen, die hun levensvatbaarheid op lange termijn aantasten.
Een internationaal team van onderzoekers heeft onlangs een nieuw membraan ontwikkeld dat zowel problemen die voortvloeien uit direct huidcontact als zweetverdunning voor zweetbiosensoren verzacht. Zoals besproken in Biomicrofluïdica , het membraan presteert honderden keren beter dan andere methoden en is bestand tegen herhaald gebruik.
"Het dagelijkse gebruik van zweet-biosensing is aan de horizon, maar eerst moeten we een paar problemen oplossen, inclusief het verkrijgen van bruikbare monsters wanneer patiënten zich niet inspannen, zei Philip Simmers, een auteur op papier. "Gecontroleerde dosering is erg belangrijk voor de medische gemeenschap."
Iontoforetische apparaten - die op het membraan van het team zouden trekken - werken door een kleine spanning over de huid aan te brengen om een geladen medicijn door de epidermis te leiden. De meeste apparaten voor zweetstimulatie gebruiken een stimulerend middel dat in hoge concentraties wordt opgelost in een hydrogel om ervoor te zorgen dat de dosering kan worden gehandhaafd.
Hoewel stimulerende middelen zoals carbachol nuttig zijn omdat het lichaam ze langzaam metaboliseert, ze kunnen niet specifiek gericht zijn op zweetklieren en vormen een potentieel risico als een extra stimulerend middel in het lichaam komt. Wanneer het stimulerende middel de zweetproductie activeert, de resulterende melange van hydrogel en zweet maakt het niet alleen moeilijk voor het stimulerende middel om de huid te bereiken, maar ook voor de biosensor om het zweet nauwkeurig af te lezen.
"Een van de grootste uitdagingen was dat wanneer we zweten, we verliezen actief analyten aan de gel, wat een probleem is dat niet is aangepakt, ' zei Simmers.
Simmers en zijn team construeerden eerst een in vitro model om te bepalen welke commercieel beschikbare filtratiemembranen het meest geschikt waren om de passieve diffusie van carbachol te beperken. Ze ontdekten dat de beste membranen poriën op nanoschaal hadden en na 24 uur meer dan 90 procent van hun aanvankelijke stimulerende concentratie vasthielden. terwijl het slechts een minimale hoeveelheid zweet doorlaat.
De groep bracht deze technologie vervolgens over naar zelfklevende pleisters ter grootte van een dubbeltje en testte ze op patiënten. Met behulp van broomfenolblauwe kleurstof en siliconenolie die van kleur verandert in aanwezigheid van zweet, ze konden bevestigen dat de poriën op nanoschaal die eerder tijdens hun in vitro-experimenten werden geïdentificeerd, nog steeds een gecontroleerde dosering konden leveren die de menselijke zweetreactie veroorzaakte, wat aantoont dat het membraan het zweet effectief isoleerde van het stimulerende middel.
Volgende, de groep hoopt hun bevindingen op te nemen in een draagbaar biosensing-prototype dat ze al hebben ontwikkeld. Simmers zei dat hij hoopt dat de bevindingen van het artikel ook de interesse zullen wekken in hoe membraanmaterialen voor dergelijke apparaten beter kunnen worden geproduceerd.
 Op kobalt gebaseerde katalysatoren kunnen de productie van waterstof uit water op industriële schaal versnellen
Op kobalt gebaseerde katalysatoren kunnen de productie van waterstof uit water op industriële schaal versnellen Hoe een chemische formule te schrijven
Hoe een chemische formule te schrijven Een supermateriaal dat toepasbaar is op batterijen en andere apparaten voor energieconversie
Een supermateriaal dat toepasbaar is op batterijen en andere apparaten voor energieconversie Molybdeen-titaancarbide levensvatbaar in additieve productie
Molybdeen-titaancarbide levensvatbaar in additieve productie Hout omzetten in farmaceutische ingrediënten
Hout omzetten in farmaceutische ingrediënten
 Analyse van het geretourneerde kernmonster van Stonehenge helpt de duurzaamheid van megalieten te verklaren
Analyse van het geretourneerde kernmonster van Stonehenge helpt de duurzaamheid van megalieten te verklaren Wat eten wilde vogels?
Wat eten wilde vogels?  Zee van wit:honderdduizenden vissen dood in Australië
Zee van wit:honderdduizenden vissen dood in Australië Wetenschappers presenteren nieuwe methode voor teledetectie van atmosferische dynamiek
Wetenschappers presenteren nieuwe methode voor teledetectie van atmosferische dynamiek Sterkere westenwind waait slechte wind voor klimaatverandering
Sterkere westenwind waait slechte wind voor klimaatverandering
Hoofdlijnen
- Nieuw model bevestigt dat bedreigde rechtse walvissen afnemen
- Hoe worden restrictie-enzymen gebruikt?
- 6 soorten vrij beweegbare gewrichten
- Studie onthult verschillen in belangrijke evoluties van het genoom van gewassen
- Muggendarmbacteriën kunnen aanwijzingen bieden voor malariabestrijding
- Video van vier bobcats in een buitenwijk toont gezonde populatie
- Hoe maak je een 3D-tandmodel voor een schoolproject
- Waarom verplaatsen chloroplasten zich in Elodea?
- Wat gebeurt er met cellen vanwege een natriumbalans?
- Supersnel kwantumgeheugen voor fotonen

- Controle van de optische eigenschappen van vaste stoffen met akoestische golven

- Projecten voor het zonnestelsel voor kinderen maken

- Onderzoekers ontcijferen de dynamiek van elektronen in perovskietkristallen
- Wetenschappers onthullen reactiemechanisme van 11Be-kern

 Google zegt dat partner geheime Nederlandse gegevens heeft gelekt
Google zegt dat partner geheime Nederlandse gegevens heeft gelekt Heeft Columbus echt syfilis in Europa geïntroduceerd?
Heeft Columbus echt syfilis in Europa geïntroduceerd? Waarom een koolstofprijs alleen niet genoeg zal zijn om de uitstoot van Nieuw-Zeeland te verlagen?
Waarom een koolstofprijs alleen niet genoeg zal zijn om de uitstoot van Nieuw-Zeeland te verlagen? Real-world toepassingen voor atom interferometrische kwantumsensoren
Real-world toepassingen voor atom interferometrische kwantumsensoren Schimmelwegen op kaaskorst beïnvloeden voedselveiligheid, rijpheid
Schimmelwegen op kaaskorst beïnvloeden voedselveiligheid, rijpheid Kroatische top oesterkwekers in paniek na gevonden norovirus
Kroatische top oesterkwekers in paniek na gevonden norovirus Computermodellering van WNK-kinaseremmers kan nieuwe hulpmiddelen bieden voor het begrijpen van hypertensie
Computermodellering van WNK-kinaseremmers kan nieuwe hulpmiddelen bieden voor het begrijpen van hypertensie Model werpt nieuw licht op de vorming van terrestrische planeten en de aarde
Model werpt nieuw licht op de vorming van terrestrische planeten en de aarde
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Dutch | Norway | Swedish | German | Danish |

-
Wetenschap © https://nl.scienceaq.com

