
Wetenschap
Wat zijn de USP -limieten van hardheidstabletten?
Dit is waarom:
* tablethardheid is geen gestandaardiseerde test in de USP. De USP (United States Pharmacopeia) biedt richtlijnen voor desintegratie- en ontbindingstesten, die essentieel zijn voor het vrijgeven van geneesmiddelen.
* Hardheid is een productspecifieke parameter. Het acceptabele hardheidsbereik voor een tablet hangt af van factoren zoals:
* Drugskenmerken: Sommige medicijnen zijn gevoeliger voor pletten of slijtage dan andere.
* Doseringsvorm: Tabletten met verschillende coatings, maten en vormen hebben verschillende hardheidseisen.
* productieproces: De compressiekracht die wordt gebruikt tijdens de productie van tablets, heeft direct invloed op de hardheid.
* Hardheid wordt vaak bepaald door de fabrikant. Bedrijven stellen interne specificaties in op basis van hun specifieke behoeften en de eigenschappen van het medicijn.
Er zijn echter enkele algemene overwegingen voor tablethardheid:
* te zacht: Tabletten die te zacht zijn, kunnen gemakkelijk breken, wat leidt tot inconsistente dosering en potentiële problemen met de behandeling.
* te hard: Extreem harde tabletten mogen mogelijk niet goed in de maag uiteenvallen, waardoor het afgifte van drugs wordt vertraagd of belemmert.
Samenvattend:
* De USP definieert geen specifieke hardheidslimieten voor tablets.
* Het acceptabele hardheidsbereik varieert sterk, afhankelijk van het individuele medicijn en de formulering ervan.
* Fabrikanten bepalen de specificaties van hardheid op basis van hun eigen kwaliteitscontrolenormen.
Als u specifieke informatie nodig hebt over hardheidslimieten voor een bepaald medicijn, moet u verwijzen naar de relevante productmonografie of contact opnemen met de fabrikant.
 Eén atmosferische verbinding is, nadat deze in water is opgelost, verantwoordelijk voor zowel de algemene zuurgraad van normaal regenwater als van veel grond. Wat is deze verbinding?
Eén atmosferische verbinding is, nadat deze in water is opgelost, verantwoordelijk voor zowel de algemene zuurgraad van normaal regenwater als van veel grond. Wat is deze verbinding?  Hoeveel protonen heeft een atoom van Co-60?
Hoeveel protonen heeft een atoom van Co-60?  Wat is de naam van samengestelde CH3 CH2 BR?
Wat is de naam van samengestelde CH3 CH2 BR?  Nabij-infrarood fotoactiveerbare oxygenatiekatalysatoren van amyloïde peptide
Nabij-infrarood fotoactiveerbare oxygenatiekatalysatoren van amyloïde peptide Schone lucht is een homogeen mengsel?
Schone lucht is een homogeen mengsel?
 In de roos:de Golf bereidt zich voor op Laura om als orkaan te slaan
In de roos:de Golf bereidt zich voor op Laura om als orkaan te slaan Verspil niet, wil niet - nieuwe benaderingen van verlaten voedsel
Verspil niet, wil niet - nieuwe benaderingen van verlaten voedsel De wetenschap is duidelijk:we moeten vandaag beginnen met het creëren van onze koolstofarme toekomst
De wetenschap is duidelijk:we moeten vandaag beginnen met het creëren van onze koolstofarme toekomst Wat is een voorbeeld van mutualisme in het park?
Wat is een voorbeeld van mutualisme in het park?  Milieuproblemen veroorzaakt door mineralen
Milieuproblemen veroorzaakt door mineralen
Hoofdlijnen
- Welke effecten kunnen glycolyse remmen?
- Wat zijn de functies van mitochondrion in plantencel?
- Wolf huilen? Debat over de aanwezigheid van wolven in het noordoosten
- Wat zijn de voordelen van genetische variatie en welk potentieel probleem dat het kan veroorzaken?
- Vergeet uw huisdieren niet tijdens koud weer
- Wat is het verschil tussen een detective en wetenschapper?
- Wat is de rol van dieren in de koolstofcyclus?
- Wat fossielen onthullen over hybridisatie van vroege mensen
- Waarom zijn Archegonia en Antheridia tegelijkertijd volwassen op een Prothallus?
- VAE versoepelt beperkingen, maar de meeste populaire apps zijn nog steeds geblokkeerd

- Onderzoekers onderzoeken deeltjesemissies van 3D-printers, veiligheidstips

- Legeronderzoeker bevordert samenwerking tussen mensen, autonome machines

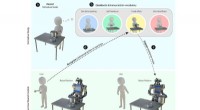
- Gedeelde controle stelt een robot in staat om twee handen te gebruiken die samenwerken om taken uit te voeren
- Mensen hoeven niet te solliciteren

 10 coole dingen over Neil deGrasse Tyson
10 coole dingen over Neil deGrasse Tyson  Neurowetenschap opent de zwarte doos van kunstmatige intelligentie
Neurowetenschap opent de zwarte doos van kunstmatige intelligentie Afbeelding:Het geval van de rotsblokken op Mars
Afbeelding:Het geval van de rotsblokken op Mars Hoe kunnen we de mondiale visserij vijf keer zoveel waard maken:studie?
Hoe kunnen we de mondiale visserij vijf keer zoveel waard maken:studie?  Wetenschappers brengen in kaart welke factoren de nieuwsagenda beïnvloeden
Wetenschappers brengen in kaart welke factoren de nieuwsagenda beïnvloeden  SpaceX gaat van start tijdens de 35e Space Coast-lancering van het jaar
SpaceX gaat van start tijdens de 35e Space Coast-lancering van het jaar  Supercycloon Amphan treft Bangladesh, India
Supercycloon Amphan treft Bangladesh, India Onderzoek toont aan hoe licht een isolatiemateriaal in een halfmetaal kan veranderen
Onderzoek toont aan hoe licht een isolatiemateriaal in een halfmetaal kan veranderen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

